
【题目】设NA为阿伏加德罗常数的数值,下列说法不正确的是( )
A.常温常压下,1.7gNH3含有NA个电子
B.标准状况下,22.4L水中含H2O分子NA个
C.1molNa完全反应生成NaCl时,失去NA个电子
D.常温常压下,22.4LCO2中含有的CO2分子数小于NA个
科目:高中化学 来源: 题型:
【题目】已知铜在常温下能被HNO3溶解。反应方程式为: 3Cu+8HNO3=3Cu(NO3)2+2NO ↑+4H2O
(1)请将上述反应改成离子方程式,并用单线桥法表示电子得失的方向和数目__________
(2)若生成448mL的NO(标准状况下),则该过程中转移的电子是___________mol。
(3)被还原的硝酸占参加反应硝酸的比例为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将0.4g NaOH和1.06g Na2CO3混合并配成溶液,向溶液中滴加0.1mol·L-1稀盐酸。下列图像能正确表示加入盐酸的体积和生成CO2的物质的量的关系的是( )
A.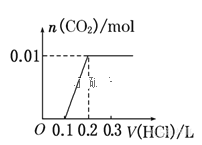 B.
B.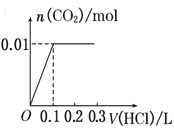
C.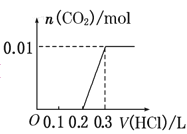 D.
D.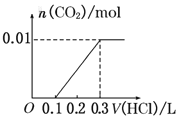
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】炼铁的矿物主要有赤铁矿、磁铁矿和菱铁矿等。目前主要采用以下流程测定铁矿石中铁元素的含量,流程分为两个环节:铁矿石预处理和重铬酸钾滴定。
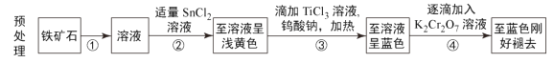
滴定过程:向预处理结束的溶液中加入适量蒸馏水和硫酸磷酸混合酸,滴加数滴二苯胺磺酸钠,用重铬酸钾标准溶液滴定,记录终点体积V。
已知:i.钨酸钠(Na2WO4)可用作指示剂,若钨由+6价变为+5价,则溶液变为蓝色。
ii.Sn2+和Ti3+均具有还原性。
iii.氧化性顺序为Cr2O72->Fe3+>WO42-。
iV.二苯胺磺酸钠可用作氧化还原指示剂,本身无色,被氧化后呈现紫红色。
请回答下列问题:
(1)①过程需要加入过量的___(填试剂名称),试剂过量的理由为___。
(2)②过程后的浅黄色溶液中铁的存在形式为___,③过程后的蓝色溶液中铁的存在形式为___。
(3)④过程中K2Cr2O7的作用为___。
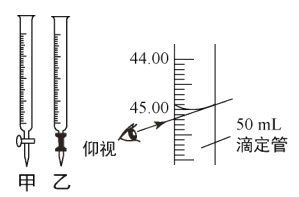
(4)滴定时,滴定管应选用___(填“甲”或“乙”);若滴定结束时,仰视读数,则测得结果___(填“偏大”“偏小”或“无影响”)
(5)滴定过程中,以二苯胺磺酸钠为指示剂,滴定终点观察到的现象为___。
(6)现称取0.4g铁矿石进行测定,滴定时共消耗45.00mL0.01mol·L-1K2Cr2O7溶液,则该铁矿石中铁的质量分数为___ %(保留1位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、M是短周期的四种元素,原子序数依次增大。X和M为同一主族元素,Y的最外层电子数为3,Z是地壳中含量最高的元素,X、Y和M三元素可组成MYX4化合物,其结构式如图所示,下列说法错.误.的是( )
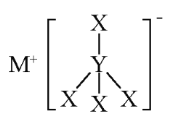
A.MYX4化合物中X的化合价为+1
B.Z与X、M形成的二元化合物均不止一种
C.M在自然界中以化合物形式存在
D.原子半径由大到小顺序为M>Y>Z>X
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨反应是重要的化工反应,请回答下列问题:
(1)①NH3(g)+![]() O2(g)
O2(g)![]() NO2(g)+
NO2(g)+![]() H2O(g) △H=-299.6kJ·mol-1
H2O(g) △H=-299.6kJ·mol-1
②H2(g)+![]() O2(g)=H2O(g) △H=-241.8kJ·mol-1
O2(g)=H2O(g) △H=-241.8kJ·mol-1
③N2(g)+2O2(g)=2NO2(g) △H=+33.9kJ·mol-1
由上述反应,可求出N2(g)+3H2(g)![]() 2NH3(g)的△H=___。
2NH3(g)的△H=___。
(2)对于反应①,在恒温恒容(H2O为气态)的容器中,下列选项表明反应已达到平衡的是___。
A.混合气体的平均摩尔质量不变
B.混合气体的密度不变
C.气体的颜色不再变化
D.体系内压强不再变化
E.每消耗1molNH3的同时生成1molNO2
(3)已知:N2(g)+3H2(g)![]() 2NH3(g)反应的熵变△S=-0.081kJ·mol-1·K-1,则298K时,该反应___(填“能”或“不能”)自发进行。
2NH3(g)反应的熵变△S=-0.081kJ·mol-1·K-1,则298K时,该反应___(填“能”或“不能”)自发进行。
(4)如图为673K温度下,某合成氨塔里各气体组分压强变化图。
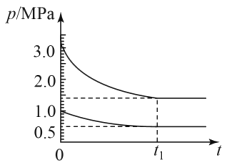
①t1平衡时,氨气的体积分数为___%(保留位小数)。
②在图中画出氨气组分压强变化图___。
③该温度下N2(g)+3H2(g)![]() 2NH3(g)反应的压力平衡常数Kp=___(MPa)-2(保留1位小数,Kp为以气体分压表示反应的平衡常数)
2NH3(g)反应的压力平衡常数Kp=___(MPa)-2(保留1位小数,Kp为以气体分压表示反应的平衡常数)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA表示阿伏加德罗常数的值。俗名为“臭碱”的硫化钠广泛应用千冶金染料、皮革等工业。硫化钠的一种制备方法是Na2SO4+2C![]() Na2S+2CO2↑。下列有关说法正确的是( )
Na2S+2CO2↑。下列有关说法正确的是( )
A.12g石墨晶体中含有碳碳键的数目为3NA
B.1L0.1molL-1Na2S溶液中含阴离子的数目小于0.lNA
C.生成1mol氧化产物时转移电子数为4NA
D.常温常压下,11.2LCO2中含质子的数目为11NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是部分短周期元素的单质及其化合物(或其溶液)的转化关系。已知在常温常压下,A是固体,B、C、D、E是非金属单质且都是气体,C呈黄绿色;化合物F是淡黄色固体,化合物G的焰色反应为黄色,化合物Ⅰ和J通常状况下呈气态;D和E反应生成一种刺激性气味的气体。
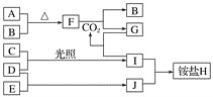
请回答下列问题:
(1)E和J的化学式分别是________和________。
(2)写出F和CO2反应的化学方程式并用单线桥法表示电子转移的情况:_________。
(3)将少量单质C通入盛有淀粉碘化钾溶液的试管中,溶液变蓝色,该反应的离子方程式为_________。
(4)标况下3.36 L气体B与A完全反应,转移电子的数目为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图实验装置用于验证某些物质的性质。在试管A中装入足量的固体NaHCO3。试回答下列问题:

(1)在A试管内发生反应的化学方程式是___________________。
(2)B装置的作用是_____________________。
(3)在双球干燥管内发生反应的化学方程式为______________________。
(4)双球干燥管内观察到的实验现象是____________________________。
上述实验现象说明____________________________。
(5)若将干燥管内的Na2O2换成Na2O,则双球干燥管内观察到的实验现象是_____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com