
| A、将铜屑加入含Fe3+溶液中:Fe3++Cu═Fe2++Cu2+ |
| B、NaOH溶液与氧化铝反应:Al2O3+2OH-═2AlO2-+H2O |
| C、NaHCO3溶液中加入氢氧化钠溶液:HCO3-+OH-═CO2↑+H2O |
| D、向Fe(OH)2中加入足量稀硝酸:Fe(OH)2+2H+═Fe2++2H2O |


科目:高中化学 来源: 题型:
| 正极 | 负极 | 电解质溶液 | |
| A | Zn | Cu | CuCl2 |
| B | Zn | Cu | ZnCl2 |
| C | Cu | Zn | CuSO4 |
| D | Cu | Zn | ZnSO4 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、50 mL 1 mol/L的NaCl |
| B、100 mL 3 mol/L的NH4Cl |
| C、75 mL 2 mol/L的KCl |
| D、75 mL 2 mol/L的CaCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、少量SO2通入NaOH 溶液中:OH-+SO2→HSO3- |
| B、H2S 通入氯水中:S2-+Cl2→S↓+2Cl- |
| C、二氧化氮溶于水:3NO2+H2O=2H++2NO3-+NO↑ |
| D、H2SO4 与Ba(OH)2 溶液反应:H++SO42-+Ba2++OH-→BaSO4↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、硫原子的原子结构示意图: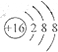 | ||
B、CH4分子的比例模型: | ||
| C、乙烯的结构简式:CH2CH2 | ||
D、原子核内有10个中子的氧原子:
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Cu与AgNO3溶液反应:Cu+Ag+═Cu2++Ag |
| B、Fe与盐酸的反应放出H2:Fe+2H+═Fe2++H2↑ |
| C、大理石与盐酸反应放出CO2气体:CO32-+2H+═CO2↑+H2O |
| D、氢氧化钡溶液与稀 H2SO4 反应:Ba2++SO42-═BaSO4↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 铝生产产业链由铝土矿开采、氧化铝制取、铝的冶炼和铝材加工等环节构成.
铝生产产业链由铝土矿开采、氧化铝制取、铝的冶炼和铝材加工等环节构成.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com