
ЁОЬтФПЁПгаЛњЛЏКЯЮяPЪЧКЯГЩПЙжзСівЉЮяЕФжаМфЬхЃЌЦфКЯГЩТЗЯпШчЯТЃК

вбжЊЃК ![]()
(1)AПЩгыNaHCO3ШмвКЗДгІЃЌаДГіAЕФЙйФмЭХУћГЦ_____ЁЃ
(2)AЁњBЕФЗДгІРраЭ_____ЁЃ
(3)CЁњDЕФЛЏбЇЗНГЬЪН_____ЁЃ
(4)МьбщFжаЙйФмЭХЕФЪдМСМАЯжЯѓ_____ЁЃ
(5)GЁњHЫљашЕФЪдМСaЪЧ______ЁЃ
(6)DЁњEЕФЛЏбЇЗНГЬЪН______ЁЃ
(7)вбжЊЃК
KОЙ§ЖрВНЗДгІзюжеЕУЕНВњЮяPЃК

ЂйLЕФНсЙЙМђЪН___________ЁЃ
ЂкQЁњMЕФЛЏбЇЗНГЬЪН___________ЁЃ
ЁОД№АИЁПєШЛљ ШЁДњЗДгІ HOOC-CH2-COOH+2C2H5OH![]() C2H5OOC-CH2-COOC2H5+2H2O FeCl3ШмвКЁЂШмвКГЪзЯЩЋ(ЛђХЈфхЫЎЁЂЩњГЩАзЩЋГСЕэ) ХЈH2SO4 ЁЂХЈHNO3 C2H5OOC-CH2-COOC2H5+CH(OC2H5)3
C2H5OOC-CH2-COOC2H5+2H2O FeCl3ШмвКЁЂШмвКГЪзЯЩЋ(ЛђХЈфхЫЎЁЂЩњГЩАзЩЋГСЕэ) ХЈH2SO4 ЁЂХЈHNO3 C2H5OOC-CH2-COOC2H5+CH(OC2H5)3![]() (C2H5OOC)2C=CHOC2H5+2C2H5OH
(C2H5OOC)2C=CHOC2H5+2C2H5OH 

ЁОНтЮіЁП
AЗжзгЪНЪЧC2H4O2ЃЌПЩвдгыNaHCO3ШмвКЗДгІЃЌдђAЪЧCH3COOHЃЌAгыCl2дкДпЛЏМСДцдкЪБЗЂЩњМзЛљЩЯЕФШЁДњЗДгІЩњГЩBЃКClCH3COOHЃЌBгыNaCNЁЂH+ДцдкЪБЗЂЩњЗДгІВњЩњCЃКHOOC-CH2-COOHЃЌCгыC2H5OHдкХЈСђЫсДцдкЪБЃЌЗЂЩњѕЅЛЏЗДгІВњЩњDЃКC2H5OOC-CH2COOC2H5ЃЌDгыCH(OC2H5)3ЗЂЩњЗДгІВњЩњEЃК(C2H5OOC)2C=CHOC2H5КЭCH3CH2OHЃЌFЗжзгЪНЪЧC6H6OЃЌНсКЯGЕФЗжзгНсЙЙМАМгШыЕФЮяжЪCH3IЃЌПЩжЊFЪЧБНЗгЃЌGЪЧ![]() ЃЌGгыХЈЯѕЫсЁЂХЈСђЫсЛьКЯМгШШЗЂЩњШЁДњЗДгІЃЌВњЩњHЃК
ЃЌGгыХЈЯѕЫсЁЂХЈСђЫсЛьКЯМгШШЗЂЩњШЁДњЗДгІЃЌВњЩњHЃК![]() ЃЌHБЛЛЙдВњЩњJЃК
ЃЌHБЛЛЙдВњЩњJЃК![]() ЃЛJгыEЗДгІВњЩњKЃК
ЃЛJгыEЗДгІВњЩњKЃК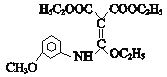 ЃЌKОЙ§вЛЯЕСаБфЛЏВњЩњPЃК
ЃЌKОЙ§вЛЯЕСаБфЛЏВњЩњPЃК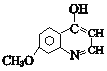 ЃЌОнДЫЗжЮіНтД№ЁЃ
ЃЌОнДЫЗжЮіНтД№ЁЃ
(1) AЪЧCH3COOHЃЌПЩгыNaHCO3ШмвКЗДгІЃЌдђAЕФЙйФмЭХУћГЦЪЧєШЛљЃЛ
(2)AЪЧCH3COOHЃЌAгыCH3IЗЂЩњШЁДњЗДгІВњЩњBЃКClCH2-COOHЃЌдђAЁњBЕФЗДгІРраЭЪЧШЁДњЗДгІЃЛ
(3)CЪЧБћЖўЫсHOOC-CH2-COOHЃЌCгыввДМдкХЈСђЫсДцдкЪБЃЌдкМгШШЬѕМўЯТЗЂЩњѕЅЛЏЗДгІВњЩњDЃКБћЖўЫсЖўввѕЅЃЌC2H5OOC-CH2-COOC2H5ЃЌдђCЁњDЕФЛЏбЇЗНГЬЪНЮЊЃКHOOC-CH2-COOH+2C2H5OH![]() C2H5OOC-CH2-COOC2H5+2H2OЃЛ
C2H5OOC-CH2-COOC2H5+2H2OЃЛ
(4)FЪЧБНЗгЃЌЙйФмЭХЪЧЗгєЧЛљЃЌМьбщFжаЙйФмЭХЕФЪдМСПЩвдЪЧFeCl3ШмвКЃЌЯђШмвКжаМгШыFeCl3ШмвКЃЌШмвКБфЮЊзЯЩЋЃЛвВПЩвдЯђБНЗгШмвКжаМгШыХЈфхЫЎЃЌЛсЙлВьЕНЕФЯжЯѓЪЧЩњГЩАзЩЋГСЕэЃЛ
(5)GЪЧБНМзУб![]() ЃЌЯђЦфжаМгШыХЈЯѕЫсЁЂХЈСђЫсЃЌВЂМгШШЃЌЛсЗЂЩњЁЊOCH3ШЁДњЛљМфЮЛЩЯЕФШЁДњЗДгІЃЌЁЊNO2ШЁДњЁЊOCH3МфЮЛЩЯЕФHдзгЃЌВњЩњHдзгЃЌвђДЫGЁњHЫљашЕФЪдМСaЪЧХЈH2SO4 ЁЂХЈHNO3ЃЛ
ЃЌЯђЦфжаМгШыХЈЯѕЫсЁЂХЈСђЫсЃЌВЂМгШШЃЌЛсЗЂЩњЁЊOCH3ШЁДњЛљМфЮЛЩЯЕФШЁДњЗДгІЃЌЁЊNO2ШЁДњЁЊOCH3МфЮЛЩЯЕФHдзгЃЌВњЩњHдзгЃЌвђДЫGЁњHЫљашЕФЪдМСaЪЧХЈH2SO4 ЁЂХЈHNO3ЃЛ
(6)DЪЧC2H5OOC-CH2-COOC2H5ЃЌDгыCH(OC2H5)3ЗЂЩњЗДгІВњЩњEЃК(H5C2OOC)2C=CHOC2H5КЭCH3CH2OHЃЌдђDЁњEЕФЛЏбЇЗНГЬЪНЪЧC2H5OOC-CH2-COOC2H5+CH(OC2H5)3![]() (H5C2OOC)2C=CHOC2H5+2C2H5OHЃЛ
(H5C2OOC)2C=CHOC2H5+2C2H5OHЃЛ
(7)ЂйKНсЙЙМђЪНЮЊ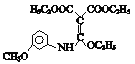 ЃЌИљОнЬтФПаХЯЂПЩжЊKдквЛЖЈЬѕМўЯТЗЂЩњБНЛЗЩЯЕФШЁДњЗДгІВњЩњLЃК
ЃЌИљОнЬтФПаХЯЂПЩжЊKдквЛЖЈЬѕМўЯТЗЂЩњБНЛЗЩЯЕФШЁДњЗДгІВњЩњLЃК ЃЌLгыPOCl3ЗЂЩњЗДгІВњЩњQЃК
ЃЌLгыPOCl3ЗЂЩњЗДгІВњЩњQЃК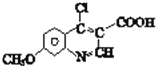 ЃЛ
ЃЛ
ЂкQгыNaOHЫЎШмвКдкМгШШЪБЗЂЩњЗДгІВњЩњMЃК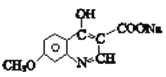 ЃЌQЁњMЕФЛЏбЇЗНГЬЪНЮЊЃК
ЃЌQЁњMЕФЛЏбЇЗНГЬЪНЮЊЃК ЁЃ
ЁЃ


 ШЋгХВтЪдОэЯЕСаД№АИ
ШЋгХВтЪдОэЯЕСаД№АИ ГхДЬ100Зж1КХОэЯЕСаД№АИ
ГхДЬ100Зж1КХОэЯЕСаД№АИ
| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПKIгУгкЗжЮіЪдМСЁЂИаЙтВФСЯжЦвЉКЭЪГЦЗЬэМгМСЕШЁЃ
жЦБИдРэШчЯТЃКЗДгІЂй 3I2+6 KOH =a KIO3+5KI+3H2O
ЗДгІЂк 3H2S+KIO3=3SЁ§+KI+3H2O

АДееЯТСаЪЕбщЙ§ГЬЃЌЧыЛиД№гаЙиЮЪЬтЁЃ
ЃЈ1ЃЉЦєЦеЗЂЩњЦїжаЗЂЩњЕФЛЏбЇЗНГЬЪНЮЊ______________________ЃЌгУИУзАжУЛЙПЩвджЦБИ___________(ЬювЛжжЦјЬхЛЏбЇЪН)ЁЃ
ЃЈ2ЃЉЙиБеЦєЦеЗЂЩњЦїЛюШћЃЌДђПЊЕЮвКТЉЖЗЕФЛюШћЃЌЕЮШы30%ЕФKOHШмвКЃЌД§ЙлВьЕН______________________(ЬюЯжЯѓ)ЃЌЭЃжЙЕЮШЫKOHШмвКЃЛШЛКѓ______________________(ЬюВйзї)ЃЌД§KIO3ЛьКЯвККЭNaOHШмвКЦјХнЫйТЪНгНќЯрЭЌЪБЭЃжЙЭЈЦјЁЃ
ЃЈ3ЃЉЕЮШЫСђЫсШмвКЃЌВЂЖдKIЛьКЯвКЫЎдЁМгШШЃЌЦфФПЕФЪЧ______________________ЁЃ
ЃЈ4ЃЉАбKIЛьКЯвКЕЙШыЩеБЃЌМгШыЬМЫсБЕЃЌдкЙ§ТЫЦїжаЙ§ТЫЃЌЙ§ТЫЕУЕНЕФГСЕэжаГ§КЌгаЙ§СПЬМЫсБЕЭтЃЌЛЙгаСђЫсБЕКЭ___________ЃЌЦфжаМгШыЬМЫсБЕЕФзїгУЪЧ______________________ЁЃКЯВЂТЫвККЭЯДвКЃЌеєЗЂжСЮіГіНсОЇЃЌТЫГіОгкдяЕУГЩЦЗЁЃ
ЃЈ5ЃЉШчЙћЕУЕН3.2gСђЕЅжЪЃЌдђРэТлЩЯжЦЕУЕФKIЮЊ___________gЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЕчРыЦНКтГЃЪ§ЪЧКтСПШѕЕчНтжЪЕчРыГЬЖШЕФЮяРэСПЃЌвбжЊШчБэЪ§Он(25Ёц)ЃК
ЛЏбЇЪН | ЕчРыЦНКтГЃЪ§ |
HCN | K=4.9ЁС10-10 |
CH3COOH | K=1.8ЁС10-5 |
H2CO3 | K1=4.4ЁС10-7ЃЌK2=4.7ЁС10-11 |
(1)25ЁцЪБЃЌЯТСаЮяжЪЕФСПХЈЖШЯрЭЌЕФЫФжжШмвКЕФpHгЩДѓЕНаЁЕФЫГађЮЊ_____(ЬюзжФИЃЌЯТЭЌ)ЁЃ
aЃЎNaCNШмвК bЃЎNa2CO3ШмвК cЃЎCH3COONaШмвК dЃЎNaHCO3ШмвК
(2)25ЁцЪБЃЌЯђNaCNШмвКжаЭЈШыЩйСПCO2ЃЌЫљЗЂЩњЕФЛЏбЇЗНГЬЪНЮЊ____________________ЁЃ
(3)ЕШЮяжЪЕФСПЕФNa2CO3КЭNaHCO3ЛьКЯШмвКжаИїРызгХЈЖШгЩДѓЕНаЁЕФЫГађЮЊ____________________ЁЃ
(4)ЖдгкДзЫсШмвККЭДзЫсФЦШмвКЕФЯТСаЫЕЗЈе§ШЗЕФЪЧ__________ЁЃ
aЃЎЯЁЪЭДзЫсШмвКЃЌДзЫсЕФЕчРыГЬЖШдіДѓЃЌЖјЯЁЪЭДзЫсФЦШмвКдђДзЫсФЦЕФЫЎНтГЬЖШМѕаЁ
bЃЎЩ§ИпЮТЖШПЩвдДйНјДзЫсЕчРыЃЌЖјЩ§ИпЮТЖШЛсвжжЦДзЫсФЦЫЎНт
cЃЎДзЫсКЭДзЫсФЦЕФЛьКЯвКжаЃЌДзЫсДйНјДзЫсФЦЕФЫЎНтЁЂДзЫсФЦвВДйНјДзЫсЕФЕчРы
dЃЎДзЫсКЭДзЫсФЦЕФЛьКЯвКжаЃЌДзЫсвжжЦДзЫсФЦЕФЫЎНтЁЂДзЫсФЦвВвжжЦДзЫсЕФЕчРы
(5)25ЁцЃЌвбжЊpH = 2ЕФИпЕтЫсШмвКгыpH = 12ЕФNaOHШмвКЕШЬхЛ§ЛьКЯЃЌЫљЕУЛьКЯвКЯдЫсадЃЛ0.01 mol/LЕФЕтЫсЛђИпУЬЫсШмвКгыpH = 12ЕФNaOHШмвКЕШЬхЛ§ЛьКЯЃЌЫљЕУЛьКЯвКЯджаадЁЃдђИпЕтЫсЪЧ____________(ЬюЁАЧПЫсЁБЛђЁАШѕЫсЁБ)ЃЛИпУЬЫсЪЧ___________(ЬюЁАЧПЫсЁБЛђЁАШѕЫсЁБ)ЁЃНЋПЩШмадЕФИпЕтЫсБЕ[Ba5(IO6)2]гыЯЁСђЫсЛьКЯЃЌЗЂЩњЗДгІЕФРызгЗНГЬЪНЮЊЃК__________________________________________________ЁЃ
(6)гУЩњЪЏЛвЮќЪеCO2ПЩЩњГЩФбШмЕчНтжЪCaCO3ЃЌЦфШмЖШЛ§ГЃЪ§Ksp=2.8ЁС10-9ЁЃЯжгавЛЮяжЪЕФСПХЈЖШЮЊ2ЁС10-4mol/LДПМюШмвКЃЌНЋЦфгыЕШЬхЛ§ЕФCaCl2ШмвКЛьКЯЃЌдђЩњГЩГСЕэЫљашCaCl2ШмвКЕФзюаЁХЈЖШЮЊ______mol/LЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПгУNAБэЪОАЂЗќйЄЕТТоГЃЪ§ЃЌЯТСаИїбЁЯюжае§ШЗЕФЪЧЃЈ ЃЉ
A.1mol/L Na2CO3ШмвКжаЕФNa+Ъ§ФПЮЊ2NA
B.ЕШжЪСПЕФNO2КЭN2O4ЃЌЧАепдзгЪ§аЁ
C.1L 0.1mol/L NaHCO3ШмвКжаКЌбѕдзгЪ§0.3NA
D.ГЃЮТГЃбЙЯТЃЌ0.2mol CO2ЕФЬхЛ§Дѓгк4.48L
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПHIдквЛЖЈЬѕМўЯТПЩЗЂЩњЗДгІ 2HI(g) ![]() H2 (g)ЃЋI2(g) ЁїHЃЌдк2LКуШнУмБеШнЦїжаЃЌГфШывЛЖЈСПЕФ HI(g)ЃЌЗДгІЮяЕФЮяжЪЕФСП nЃЈmolЃЉЫцЪБМфtЃЈminЃЉБфЛЏЕФЪ§ОнШчЯТЃК
H2 (g)ЃЋI2(g) ЁїHЃЌдк2LКуШнУмБеШнЦїжаЃЌГфШывЛЖЈСПЕФ HI(g)ЃЌЗДгІЮяЕФЮяжЪЕФСП nЃЈmolЃЉЫцЪБМфtЃЈminЃЉБфЛЏЕФЪ§ОнШчЯТЃК

ИљОнБэжаЪ§ОнЃЌЯТСаЫЕЗЈе§ШЗЕФЪЧ
A. ЪЕбщ 1жаЃЌЗДгІдк 0жС 10minФкЃЌv(HI)ЃН0.02molЁЄLЃ1 ЁЄminЃ1
B. 800ЁцЪБЃЌИУЗДгІЕФЦНКтГЃЪ§K=0.25
C. ИљОнЪЕбщ 1КЭЪЕбщ2ПЩЫЕУїЃКЗДгІЮяХЈЖШдНДѓЃЌЗДгІЫйТЪдНПь
D. ЁїH<0
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТБэЮЊЪЕбщЪвФГХЈбЮЫсЪдМСЦПБъЧЉЩЯЕФгаЙиЪ§ОнЃЌЪдИљОнБъЧЉЩЯгаЙиЪ§ОнЛиД№ЯТСаЮЪЬтЃК

(1)ИУХЈбЮЫсжаHClЕФЮяжЪЕФСПХЈЖШЮЊ _________ mol/LЃЛ
(2)ФГбЇЩњгћгУЩЯЪіХЈбЮЫсКЭеєСѓЫЎХфжЦ480mL ЮяжЪЕФСПХЈЖШЮЊ0.400mol/LЕФЯЁбЮЫсЃЌ
ЂйИУбЇЩњашвЊСПШЁ__________ mLЩЯЪіХЈбЮЫсНјааХфжЦЃЛ
ЂкЫљашВЃСЇвЧЦїгаЃКВЃСЇАєЁЂЩеБЁЂСПЭВЁЂ__________ ЁЂ__________ ЃЛ
ЂлдкХфжЦЙ§ГЬжаЃЌЯТСаЪЕбщВйзїЛсЕМжТЫљХфжЦЕФЯЁбЮЫсЕФЮяжЪЕФСПХЈЖШЦЋИпЕФга__________ ЁЃ
A.ЖЈШнЪБЃЌИЉЪгШнСПЦППЬЖШЯпНјааЖЈШнЃЛ
B.дкЩеБжаНЋХЈбЮЫсНјааЯЁЪЭКѓСЂМДзЊШыШнСПЦПЃЛ
C.зЊвЦШмвКЪБЃЌВЛЩїгаЩйСПШмвКШїЕНШнСПЦПЭтУцЃЛ
D.ШнСПЦПгУеєСѓЫЎЯДЕгКѓЮДИЩдяЃЌКЌгаЩйСПеєСѓЫЎЃЛ
E.ЖЈШнвЁдШКѓЃЌЗЂЯжвКУцЕЭгкПЬЖШЯпЃЌдйМгеєСѓЫЎжСПЬЖШЯпЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПУЬЕФЛЏКЯЮядкЙЄвЕЁЂвНСЦЕШСьгђгаживЊгІгУЁЃФГаЫШЄаЁзщФЃФтжЦБИKMnO4МАЬНОПУЬ(II)бЮФмЗёБЛбѕЛЏЮЊИпУЬ(VII)ЫсбЮЁЃ
IЃЎKMnO4ЕФжЦБИЃК
![]()
ЗДгІдРэ
ВНжшвЛЃК3MnO2+6KOH+KClO3![]() 3K2MnO4+KCl+3H2O
3K2MnO4+KCl+3H2O
ВНжшЖўЃК3K2MnO4+2CO2 =2KMnO4+MnO2+2K2CO3
ЪЕбщВйзї
ВНжшвЛЃКНЋвЛЖЈБШР§ЕФMnO2ЁЂKOHКЭKClO3 ЙЬЬхЛьКЯМгШШЃЌЕУЕНФЋТЬЩЋЕФЙЬЬхЃЌРфШДКѓМгЫЎШмНтЕУЕНМюадK2MnO4ШмвКЗХШыЩеБCжаЁЃ
ВНжшЖўЃКСЌНгзАжУЃЌМьВщЦјУмадКѓзАвЉЦЗЁЃДђПЊЗжвКТЉЖЗЛюШћЃЌЕБCжаШмвКЭъШЋБфЮЊзЯКьЩЋЪБЃЌЙиБеЛюШћЭЃжЙЗДгІЃЌЗжРыЁЂЬсДПЛёШЁKMnO4ОЇЬхЁЃ
зАжУЭМШчЯТЃК

(1)МьВщзАжУAЦјУмадЃКЙиБеЗжвКТЉЖЗЛюШћЃЌдкBжаМгШыеєСѓЫЎжСвКУцГЌЙ§ГЄЕМЙмПкЃЌгУШШУЋНэЮцзЁдВЕзЩеЦПЃЌШє__________ЃЌдђЫЕУїзАжУЦјУмадСМКУЁЃ
(2)BжаЪдМСбЁдёЕФРэгЩ________ЁЃ
(3)ЗДгІНсЪјКѓЃЌЮДФмМАЪБЗжРыKMnO4ОЇЬхЃЌЗЂЯжCжазЯКьЩЋШмвКБфЧГЁЃИУаЁзщЭЌбЇШЯЮЊЪЧМюадK2MnO4ШмвКжаЕФCl-НЋЩњГЩЕФMnO4- ЛЙдЃЌЕМжТбеЩЋБфЧГЃЌжИГіКЌгаCl-ЕФХаЖЯвРОн_____________ЁЃ
IIЃЎИУаЁзщМЬајЬНОПMn2+ФмЗёбѕЛЏЮЊMnO4-ЃЌНјааСЫЯТСаЪЕбщЃК
зАжУЭМ | ЪдМСX | ЪЕбщЯжЯѓ |
| Ђй 0.5mL 0.1mol/LNaOHШмвК | ЩњГЩЧГзиЩЋГСЕэЃЌвЛЖЮЪБМфКѓБфЮЊзиКкЩЋ |
Ђк0.5mL 0.1mol/LNaOH КЭ15%H2O2 ЛьКЯвК | СЂМДЩњГЩзиКкЩЋГСЕэ | |
Ђл 0.5mL 0.1mol/LHNO3ШмвК | ЮоУїЯдЯжЯѓ | |
Ђм 0.5mL 0.1 mol/LHNO3ШмвККЭЩйСПPbO2 | ЕЮМгHNO3ЮоУїЯдЯжЯѓЃЌМгШыPbO2СЂМДБфЮЊзЯКьЩЋЃЌЩдКѓзЯКьЩЋЯћЪЇЃЌЩњГЩзиКкЩЋГСЕэ |
вбжЊЃКi.MnO2ЮЊзиКкЩЋЙЬЬхЃЌФбШмгкЫЎЃЛ
iiKMnO4дкЫсадЛЗОГЯТЛКТ§ЗжНтВњЩњMnO2ЁЃ
(4)ЪЕбщЂйжаЩњГЩзиКкЩЋГСЕэПЩФмЕФдвђ_____ЁЃ
(5)ЪЕбщЂкжабИЫйЩњГЩзиКкЩЋГСЕэЕФРызгЗНГЬЪН_____ЁЃ
(6)ЖдБШЪЕбщЂлКЭЂмЃЌЪЕбщЂлЕФзїгУ_____ЁЃ
(7)МзЭЌбЇВТВтЪЕбщЂмжазЯКьЩЋЯћЪЇЕФдвђЃКЫсадЬѕМўЯТKMnO4ВЛЮШЖЈЃЌЗжНтВњЩњСЫMnO2ЃЌввШЯЮЊВЛГЩСЂЃЌРэгЩЪЧ________ЃЛввШЯЮЊЪЧШмвКжаЕФMn2+НЋMnO4- ЛЙдЃЌВЂЩшМЦСЫЪЕбщЗНАИжЄУїДЫЭЦВтГЩСЂЃЌЦфЗНАИЮЊ_________ЁЃ
ЬНОПНсЙћЃКЫсадЬѕМўЯТЯТЃЌФГаЉЧПбѕЛЏМСПЩвдНЋMn2+бѕЛЏЮЊMnO4-ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЪЕбщаЁзщжЦБИНЙбЧСђЫсФЦ(Na2S2O5)ВЂЬНОПЦфаджЪЁЃ
зЪСЯЃКНЙбЧСђЫсФЦЮЊАзЩЋОЇЬхЃЛПЩШмгкЫЎЁЃ
(1)жЦБИNa2S2O5(МаГжзАжУТд)

Ђй AЮЊSO2ЗЂЩњзАжУЃЌAжаЗДгІЗНГЬЪНЪЧ_____________________________________ЁЃ
Ђк B жаЮіГіАзЩЋОЇЬхЃЌПЩВЩШЁЕФЗжРыЗНЗЈЪЧ___________________ЁЃ
Ђл НЋЮВЦјДІРэзАжУCВЙГфЭъећВЂБъУїЫљгУЪдМСЁЃ___________________
(2) ЬНОПNa2S2O5ЕФаджЪ
ЪЕбщБрКХ | ЪЕбщВйзїМАЯжЯѓ |
ЪЕбщЂё | ШЁBжаЩйСПАзЩЋОЇЬхгкЪдЙмжаЃЌМгШыЪЪСПеєСѓЫЎЃЌЕУШмвКaЃЌВтЕУШмвКГЪЫсадЁЃ |
ЪЕбщЂђ | ШЁЩйСПШмвКaгкЪдЙмжаЃЌЕЮМгзуСПЧтбѕЛЏБЕШмвКЃЌгаАзЩЋГСЕэЩњГЩЃЌЙ§ТЫКѓЃЌНЋГСЕэЗХШыЪдЙмжаЃЌЕЮМгЙ§СПбЮЫсЃЌГфЗжеёЕДЃЌВњЩњЦјХнЃЌАзЩЋГСЕэШмНтЁЃ |
ЪЕбщIII | ШЁBжаЩйСПАзЩЋОЇЬхгкЪдЙмжаЃЌЕЮМг1mL 2 mol / LЫсадKMnO4ШмвКЃЌОчСвЗДгІЃЌШмвКзЯКьЩЋКмПьЭЪШЅ ЁЃ |
ЪЕбщIV | ШЁBжаЩйСПАзЩЋОЇЬхгкДѓЪдЙмжаМгШШЃЌНЋВњЩњЕФЦјЬхЭЈШыЦЗКьШмвКжаЃЌКьЩЋЭЪШЅЃЛНЋЭЪЩЋКѓЕФШмвКМгШШЃЌКьЩЋЛжИДЁЃ |
Ђй гЩЪЕбщЂёПЩжЊЃЌNa2S2O5ШмгкЫЎЃЌШмвКГЪЫсадЕФдвђ_______________________________________(гУЛЏбЇЗНГЬЪНБэЪО) ЁЃ
Ђк ЪЕбщЂђжаАзЩЋГСЕэЕЮМгЙ§СПбЮЫсЃЌГСЕэШмНтЃЌгУЦНКтдРэНтЪЭдвђ______________________ЁЃ
Ђл ЪЕбщIIIжаОВтЖЈШмвКжаВњЩњMn2+ЃЌИУЗДгІЕФРызгЗНГЬЪНЪЧ_________________________ЁЃ
Ђм ЪЕбщIV жаВњЩњЕФЦјЬхЮЊ____________ЃЌЪЕбщжаРћгУИУЦјЬхЕФ_________ аджЪНјааМьбщЁЃ
Ђн ДгЩЯЪіЪЕбщЬНОПжаЃЌЬхЯжГіNa2S2O5Опга _____________________аджЪЁЃ ( жСЩйЫЕГіСНЕу )ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁП(1) дкЮЂЩњЮязїгУЕФЬѕМўЯТЃЌNH![]() ОЙ§СНВНЗДгІБЛбѕЛЏГЩNO
ОЙ§СНВНЗДгІБЛбѕЛЏГЩNO![]() ЁЃСНВНЗДгІЕФФмСПБфЛЏЪОвтЭМШчЯТЃК
ЁЃСНВНЗДгІЕФФмСПБфЛЏЪОвтЭМШчЯТЃК

Ђй ЕквЛВНЗДгІЪЧ________(ЬюЁАЗХШШЁБЛђЁАЮќШШЁБ)ЗДгІЃЌХаЖЯвРОнЪЧ_______________________ЁЃ
Ђк 1 mol NH4+(aq)ШЋВПбѕЛЏГЩNO3-(aq)ЕФШШЛЏбЇЗНГЬЪНЪЧ__________________________ЁЃ
(2) вбжЊКьСзБШАзСзЮШЖЈЃЌдђЗДгІP4(АзСзЃЌs)ЃЋ5O2(g)===2P2O5(s)ЁЁІЄH1ЃЛ4P(КьСзЃЌs)ЃЋ5O2(g)===2P2O5(s)ЁЁІЄH2ЃЛІЄH1КЭІЄH2ЕФЙиЯЕЪЧІЄH1________ІЄH2 (ЬюЁА>ЁБЁА<ЁБЛђЁАЃНЁБ)ЁЃ
(3) дк298 KЁЂ101 kPaЪБЃЌвбжЊЃК
2H2O(g)===O2(g)ЃЋ2H2(g)ЁЁІЄH1
Cl2(g)ЃЋH2(g)===2HCl(g)ЁЁІЄH2
2Cl2(g)ЃЋ2H2O(g)===4HCl(g)ЃЋO2(g)ЁЁІЄH3
дђІЄH3гыІЄH1КЭІЄH2жЎМфЕФЙиЯЕе§ШЗЕФЪЧ________ЁЃ
AЃЎІЄH3ЃНІЄH1ЃЋ2ІЄH2 BЃЎІЄH3ЃНІЄH1ЃЋІЄH2
CЃЎІЄH3ЃНІЄH1Ѓ2ІЄH2 DЃЎІЄH3ЃНІЄH1ЃІЄH2
ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com