
����Ŀ�� ��25 ��ʱ����a g NH3��ȫ����ˮ���õ�V mL pH��8�İ�ˮ������ð�ˮ���ܶ�Ϊ�� g��cm-3�����ʵ���������Ϊ�������к�NH![]() �����ʵ���Ϊb mol������������һ����ȷ����
�����ʵ���Ϊb mol������������һ����ȷ����
A�����ʵ���������Ϊ����![]() ��100%
��100%
B�����ʵ����ʵ���Ũ��c��![]() mol��L-1
mol��L-1
C����Һ��c(OH-)��![]() mol�� L-1
mol�� L-1
D��������Һ���ټ���V mLˮ��������Һ��������������0.5��
���𰸡�B
��������
���������A����ˮ��Һ����Ϊ����������Һ���ܶ�Ϊ�� gcm-3�����ΪVmL��������Һ����Ϊ��Vg�����ʰ���������Ϊag�����ʵ���������Ϊ��![]() ��100%����A����B��a g NH3�����ʵ���Ϊ��
��100%����A����B��a g NH3�����ʵ���Ϊ��![]() =
=![]() mol����Һ���ΪVmL��������Һ�����ʵ���Ũ��Ϊ��
mol����Һ���ΪVmL��������Һ�����ʵ���Ũ��Ϊ��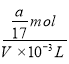 =
=![]() mol/L����B��ȷ��C����ҺOH-��Դ��һˮ�ϰ���ˮ�ĵ��룬NH4+��Ũ��Ϊ��
mol/L����B��ȷ��C����ҺOH-��Դ��һˮ�ϰ���ˮ�ĵ��룬NH4+��Ũ��Ϊ��![]() =
=![]() mol/L��һˮ�ϰ�����NH3H2O
mol/L��һˮ�ϰ�����NH3H2O![]() NH4++OH-��һˮ�ϰ��������OH-Ũ��Ϊ
NH4++OH-��һˮ�ϰ��������OH-Ũ��Ϊ![]() mol/L�����ݵ���غ�ɵã�c(OH-)=
mol/L�����ݵ���غ�ɵã�c(OH-)=![]() molL-1+c(H+)����C����D��ˮ���ܶȴ��ڰ�ˮ���������İ�ˮ��ˮ��ˮ�������������Ϻ���Һ����������ԭ��ˮ��2�������Һ�а�����������ͬ����������������Һ���ʵ���������С��0.5w����D����ѡB��
molL-1+c(H+)����C����D��ˮ���ܶȴ��ڰ�ˮ���������İ�ˮ��ˮ��ˮ�������������Ϻ���Һ����������ԭ��ˮ��2�������Һ�а�����������ͬ����������������Һ���ʵ���������С��0.5w����D����ѡB��


 ������ÿ�ʱ�Ż���ҵϵ�д�
������ÿ�ʱ�Ż���ҵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���¶��£�������X��Y��0.16 mol����10 L�����ܱ������У�������ӦX(g)��Y(g)![]() 2Z(g) ��H��0��һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ���������±���
2Z(g) ��H��0��һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ���������±���
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
����˵����ȷ����( )
A����Ӧǰ2 min��ƽ������v(Z)��2.0��10��3 mol/(L��min)
B�������������䣬�����¶ȣ���Ӧ�ﵽ��ƽ��ǰv�棾v��
C�����¶��´˷�Ӧ��ƽ�ⳣ��K��1.44
D�������������䣬�ٳ���0.2 mol Z��ƽ��ʱX�������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ˵���ȱ���ķǽ�����ǿ��������ʵ�������ݵ���
A. HCl���ܽ���ǿ��H2S
B. �ȵ����Ϊ+7��
C. H2S�е�S2���ܱ�Cl2����
D. HClO��������ǿ��H2SO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����϶�һ�������Ĵ��ѧĿ��֮һ��̽������14��Ԫ���������ϵĺ����ͷֲ���K��Th(��)��U(��)��O��Si��Mg��Al��Ca��Fe��Ti(��)��Na��Mn��Cr(��)��Gd(��)��������������Ԫ�ص���(����)
A. 4�� B. 5�� C. 6�� D. 7��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���100ml0.01mol/LHA����Һ����μ���0.02mol/LMOH��Һ����ͼ��ʾ�����߱�ʾ�����Һ��pH�仯���(��Һ����仯���Բ���)������˵���в���ȷ����

A. HAΪһԪǿ�ᣬMOHΪһԪǿ��
B. N��ˮ�ĵ���̶ȴ���K��ˮ�ĵ���̶�
C. ����MOH��Һ�����Ϊ50mlʱ��c(M+)>c(A-)
D. K��ʱ������c(MOH)+(M+)��0.02mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A. �����������͵�������ȵ�����һ����ԭ��
B. �������������������Ų���ͬ����ѧ���ʾ�һ����ͬ
C. ��������ͬ��ԭ���仯ѧ����һ����ͬ
D. ������ͬ�˵������ԭ�ӻ�����ӣ�һ����ͬ��Ԫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ǹ��÷�չ����Ҫ�������ҹ�Ŀǰʹ�õ���Դ��Ҫ�ǻ�ʯȼ�ϡ�
��1����֪��C(s)+O2(g)=CO2(g)����H����437.3 kJ��mol��1
H2(g)+O2(g)=H2O(g)����H����285.8 kJ��mol��1
CO(g)+O2(g)=CO2(g)����H����283.0 kJ��mol��1
��ú������ӦC(s)+H2O(g)=CO(g)+H2(g)���ʱ���H��________kJ��mol��1��
��2��������ȼ�ϵ�ؾ��иߵķ���Ч�ʣ�����ܵ����ӡ��������ڵ�̼����������ʡ�������ȼ����CH4���ÿ����� CO2 �Ļ������Ϊ��������ȼ������ʯīΪ�缫���ϣ��Ƶ�ȼ�ϵ�ء�����������, CO32-����_________��(����������������) ����֪ CH4 �����ĵ缫��ӦʽΪ CH4 + 4CO32-�D8e-�� 5CO2+2H2O������һ���ĵ缫��Ӧ����ʽΪ��
��3����������ȼ�ϵ�أ�����ͼ��ʾװ�ý��е�⣬A��B��C��D ��Ϊ���缫��

A���ײ�����200mlһ��Ũ�ȵ�NaCl��C uSO4�����Һ��������������������������ʱ��仯�Ĺ�ϵ����ͼ��ʾ(��������ѻ���ɱ�״���µ����)��(���ǰ����Һ������仯��ϵ���Բ���)
��ԭ�����ҺNaCl�����ʵ���Ũ�� mol/L�� CuSO4�����ʵ���Ũ�� mol/L��
��t2ʱ������Һ��pH=___________
B���Ҳ�CuSO4 ��Һ200ml���Ҳ��ڵ����ܻ�ѧ����ʽ________________��
���� C ������ 0.64g ����ʱ���ұ���Һ�����ɵ�����Ϊ_________mol��������ʹ�ҳ��ڵ���Һ��ȫ��ԭ�������ҳ��м���_____________(ѡ����ĸ���)
A��Cu(OH)2 B��CuO C��CuCO3 D��Cu2(OH)2CO3
����ͨ��һ��ʱ��������õ��ұ���Һ�м��� 0.2mol �� Cu(OH)2 ����ǡ�ûָ������ǰ��Ũ�ȣ����������ת�Ƶĵ�����Ϊ______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������Ϊ��ɫ�д̼�����ζ���ж����壬��Һ����������ˮ��ijͬѧ�������ʵ�鷽�����Զ�������Ļ�ѧ���ʽ���̽����װ������ͼ��ʾ����ش��������⣺

��1����Ӧ����ʱ��ƿ��Cu��ʣ�࣬ijͬѧ��ΪH2SO4Ҳ��ʣ�࣬�����������ʵ�鷽�����ⶨʣ��H2SO4����������ȴ������ϡ�ͺ��������ʵ�飬�ܴﵽ��Ŀ���� (�����)
a��������к͵ζ����ⶨ
b��������Zn��Ӧ����������H2�����
c����pH�Ʋ���ҺPHֵ
d��������BaCl2��Һ��Ӧ���������ɳ���������
��2��װ��B�������� �����װ��C��Ŀ������֤SO2�� �ԣ�װ��C�з�����Ӧ�����ӷ���ʽ ��װ��D��NaOHȫ��ת��ΪNaHSO3�ı�־��____________
��3����NaHSO3��Һ�м���NaClO��Һʱ����Ӧ�����ֿ��������
I��HSO3-��ClO-�պ÷�Ӧ�ꣻ ����NaClO���㣻 ����NaClO����
��ͬѧ�ֱ�ȡ���������Һ���Թ��У�ͨ������ʵ��ȷ���÷�Ӧ������һ���������������±���(��֪���ԣ�H2SO3>H2CO3>HClO)
ʵ����� | ʵ����� | ���� | ��Ӧ�Ŀ������ |
�� | ���뼸С��CaCO3���� | �����ݲ��� | |
�� | �μ���������KI��Һ���� | �� | |
�� | �μ�������ˮ���� | �� | |
�� | �������������KMnO4��Һ���� | ��ҺΪ��ɫ |
��4����Ƽ�ʵ��֤����������HSO3-�ĵ���ƽ�ⳣ��Ka��ˮ��ƽ�ⳣ��Kb����Դ�С ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���� 700��ʱ�����ݻ�Ϊ 2 L ���ܱ������г���һ������ CO �� H2O��������Ӧ��CO(g) + H2O(g) ![]() CO2(g)+ H2(g)����Ӧ�����вⶨ�IJ������ݼ��±�(���� t2 > t1)��
CO2(g)+ H2(g)����Ӧ�����вⶨ�IJ������ݼ��±�(���� t2 > t1)��
��Ӧʱ��/min | n(CO)/mol | n(H2O)/mol |
0 | 1.20 | 0.60 |
t1 | 0.80 | |
t2 | 0.20 |
����˵������ȷ����
A����Ӧ�� t1 min �ڵ�ƽ����Ӧ����Ϊ��(CO2) = ![]() mol/(L��min)
mol/(L��min)
B���� t1 min ʱ����Ӧδ�ﵽƽ��״̬
C���¶����� 800��ʱ��������Ӧ��ƽ�ⳣ��Ϊ 0.64��������ӦΪ���ȷ�Ӧ
D������ 700�����䣬��ƽ����ϵ����ͨ�� 0.60 mol CO �� 0.30 mol H2O���ﵽ�µ�ƽ�⣬��ԭƽ����ȣ�CO��ת��������H2 �������������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com