
(一)(4分)括号中的物质是杂质,写出除去这些杂质的试剂:
(1)MgO (Al2O3) (2)Cl2(HCl)
(3)FeCl3(FeCl2) (4)NaHCO3溶液(Na2CO3)
(二)(6分)海水中含有大量的氯化镁,从海水中提取镁的生产流程如下图所示:
回答下列问题:
写出在海水中加入氧化钙生成氢氧化镁的化学方程式 ;
操作①主要是指 ;试剂①可选用 ;
操作②是指 ;经操作③最终可得金属镁。
(三)(8分)实验室配制480ml 0.1mol·L-1的Na2CO3溶液,回答下列问题:
(1)应用托盘天平称取十水碳酸钠晶体 g。
(2)如图所示的仪器配制溶液肯定不需要的是 (填序号),本实验所需玻璃仪器E规格为 mL。
(3)容量瓶上标有:①温度、②浓度、③容量、④压强、⑤刻度线、⑥酸式或碱式这六项中的 。(填数字符号)
(4)配制所需的主要仪器是:a容量瓶、b烧杯、c胶头滴管、d托盘天平,它们在操作过程中使用的前后顺序是 。(填写字母,每种仪器只能选择一次)
(5)玻璃棒是化学实验中常用的一种玻璃工具,则在配制溶液的过程中玻璃棒共起到了
种用途。(填写数字)
(6)若实验时遇到下列情况,将使溶液的浓度偏低的是 。
| A.配制前没有将容量瓶中的水除尽; | B.碳酸钠失去了部分结晶水; |
| C.碳酸钠晶体不纯,其中混有氯化钠; | D.称量碳酸钠晶体时所用砝码生锈; |
(一)(4分)(1) NaOH溶液 (2)饱和NaCl溶液 (3)Cl2(4)CO2 (每格1分)
(二)(6分)CaO+H2O+MgCl2=Mg(OH)2+CaCl2(2分)过滤(1分) HCl(1分)
蒸发浓缩,冷却结晶,过滤(2分)
(三)(8分)(1)14.3;(2)AC 500 (3)①③⑤
(4)dbac (5)2 (6)CE (第(6)题2分,其它每格1分,共8分)
解析试题分析:(一)(1)Al2O3与NaOH溶液反应生成偏铝酸钠溶液过滤即可。(2)Cl2在饱和NaCl溶液中溶解度小。(3)FeCl2用Cl2氧化。(4)Na2CO3与CO2反应生成碳酸氢钠溶液。
(二)海水中加入氧化钙:CaO+H2O+MgCl2=Mg(OH)2+CaCl2,分离出氢氧化镁固体要过滤,氢氧化镁要转化为氯化镁必须要加HCl,氯化镁得到固体氯化镁需要蒸发浓缩,冷却结晶,过滤。
(三)(1)配制480ml 0.1mol·L-1的溶液常选用500mL的容量瓶,则Na2CO3的物质的量是0.05mol,称取十水碳酸钠晶体质量是0.05×(106+180)g=14.3g。(2)肯定不要平底烧瓶和分液漏斗。(3)容量瓶上标有:①温度、③容量、⑤刻度线;(4)配制步骤可概括为:一算(计算);二称;三溶(溶解) 四转(转移) 五洗(洗涤) 六定(定容) 七摇(摇匀);八装(装瓶);九贴(贴标签);则顺序是dbac。(5)玻璃棒在溶解时搅拌,在转移时的引流作用,2种作用。(6)配制前没有将容量瓶中的水除尽,不影响;B项碳酸钠失去了部分结晶水,则浓度升高;C项碳酸钠晶体不纯,其中混有氯化钠,浓度偏低;D项称量碳酸钠晶体时所用砝码生锈,则称量的固体多,浓度偏高;E项定容时仰视刻度线,体积偏大,浓度偏小。
考点:考查了用化学方法除杂,海水提取镁,溶液的配制等。
点评:虽然考查点较多,但都是简单、基础的操作方法,属于简单题。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:







 由甲苯与氯气在光照条件下反应生成,甲苯在工业上可通过下列流程获得:
由甲苯与氯气在光照条件下反应生成,甲苯在工业上可通过下列流程获得: 请在括号中填写加工方法或操作名称
请在括号中填写加工方法或操作名称查看答案和解析>>
科目:高中化学 来源:2015届山东省聊城市高一上学期七校联考期末检测化学试卷(解析版) 题型:实验题
(一)(4分)括号中的物质是杂质,写出除去这些杂质的试剂:
(1)MgO (Al2O3) (2)Cl2(HCl)
(3)FeCl3(FeCl2) (4)NaHCO3溶液(Na2CO3)
(二)(6分)海水中含有大量的氯化镁,从海水中提取镁的生产流程如下图所示:
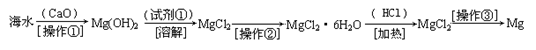
回答下列问题:
写出在海水中加入氧化钙生成氢氧化镁的化学方程式 ;
操作①主要是指 ;试剂①可选用 ;
操作②是指 ;经操作③最终可得金属镁。
(三)(8分)实验室配制480ml 0.1 mol·L-1的Na2CO3溶液,回答下列问题:
(1)应用托盘天平称取十水碳酸钠晶体 g。
(2)如图所示的仪器配制溶液肯定不需要的是 (填序号),本实验所需玻璃仪器E规格为 mL。
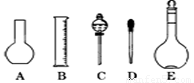
(3)容量瓶上标有:①温度、②浓度、③容量、④压强、⑤刻度线、⑥酸式或碱式这六项中的 。(填数字符号)
(4)配制所需的主要仪器是:a容量瓶、b烧杯、c胶头滴管、d托盘天平,它们在操作过程中使用的前后顺序是 。(填写字母,每种仪器只能选择一次)
(5)玻璃棒是化学实验中常用的一种玻璃工具,则在配制溶液的过程中玻璃棒共起到了 种用途。(填写数字)
(6)若实验时遇到下列情况,将使溶液的浓度偏低的是 。
A.配制前没有将容量瓶中的水除尽;
B.碳酸钠失去了部分结晶水;
C.碳酸钠晶体不纯,其中混有氯化钠;
D.称量碳酸钠晶体时所用砝码生锈;
E.定容时仰视刻度线
查看答案和解析>>
科目:高中化学 来源:2015届浙江省台州市高一上学期期中考试化学试卷(解析版) 题型:实验题
(一)(4分)括号中的物质是杂质,写出除去这些杂质的试剂:
(1)MgO (Al2O3) (2)Cl2(HCl)
(3)FeCl3(FeCl2) (4)NaHCO3溶液(Na2CO3)
(二)(6分)海水中含有大量的氯化镁,从海水中提取镁的生产流程如下图所示:

回答下列问题:
写出在海水中加入氧化钙生成氢氧化镁的化学方程式 ;
操作①主要是指 ;试剂①可选用 ;
操作②是指 ;经操作③最终可得金属镁。
(三)(8分)实验室配制480ml 0.1 mol·L-1的Na2CO3溶液,回答下列问题:
(1)应用托盘天平称取十水碳酸钠晶体 g。
(2)如图所示的仪器配制溶液肯定不需要的是 (填序号),本实验所需玻璃仪器E规格为 mL。

(3)容量瓶上标有:①温度、②浓度、③容量、④压强、⑤刻度线、⑥酸式或碱式这六项中的 。(填数字符号)
(4)配制所需的主要仪器是:a容量瓶、b烧杯、c胶头滴管、d托盘天平,它们在操作过程中使用的前后顺序是 。(填写字母,每种仪器只能选择一次)
(5)玻璃棒是化学实验中常用的一种玻璃工具,则在配制溶液的过程中玻璃棒共起到了
种用途。(填写数字)
(6)若实验时遇到下列情况,将使溶液的浓度偏低的是 。
A. 配制前没有将容量瓶中的水除尽; B. 碳酸钠失去了部分结晶水;
C. 碳酸钠晶体不纯,其中混有氯化钠; D. 称量碳酸钠晶体时所用砝码生锈;
E. 定容时仰视刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
(4分)括号中的物质是杂质,写出除去这些杂质的试剂:
(1)MgO (Al2O3) (2)Cl2(HCl)
(3)FeCl3(FeCl2) (4)NaHCO3溶液(Na2CO3)
(二)(6分)海水中含有大量的氯化镁,从海水中提取镁的生产流程如下图所示:

回答下列问题:
写出在海水中加入氧化钙生成氢氧化镁的化学方程式 ;
操作①主要是指 ;试剂①可选用 ;
操作②是指 ;经操作③最终可得金属镁。
(三)(8分)实验室配制480ml 0.1 mol·L-1的Na2CO3溶液,回答下列问题:
(1)应用托盘天平称取十水碳酸钠晶体 g。
(2)如图所示的仪器配制溶液肯定不需要的是 (填序号),本实验所需玻璃仪器E规格为 mL。

(3)容量瓶上标有:①温度、②浓度、③容量、④压强、⑤刻度线、⑥酸式或碱式这六项中的 。(填数字符号)
(4)配制所需的主要仪器是:a容量瓶、b烧杯、c胶头滴管、d托盘天平,它们在操作过程中使用的前后顺序是 。(填写字母,每种仪器只能选择一次)
(5)玻璃棒是化学实验中常用的一种玻璃工具,则在配制溶液的过程中玻璃棒共起到了
种用途。(填写数字)
(6)若实验时遇到下列情况,将使溶液的浓度偏低的是 。
A. 配制前没有将容量瓶中的水除尽; B. 碳酸钠失去了部分结晶水;
C. 碳酸钠晶体不纯,其中混有氯化钠; D. 称量碳酸钠晶体时所用砝码生锈;
E. 定容时仰视刻度线
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com