
【题目】pH=3的HF和pH=11的NaOH溶液等体积混合后,溶液显________,溶液中的离子浓度大小关系是_________。
【答案】酸 c(F-)>c(Na+)>c(H+)>c(OH-)
【解析】
氢氟酸是弱酸,在溶液中存在电离平衡,根据与NaOH溶液混合后溶液中溶质成分判断溶液酸碱性,并比较离子浓度大小。
氢氟酸是弱酸,在溶液中存在电离平衡HF![]() H++F-,pH=3的HF溶液中,c(HF)>10-3 mol/L,pH=11的NaOH溶液中c(OH-)=10-3 mol/L,二者等体积混合后,电离的HF与NaOH恰好中和,溶液中还有过量的HF,溶液为HF与NaF的混合溶液,HF进一步电离产生H+、F-,使溶液显酸性,所以c(H+)>c(OH-),c(F-)>c(Na+),盐电离产生的离子浓度大于弱电解质电离产生的离子浓度,c(Na+)>c(H+),故溶液中离子浓度关系为:c(F-)>c(Na+)>c(H+)>c(OH-)。
H++F-,pH=3的HF溶液中,c(HF)>10-3 mol/L,pH=11的NaOH溶液中c(OH-)=10-3 mol/L,二者等体积混合后,电离的HF与NaOH恰好中和,溶液中还有过量的HF,溶液为HF与NaF的混合溶液,HF进一步电离产生H+、F-,使溶液显酸性,所以c(H+)>c(OH-),c(F-)>c(Na+),盐电离产生的离子浓度大于弱电解质电离产生的离子浓度,c(Na+)>c(H+),故溶液中离子浓度关系为:c(F-)>c(Na+)>c(H+)>c(OH-)。


科目:高中化学 来源: 题型:
【题目】工业制氢气的一个重要反应是:CO(g)+H2O(g)=CO2(g)+H2(g)。
已知在25℃时:①C(s)+![]() O2(g)
O2(g)![]() CO(g) H4=-111kJ/mol
CO(g) H4=-111kJ/mol
②H2(g)+![]() O2(g)=H2(g) H2=-242kJ/mol
O2(g)=H2(g) H2=-242kJ/mol
③C(s)+O2(g)=CO2(g) H2=-394kJ/mol
下列说法不正确的是( )
A.25℃时,![]()
B.增大压强,反应①的平衡向逆反应方向移,平衡常数K减小
C.反应①达到平衡时,每生成![]() 的同时生成0.5molO2
的同时生成0.5molO2
D.反应②断开2molH2和1molO2中的化学键所吸收的能量比形成4molO-H键所放出的能量少484kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】芳香化合物A是一种基本化工原料,可以从煤和石油中得到。OPA是一种重要的有机化工中间体。A、B、C、D、E、F和OPA的转化关系如图所示:

已知:2
回答下列问题:
(1)A的化学名称是____,B中官能团的名称是____,由A生成B的反应类型是____ 。
(2)写出C所有可能的结构简式____;
(3)D(邻苯二甲酸二乙酯)是一种增塑剂。请用A及不超过两个碳原子的有机物及合适的无机试剂为原料,经两步反应合成D。其合成路线为:_____;
(合成路线流程图示例如下:H2C=CH2![]() CH3CH3Br
CH3CH3Br![]() CH3CH2OH)
CH3CH2OH)
(4)由E可合成一种聚酯类高分子化合物F。
①1molE与足量饱和NaHCO3溶液反应可放出____LCO2(标况);
②由E合成F的反应类型为____,该反应的化学方程式为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年诺贝尔化学奖授予锂离子电池的发明者,LiFePO4是锂离子电池的正极材料。用含锂废渣(主要金属元素的含量:Li 8.50%、Ni 6.55%、Mg 13.24%)制备Li2C2O4,并用其制备LiFePO4部分工艺流程如图(该流程可能造成水体砷污染):
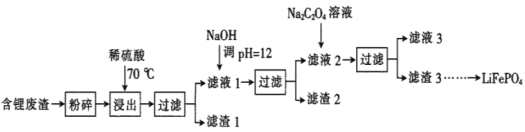
已知:滤液1、滤液2中部分离子的浓度(g·L-1):
Li+ | Ni2+ | Mg2+ | |
滤液1 | 22.72 | 20.68 | 60.18 |
滤液2 | 21.94 | 7.7×10-3 | 0.78×10-3 |
I.制备Li2C2O4
(1)滤渣2的主要成分有__(填化学式)。
(2)Na2C2O4溶液中各离子的浓度由大到小顺序为__。
(3)写出加入Na2C2O4溶液时发生反应的离子方程式:__。
Ⅱ.制备LiFePO4
(4)将电池极Li2C2O4和FePO4置于高温下反应生成LiFePO4和一种温室气体,该反应的化学方程式是___。
(5)LiFePO4需要在高温下成型后才能作为电极,高温成型时要加入少量石墨,则石墨的作用是__(任写一点)。
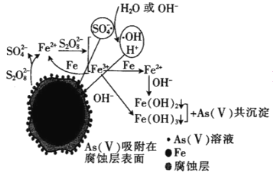
(6)我国科学家研究零价铁活化过硫酸钠(Na2S2O8)去除废水中的As(Ⅴ),其机制模型如图,其中零价铁与过硫酸钠反应的离子方程式是__。在该模型中得到的铁砷共沉淀物经灼烧(无元素化合价变化)后得到一种磁性化合物,化学式为Fe7As2O14,该物质中二价铁与三价铁的个数比为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是某化学兴趣小组设计的乙醇氧化的实验装置(图中加热仪器、铁架台、试管夹均未画出)。图中A处为无水乙醇(沸点为78℃),B处为绕成螺旋状的细铜丝或银丝,C处为无水CuSO4粉末,D处为碱石灰,F处为新制的碱性Cu(OH)2悬浊液。
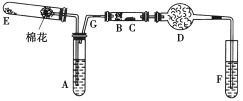
(1)在上述装置中,实验需要加热的仪器按加热的先后顺序排列为_______(填代号)。E处是一种纯净物,其发生的化学反应方程式为__________。
(2)为使A中乙醇平稳地汽化成乙醇蒸气,常用的方法是____________。D处使用碱石灰的作用是________________。
(3)能证明乙醇反应后所生成的产物的现象是___________。
(4)图中G导管倾斜的作用是____________。
(5)本实验中若不加热E处,其他操作不变,则发现C处无明显变化,而F处现象与(3)相同,B处发生反应的化学方程式为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环丙烷可作为全身麻醉剂,环已烷是重要的有机溶剂,下面是部分环烷烃及烷烃衍生物的 结构简式、键线式和某些有机化合物的反应式(其中 Pt、Ni 是催化剂)。

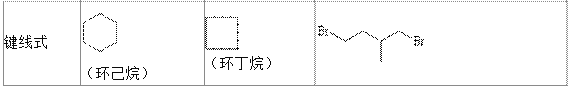
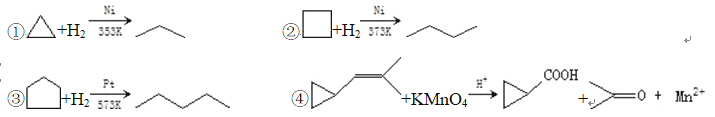
回答下列问题:
(1)环烷烃与____________是同分异构体。
(2)从反应①~③可以看出,最容易发生开环加成反应的环烷烃是____________(填名称)。判断依 据为____________。
(3)环烷烃还可以与卤素单质,卤化氢发生类似的开环加成反应,如环丁烷与 HBr 在一定条件下反 应,其化学方程式为____________(不需注明反应条件)。
(4)写出鉴别环丙烷和丙烯的一种方法.试剂____________;现象与结论____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从葡萄籽中提取的原花青素结构如图,具有生物活性,如抗氧化和自由基清除能力等。有关原花青素的下列说法不正确的是
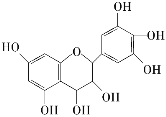
A. 该物质可以看作醇类,也可看做酚类
B. 1 mol该物质可与4 mol Br2反应
C. 1 mol该物质可与7 mol NaOH反应
D. 1 mol该物质可与7 mol Na反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,取0.1mol/L的NaA和NaB两种盐溶液各1L,分别通入0.02molCO2,发生如下反应:NaA+CO2+H2O=HA+NaHCO3、2NaB+CO2+H2O=2HB+Na2CO3。HA和HB的1L溶液分别加水稀释至体积为VL时可能有如图曲线,则下列说法正确的是
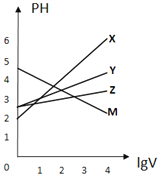
A. 相同条件下,对于c(R-)/[c(HR)·c(OH-)]的值(R代表A或B),一定存在HA>HB
B. 常温下pH:NaA溶液>NaB溶液
C. X是HA,M是HB
D. 若常温下浓度均为0.1mol/L的NaA和HA的溶液等体积混合,则c(A-)+c(HA)=0.2mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com