
【题目】乙酸乙酯广泛用于药物、染料、香料等工业,中学化学实验常用装置来制备. 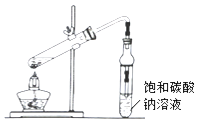
完成下列填空:
(1)铁架台上的试管中发生的反应方程式是 .
(2)饱和Na2CO3溶液的作用是 .
(3)反应结束后,将试管中收集到的产品倒入分液漏斗中,、 , 然后分液.
【答案】
(1)CH3COOH+CH3CH2OH ![]() CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O
(2)溶解乙醇、吸收乙酸,降低乙酸乙酯在水中的溶解度
(3)振荡;静置分层
【解析】解:(1)乙酸与乙醇在浓硫酸作用下发生酯化反应生成乙酸乙酯和水,反应为CH3COOH+CH3CH2OH ![]() CH3COOCH2CH3+H2O,
CH3COOCH2CH3+H2O,
所以答案是:CH3COOH+CH3CH2OH ![]() CH3COOCH2CH3+H2O;(2)饱和Na2CO3溶液的作用是溶解乙醇、吸收乙酸,降低乙酸乙酯在水中的溶解度,便于分层,
CH3COOCH2CH3+H2O;(2)饱和Na2CO3溶液的作用是溶解乙醇、吸收乙酸,降低乙酸乙酯在水中的溶解度,便于分层,
所以答案是:溶解乙醇、吸收乙酸,降低乙酸乙酯在水中的溶解度;(3)反应结束后,将试管中收集到的产品倒入分液漏斗中,振荡、静置分层,然后分液,
所以答案是:振荡;静置分层.


科目:高中化学 来源: 题型:
【题目】下列电离方程式书写正确的是: ( )
A.CuCl2 = Cu + Cl2 ↑B.HI = H++I-
C.H2SO4 = 2H++SO4-2D.NaHCO3 = Na++H++CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳酸亚铁(白色固体,难溶于水)是一种重要的工业原料,可用于制备补血剂乳酸亚铁,也可用作可充电电池的电极。某研究小组通过下列实验,寻找利用复分解反应制备FeCO3的最佳方案:
实验 | 试剂 | 现象 | |
滴管 | 试管 | ||
| 0.8 mol/L FeSO4溶液 (pH=4.5) | 1 mol/L Na2CO3溶液 (pH=11.9) | 实验Ⅰ:立即产生灰绿色沉淀,5min后出现明显的红褐色 |
0.8 mol/L FeSO4溶液 (pH=4.5) | 1 mol/L NaHCO3溶液 (pH=8.6) | 实验Ⅱ:产生白色沉淀及少量无色气泡,2min后出现明显的灰绿色 | |
0.8 mol/L (NH4)2Fe(SO4)2 溶液(pH=4.0) | 1 mol/L NaHCO3溶液 (pH=8.6) | 实验Ⅲ:产生白色沉淀及无色气泡,较长时间保持白色 | |
(1)实验I中红褐色沉淀产生的原因可用如下反应表示,请补全反应:_____________
![]() Fe2++
Fe2++ ![]() +
+ ![]() +
+ ![]() H2O
H2O ![]()
![]() Fe(OH)3 +
Fe(OH)3 + ![]() HCO3
HCO3
(2)实验II中产生FeCO3的离子方程式为__________________。
(3)为了探究实验III中NH4+所起的作用,甲同学设计了实验IV进行探究:
操作 | 现象 | |
实验IV | 向0.8 mol/L FeSO4溶液中加入________,再加入一定量Na2SO4固体配制成混合溶液(已知Na+对实验无影响,忽略混合后溶液体积变化)。再取该溶液一滴管,与2mL 1mol/L NaHCO3溶液混合 | 与实验III现象相同 |
实验IV中加入Na2SO4固体的目的是_________。
对比实验II、III、IV,甲同学得出结论:NH4+水解产生H+,降低溶液pH,减少了副产物Fe(OH)2的产生。
乙同学认为该实验方案不够严谨,应补充的对比实验操作是:_________,再取该溶液一滴管,与2mL 1mol/L NaHCO3溶液混合。
(4)小组同学进一步讨论认为,定性实验现象并不能直接证明实验III中FeCO3的纯度最高,需要利用如图所示的装置进行定量测定。分别将实验I、II、III中的沉淀进行过滤、洗涤、干燥后称量,然后转移至A处的广口瓶中。

① 补全A中装置并标明所用试剂。____________
② 为测定FeCO3的纯度,除样品总质量外,还需测定的物理量是____________。
(5)实验反思:经测定,实验III中的FeCO3纯度高于实验I和实验II。通过以上实验分析,制备FeCO3实验成功的关键因素是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.摩尔是七个基本物理量之一
B.1 mol任何物质都含有6.02×1023个分子
C.标准状况下,1 mol任何物质体积均为22.4 L
D.摩尔质量在数值上等于该物质的相对分子质量或相对原子质量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学在环境保护中起着十分重要的作用,电化学降解NO3-的原理如图所示。下列说法不正确的是( )
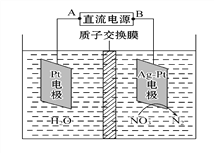
A. A为电源的正极
B. 溶液中H+从阳极向阴极迁移
C. 电解过程中,每转移2 mol电子,则左侧电极就产生32gO2
D. Ag-Pt电极的电极反应式为2NO3-+12H++10e- = N2↑+ 6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关热化学方程式的表示及说法正确的是( )
A.已知2H2(g)+O2(g)=2H2O(g)△H=﹣483.6kJ/mol,则氢气的燃烧热为241.8kJ/mol
B.含20.0g NaOH的稀溶液与稀硫酸完全中和,放出28.7kJ的热量,则表示该反应中和热的热化学方程式为:NaOH(aq)+ ![]() H2SO4 (aq)=NaCl(aq)+H2O(l)△H=﹣57.4kJ/mol
H2SO4 (aq)=NaCl(aq)+H2O(l)△H=﹣57.4kJ/mol
C.已知C(石墨,s)=C(金刚石,s)△H>0,则金刚石比石墨稳定
D.已知I2(g)+H2(g)=2HI(g)△H1<0;I2(s)+H2(g)=2HI(g )△H2<0,则△H1>△H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁及其化合物与生产、生活关系密切.已知t℃时,反应FeO(s)+CO(g)Fe(s)+CO2(g)的平衡常数K=0.25.若在2L密闭容器中加入0.02mol FeO(s),并通入xmolCO,t℃时反应达到平衡.此时FeO(s)转化率为50%,则x的值为( )
A.0.1
B.0.05
C.0.04
D.0.02
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素a、b、c、d的原子序数之和为45,四种元素均位于不同主族。a的最高正价和最低负价代数和等于0;b单质可作半导体材料;d的气态氢化物与其最高价含氧酸都是强酸。下列说法正确的是
A. 四种元素中b的非金属性最强 B. 原子半径:c>b
C. 最简单氢化物的稳定性:b>d D. 化合物bad3中存在离子键和极性键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com