
【题目】氟化铬可用作毛织品防蛀剂、卤化催化剂、大理石硬化及着色剂。以铬云母矿石(含4.5%Cr2O3,还含Fe2O3、FeO、MgO、SiO2)为原料制备氟化铬的工艺流程如图。
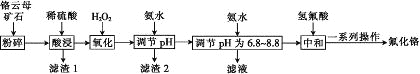
表中列出了相关金属离子生成氢氧化物沉淀的pH:
氢氧化物 | Fe(OH)3 | Mg(OH)2 | Cr(OH)3 | Fe(OH)2 |
开始沉淀的pH | 2.3 | 8.8 | 4.9 | 7.5 |
沉淀完全的pH | 4.1 | 10.4 | 6.8 | 9.7 |
请回答下列问题:
(1)Fe2O3、MgO、FeO、SiO2中属于碱性氧化物的有________种。
(2)将铬云母矿石粉碎的目的是________。
(3)滤渣1主要成分的用途是________。(写一种)
(4)Cr2O3与稀硫酸反应的化学方程式为___________。
(5)第一次滴加氨水调节pH范围为________。
(6)第二次滴加氨水调节pH为6.8~8.8的目的是_______,Cr(OH)3与 Al(OH)3一样具有两性,若第二次滴加的氨水改为NaOH溶液,生成的Cr(OH)3会部分溶解,写出Cr(OH)3溶解的离子方程式:________。
【答案】3 增大接触面积,提高浸取率,加快浸取速率 用于制备光导纤维 Cr2O3+3H2SO4=Cr2(SO4)3+3H2O 4.1~4.9(或4.1≤pH<4.9) 使Cr3+完全沉淀,Mg2+不沉淀 Cr(OH)3+OH-=Cr(OH)4-或Cr(OH)3+OH-=CrO2-+2H2O
【解析】
将铬云母矿石粉碎后与加入的稀硫酸充分混合,其中金属氧化物反应变为可溶性盐进入溶液,SiO2进入滤渣I中,溶液中通入H2O2可以将溶液中的Fe2+氧化为Fe3+,然后加入氨水调节溶液的4.1<pH<4.9,得到Fe(OH)3沉淀,将沉淀过滤除去后,在继续加入氨水调节溶液的pH为6.8~8.8,就可以使Cr3+形成沉淀,而Mg2+仍然以离子形式存在于溶液中,Cr(OH)3是两性氢氧化物,会与NaOH溶液发生反应而溶解。
(1) Fe2O3、MgO、FeO都会与酸反应产生盐和水,属于碱性氧化物,而SiO2则与酸不能反应,与碱能反应产生盐和水,属于酸性氧化物,属于属于碱性氧化物的有3种;
(2)铬云母矿石是固态物质,将铬云母矿石粉碎的目的是增大反应时遇酸的接触面积,提高酸浸取率,加快浸取速率;
(3)滤渣1主要成分是SiO2,可用于制备光导纤维、制晶体硅、水泥等;
(4)Cr2O3是碱性氧化物与稀硫酸反应产生硫酸铬和水,反应的化学方程式为Cr2O3+3H2SO4=Cr2(SO4)3+3H2O;
(5)向酸浸后的溶液中加入H2O2,可以将Fe2+氧化产生Fe3+,第一次滴加氨水调节pH范围为4.1<pH<4.9,目的是除去溶液中的Fe3+,得到Fe(OH)3沉淀,并将该沉淀过滤除去;
(6)第二次滴加氨水调节pH为6.8~8.8的目的是使Cr3+完全形成Cr(OH)3沉淀,而Mg2+仍然以离子形式存在于溶液中,不产生Mg(OH)2沉淀;Cr(OH)3与 Al(OH)3一样具有两性,若第二次滴加的氨水改为NaOH溶液,生成的Cr(OH)3会部分溶解,则Cr(OH)3与NaOH发生反应而溶解的离子方程式为:Cr(OH)3+OH-=Cr(OH)4-或Cr(OH)3+OH-=CrO2-+2H2O。


科目:高中化学 来源: 题型:
【题目】化合物H是一种有机光电材料中间体。实验室由芳香化合物A制备H的一种合成路线如下:

已知:①RCHO+CH3CHO ![]() RCH=CHCHO+H2O;②
RCH=CHCHO+H2O;②![]() 。
。
回答下列问题:
(1)C的结构简式为_______________________。
(2)F中官能团的名称为___________________。
(3)B与新制Cu(OH)2悬浊液反应的化学方程式为________________。
(4)从转化流程图可见,由D到E分两步进行,其中第一步反应的类型为__________。
(5)化合物G的二氯代物有__________种同分异构体。
(6)芳香化合物X是D的同分异构体,X能发生银镜反应,其核磁共振氢谱显示有3种化学环境的氢,峰面积之比为6∶1∶1,符合条件的X的结构共有多种,任写出2种符合要求的X的结构简式________、___________。
(7)写出用甲醛和乙醛为原料制备化合物CH2=CHCOOCH3的合成路线(其他试剂任选)____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】第三周期X、Y、Z、W四种元素的最高价氧化物溶于水可得到四种溶液,0.010 mol/L的这四种溶液在25℃时的pH与该元素原子半径的关系如图所示。下列说法正确的是
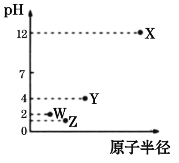
A.简单离子半径:X>Y>Z>W
B.W的氧化物对应的水化物一定是强酸
C.气态氢化物的稳定性:W<Z<Y
D.W与Z可形成一种各原子均达到8电子稳定结构的化合物Z2W2,其结构式为:W-Z-Z-W
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向硫酸铜水溶液中逐滴滴加氨水,先生成蓝色沉淀,继续滴加氨水得到深蓝色溶液,再向溶液中加入乙醇,有深蓝色晶体[Cu(NH3)4]SO4·H2O析出。
(1)铜元素位于元素周期表中____区,高温超导体钇钡铜氧材料中铜元素有+2和+3两种价态,基态Cu3+的电子排布式为____。
(2)非金属元素N、O、S的第一电离能由大到小的顺序是____(用元素符号表示)。
(3)上述深蓝色晶体中含有的元素的电负性最小的是____(用元素符号表示)。
(4)H2O的中心原子轨道杂化类型为____杂化;SO42-离子的立体构型是____,写出与SO42-互为等电子体的一种离子____。
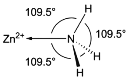
(5)NH3分子在独立存在时H-N-H键角为106.7°。如图为[Zn(NH3)6]2+离子的部分结构以及H-N-H键角的测量值。解释配合物中H-N-H键角变为109.5°的原因____。
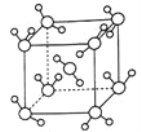
(6)最新研究发现,水能凝结成13种类型的结晶体。除普通冰外,还有-30℃才凝固的低温冰,180℃依然不变的热冰,比水密度大的重冰等。重冰的结构如图所示。已知晶胞参数a=333.7pm,阿伏加德罗常数的值取6.02×1023,则重冰的密度为____g.cm-3(只列式,不计算)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)现有氧化还原反应:3H2O2 + 2H2CrO4 =2Cr(OH)3 + 3O2 ↑+ 2H2O
①用单线桥标出反应中的电子转移数目和方向_____________;
②其中Cr被___________,H2O2作___________剂;
③反应转移了0.3mol电子,则产生的气体在标准状态下体积约为__________。
(2)①将用砂纸打磨过的铝片用坩埚钳夹住在酒精灯上点燃,现象是:________;
②在试管中加入少量Na2O2再加入少量水,用带火星的木条伸入试管,再滴入几滴酚酞,可观察到的现象是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求答题:
(1)向偏铝酸钠溶液中通入足量的CO2离子反应方程式____________;
(2)铝与氢氧化钠溶液化学反应方程式_____________;
(3)将饱和FeCl3溶液滴入沸水中制备氢氧化铁胶体化学反应方程式_________;
(4)向Al2(SO4)3溶液中滴加氨水制备氢氧化铝的离子反应方程式________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室常用盐酸的质量分数为36.5%,密度为1.20 g·mL-1。
(1)此浓盐酸中HCl的物质的量浓度是________。
(2)配制100 mL该浓盐酸,需要标准状况下HCl的体积为________。
(3)配制100 mL 3.00 mol·L-1的盐酸,需以上浓盐酸的体积为________。
(4)将10.0 mL 3.00 mol·L-1的盐酸与10.0 mL 1.00 mol·L-1的MgCl2溶液混合,则混合溶液中Cl-的物质的量浓度是________。(设混合后溶液的体积不变)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将铁粉和活性炭的混合物用NaCl溶液湿润后,置于如图所示装置中,进行铁的电化学腐蚀实验。下列有关该实验的说法正确的是
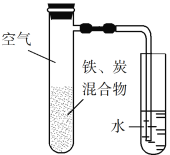
A. 铁被氧化的电极反应式为Fe3e![]() Fe3+
Fe3+
B. 铁腐蚀过程中化学能全部转化为电能
C. 活性炭的存在会加速铁的腐蚀
D. 以水代替NaCl溶液,铁不能发生吸氧腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以A(C2H2)为原料合成食用香料E和吡咯(pyrrole)的路线如图所示,部分反应条件及产物略去。其中D在一定条件下可被氧化成酮。
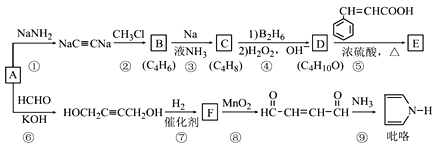
回答下列问题:
(1)A的名称是______;F中含氧官能团的名称是________________。
(2)⑥的反应类型是_____________,⑧的反应类型是_________________。
(3)反应⑤的化学方程式为____________________。
(4)已知C是反式产物,则C的结构简式为_______________。
(5)肉桂酸(![]() )的同分异构体中,含有苯环和碳碳双键,且能够发生水解反应的共有________种(不考虑顺反异构)。与D互为同分异构体,且核磁共振氢谱有面积比为2∶3的两组峰的有机物的结构简式是_________。
)的同分异构体中,含有苯环和碳碳双键,且能够发生水解反应的共有________种(不考虑顺反异构)。与D互为同分异构体,且核磁共振氢谱有面积比为2∶3的两组峰的有机物的结构简式是_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com