
【题目】Ⅰ.已知常温下E为无色无味的液体,F为淡黄色粉末,G为常见的无色气体(反应条件均已略去) ,请回答下列问题:
(1)请写出F的化学式 ;在②反应中,当生成2.24L的G(标准状况)时,反应中转移的电子的物质的量为 moL。
(2)若A、C、D均含有氯元素,且A中的化合价介于C与D之间,写出反应①的离子方程式: 。
(3)若C、D均为气体且都能使澄清石灰水变浑浊,则A与B分别为 、 。(写化学式)
(4)若A与B均为固体化合物,D是一种能使湿润的红色石蕊试纸变蓝的气体,反应①是实验室制备D的反应,则反应①的化学方程式为 。
Ⅱ.A、B、C是中学化学常见的三种物质,它们之间的相互转化关系如下(部分反应产物略去)。
![]()
(1)若A是一种黄色非金属单质固体,则B→C的化学方程式为 。
(2)若A是一种活泼金属,C是淡黄色固体,则C的电子式为 ,写出C和CO2反应的化学方程式,并标出单线桥 。
(3)若A是碱性气体,试写出A与氧气反应的化学方程式 。
【答案】Ⅰ.(1)Na2O2 0.2
(2)Cl2+2OH-=Cl-+ClO-+H2O(3)C、浓H2SO4
(4)2NH4Cl+Ca(OH)2![]() CaCl2+2H2O+2NH3↑(2分)
CaCl2+2H2O+2NH3↑(2分)
Ⅱ.(1)2SO2+O2![]() 2SO3
2SO3
(2)![]()
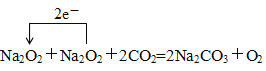
(3)4NH3+5O2![]() 4NO+6H2O
4NO+6H2O
【解析】
试题分析:Ⅰ.已知常温下E为无色无味的液体,则E是水。F为淡黄色粉末,能与E反应,说明F是过氧化钠。G为常见的无色气体(反应条件均已略去) ,因此G是氧气,H是氢氧化钠。
(1)F的化学式为Na2O2;过氧化钠中氧元素的化合价是-1价,反应转化为氧气中的0价,所以在②反应中,当生成2.24L的G(标准状况)即0.1mol氧气时,反应中转移的电子的物质的量为0.2moL。
(2)若A、C、D均含有氯元素,且A中的化合价介于C与D之间,这说明该反应是氯气与碱溶液的反应,则反应①的离子方程式为Cl2+2OH-=Cl- + ClO- +H2O。
(3)若C、D均为气体且都能使澄清石灰水变浑浊,则分别是CO2和SO2,因此A与B分别为C、浓H2SO4。
(4)若A与B均为固体化合物,D是一种能使湿润的红色石蕊试纸变蓝的气体,该气体是氨气,实验室制备氨气的化学方程式为2NH4Cl+Ca(OH)2![]() CaCl2 +2H2O+2NH3↑。
CaCl2 +2H2O+2NH3↑。
Ⅱ.(1)若A是一种黄色非金属单质固体,则A是S,所以B是SO2,C是三氧化硫,因此B→C的化学方程式为2SO2+O2![]() 2SO3。
2SO3。
(2)若A是一种活泼金属,C是淡黄色固体,则A是Na,B是氧化钠,C是过氧化钠,所以C的电子式为![]() ,过氧化钠和CO2反应的化学方程式为
,过氧化钠和CO2反应的化学方程式为
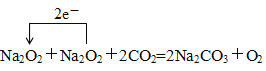 。
。
(3)若A是碱性气体,因此A是氨气,所以B是NO,C是NO2,则A与氧气反应的化学方程式为4NH3+5O2![]() 4NO+6H2O。
4NO+6H2O。


 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源: 题型:
【题目】已知 2SO2(g)+O2(g)2SO3 (g)△H<0,下列说法不正确的是( )
A. 升高温度,正、逆反应速率均加快
B. 增大压强,化学平衡正向移动
C. 当气体总质量不变时,反应达平衡状态
D. 充入O2,可提高SO2的转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在日常生活中,我们经常看到铁制品生锈、铝制品表面出现白斑等众多的金属腐蚀现象。可以通过下列装置所示实验进行探究。下列说法正确的是

A. 按图Ⅰ装置实验,为了更快更清晰地观察到液柱上升,可采用下列方法:用酒精灯加热具支试管
B. 图Ⅱ是图Ⅰ所示装置的原理示意图,图Ⅱ的正极材料是铁
C. 铝制品表面出现白斑可以通过图Ⅲ装置进行探究,Cl-由活性炭区向铝箔表面区迁移,并发生电极反应:2Cl--2e-=Cl2↑
D. 图Ⅲ装置的总反应为4Al+3O2+6H2O=4Al(OH)3,生成的Al(OH)3进一步脱水形成白斑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,可用离子方程式H++OH-= H2O表示的是
A.NH4Cl+NaOH![]() NaCl+NH3↑+H2O
NaCl+NH3↑+H2O
B.Mg(OH)2+2HCl==MgCl2+2H2O
C.NaOH+NaHCO3==Na2CO3+H2O
D.NaOH+HNO3==NaNO3+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E都是短周期的主族元素,原子序数依次增大,A、B处于同周期,C、D、E同处另一周期,C、A可按原子个数比2∶l和1∶1分别形成两种离子化合物甲和乙,D是地壳中含量最高的金属元素,E的最高价氧化物对应的水化物是酸性最强的含氧酸。回答下列问题:
(1)B和E分别对应的氢化物的化学式为HB、HE,氢化物的沸点HB HE(填“>”、“<”、“=”,下同) ,氢化物的稳定性HB HE。
(2)物质乙的电子式为 ;物质乙可用于呼吸面具作供氧剂,写出乙与CO2反应的化学方程式:____________________________ 。
(3)元素C的最高价氧化物对应水化物和D的简单阳离子按照物质的量之比为7︰2在水溶液中反应的离子方程式:______________________________。
(4)1 mol 单质B的气体与1 mol C的氢氧化物在一定条件下恰好完全反应,生成一种盐、水及另一种气体,则所得气体的化学式为:___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 油脂在人体内水解为高级脂肪酸和甘油等物质被吸收
B. 维生素C具有较强还原性,高温烹饪蔬菜会导致维生素C损失
C. 用金属钠在高温下还原TiCl4制取金属钛
D. 纳米铁粉通过物理吸附可除去污水中的Pt2+、Cu2+、Cd2+、Hg2+等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应4NH3(g)+5O2(g)4NO(g)+6H2O(g)在2L的密闭容器中进行,1min后,NH3减少了0.12mol,则平均每秒钟浓度变化正确的是
A.NO:0.06molL﹣1 B.H2O:0.002molL﹣1
C.NH3:0.002molL﹣1 D.O2:0.00125molL﹣1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com