
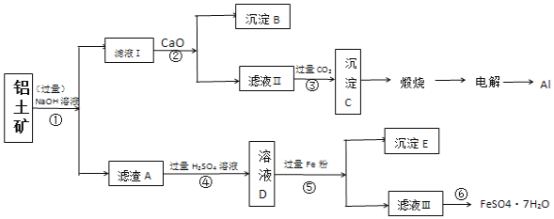
【题目】以铝土矿(主要成分为Al2O3,含SiO2和铁的氧化物等杂质)为原料制备铝与硫酸亚铁,工艺流程如图所示:请回答下列问题:
(1)步骤①中提高碱浸速率的方法_______。
(2)滤液Ⅰ中主要的阴离子是______。
(3)步骤⑤加入过量的铁粉的目的___(用离子方程式解释)
(4)检验滤液Ⅲ中的金属阳离子的方法是:_____。
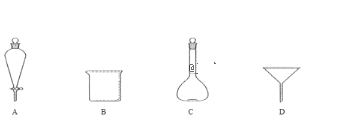
(5)滤液Ⅲ经过蒸发浓缩,_______,过滤得到硫酸亚铁晶体,过滤时需要的玻璃仪器有___(填标号)。
【答案】粉碎铝土矿(升高温度) AlO2-、SiO32- Fe+2Fe3+=3Fe2+ 加入KSCN溶液,无现象,再通入Cl2 ,产生血红色的络合物 冷却结晶 BD
【解析】
铝土矿(主要成分为Al2O3,含SiO2和铁的氧化物等杂质),加入过量NaOH溶液,滤液Ⅰ含有偏铝酸钠、氢氧化钠以及硅酸钠,滤渣A含有铁的氧化物,滤液Ⅰ加入CaO,可生成硅酸钙沉淀,滤液Ⅱ含有偏铝酸钠,通入二氧化碳,生成氢氧化铝沉淀,经煅烧、电解,可得到铝;滤渣A加入稀硫酸,得到溶液D为硫酸铁、硫酸亚铁等,加入过量铁粉得到硫酸亚铁,经蒸发结晶得到FeSO4.7H2O。
(1)提高碱浸速率,可粉碎铝土矿(升高温度)等;
(2)由以上分析可知滤液Ⅰ中主要的阴离子是AlO2-,SiO32-;
(3)步骤⑤加入过量的铁粉可生成亚铁离子,除去铁离子,反应的离子方程式为Fe+2Fe3+=3Fe2+;
(4)滤液Ⅲ中的金属阳离子为亚铁离子,检验方法是加入KSCN溶液,无现象,再通入Cl2,产生血红色的络合物;
(5)滤液Ⅲ经过蒸发浓缩,冷却结晶,过滤得到硫酸亚铁晶体,过滤时需要的玻璃仪器有烧杯、漏斗等,故选BD。


科目:高中化学 来源: 题型:
【题目】1.52 g铜镁合金完全溶解于50 mL 14 mol/L的浓硝酸中,得到NO2和N2O4的混合气体1120 mL(标准状况),向反应后的溶液中加入1.0 mol/L NaOH溶液,当金属离子全部沉淀时,得到2.54 g沉淀。下列说法不正确的是( )
A.该合金中铜与镁的物质的量之比是2:1
B.得到2.54 g沉淀时,加入NaOH溶液的体积是600 mL
C.NO2和N2O4的混合气体中,NO2的体积分数是80%
D.与铜镁合金反应的HNO3的物质的量为0.12 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“化学是人类进步的关键”。下列说法不正确的是 ( )
A.PM2.5是指空气中直径≤2.5 μm的固体颗粒或液滴的总称
B.根据分散质粒子的直径大小,分散系可分为溶液、浊液和胶体,浊液的分散质粒子大小介于溶液与胶体之间
C.科学家发现一种新细菌的DNA链中有砷(As)元素,该As元素最有可能取代了普通DNA链中的P元素
D.![]() 和CO2反应生成可降解聚合物
和CO2反应生成可降解聚合物![]() ,该反应符合绿色化学的原则
,该反应符合绿色化学的原则
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色溶液中含有的阳离子为H+、Na+、Mg2+、Al3+、Ba2+中的一种或几种,向该溶液中缓慢地滴入NaOH溶液直至过量,产生沉淀的质量与加入NaOH溶液的体积的关系如图所示,由此确定原溶液中一定含有的阳离子是

A. Mg2+、Al3+、Na+ B. H+、Mg2+、Al3+ C. H+、Ba2+、Al3+ D. Ba2+、Mg2+、Al3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na2O2是重要的化工原料,具有多种用途。
(1)Na2O2具有氧化性,可以将SO2氧化为硫酸钠,写出该反应的化学方程式:______________,该反应中,Na2O2的作用为____________(填“还原剂”、“氧化剂”或“既是氧化剂又是还原剂”)。
(2)Na2O2与CO2反应可以产生氧气。某同学通过下列装置验证Na2O2能否与CO2反应。 (图中铁架台等装置已略去)。
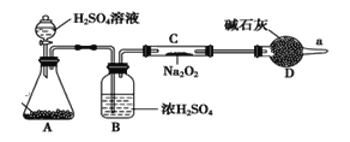
①装置A的名称是_______,A中的固体为_________,装置B中试剂的作用为______
②若Na2O2能与CO2,则装置C中的现象是____________
(3)无水氯化钙是干燥剂,在a处收集气体,检测发现该气体中几乎都是CO2气体(过氧化钠足量),则说明过氧化钠与CO2气体不反应。该同学查阅相关文献,然后撤掉装置B,其他都保留(包括试剂),连接好装置后再次进行实验,重新收集气体检测,发现得到的气体几乎都是氧气,该实验结果说明过氧化钠与CO2气体反应需要_______________。
(4)将一定量的Na2O2固体投入到含有下列离子的溶液中:SO32-、HCO3-、CO32-、Na+,反应完毕后,溶液中上述离子数目几乎不变的有(不考虑溶液体积的变化)__________(填离子符号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 反应A(g)+3B(g)![]() 2C(g)+2D(g),在四种不同情况下用不同物质表示的反应速率
2C(g)+2D(g),在四种不同情况下用不同物质表示的反应速率
分别如下,其中反应速率最大的是( )
A.v(C)=0.04 mol/(L·s)
B.v(B)=0.06 mol/(L·min)
C.v(A)=0.15 mol/(L·min)
D.v(D)=0.01 mol/(L·s)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验结论正确的是( )
A.向某溶液中加入酚酞,溶液不变色,则该溶液一定显酸性
B.向某溶液中加入氯化钡溶液产生白色沉淀,再加入盐酸沉淀不消失,则该溶液中一定有 ![]()
C.向某溶液中加入稀盐酸产生无色无味气体,将气体通入澄清石灰水中,石灰水变浑浊,则原溶液中一定有 ![]()
D.向某溶液中滴加KSCN试剂,溶液变成血红色,则该溶液中一定有Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘化钾是一种无色晶体,易溶于水。实验室制备KI晶体的步骤如下:
Ⅰ.在如下图所示的三颈烧瓶中加入研细的I2和一定量的30%KOH溶液,搅拌(已知:I2与KOH反应产物之一是KIO3);
Ⅱ.碘完全反应后,打开分液漏斗中的活塞、弹簧夹1、2,向装置C中通入足量的H2S;
Ⅲ.反应结束后,向装置C中加入稀H2SO4酸化,水浴加热;
Ⅳ.冷却,过滤得KI粗溶液。
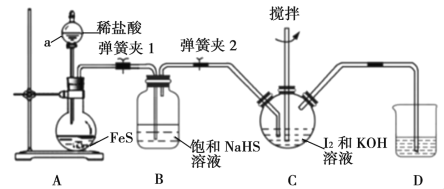
(1)仪器a的名称是__________,步骤Ⅰ中控制KOH溶液过量的目的是______________。
(2)装置B的作用是_____________,装置D中盛放的溶液是________________。
(3)装置C中H2S和KIO3反应的离子方程式为_______________________。
(4)步骤Ⅲ中水浴加热的目的是除去_________________________(填化学式)。
(5)由步骤Ⅳ所得的KI粗溶液中含有少量K2SO4,需进行提纯,提纯流程如下:
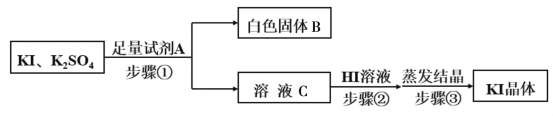
①已知白色固体B是混合物,试剂A为__________,为除去溶液C中的杂质,步骤②中调节溶液为弱酸性,则加入HI溶液后产生的现象是___________________。
②为测定最后所得KI晶体的纯度,取a g晶体配制100mL溶液,取出25mL溶液,滴入足量稀的酸性K2Cr2O7溶液,充分反应后,滴加几滴淀粉溶液为指示剂,用b mol·L-1的Na2S2O3溶液进行滴定,消耗Na2S2O3溶液VmL。
滴定过程中涉及的反应为:![]() ,
,![]() 则滴定终点时的现象为________________________,晶体的纯度为_______________________(列出计算式)。
则滴定终点时的现象为________________________,晶体的纯度为_______________________(列出计算式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国政府为了消除碘缺乏病,规定在食盐中必须加入适量的碘酸钾。检验食盐中是否加碘,可利用如下反应:
KIO3+ KI+ H2SO4═ K2SO4+ I2 + H2O
(1)配平该方程式,并且用双线桥法表示该方程式电子转移的方向与数目:____________________
(2)该反应中氧化剂和还原剂的物质的量之比为______________;
(3)如果反应中转移0.5mol电子,则生成I2的物质的量为____________;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com