
| A、SO2发生还原反应 |
| B、NaClO3失去电子 |
| C、H2SO4作氧化剂 |
| D、1mol氧化剂得到1mol电子 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、该反应体现了浓硫酸的酸性和强氧化性 | ||
| B、应体结束后两两种反应物均有剩余 | ||
C、被还原的硫酸为
| ||
| D、参加反应的Cu为0.9 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A | c(OH-)=1×10-13mol/L溶液中:Fe2+、NO3-、SO42-、Na+ | 不能共存 | 发生反应 3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O |
| B | 溶液中:K+、Cu2+、Cl-、NH3?H2O | 不能共存 | 发生反应Cu2++2OH-=Cu(OH)2↓ |
| C | 常温常压下:NH3、O2、H2、CO2 | 不能共存 | NH3为碱性气体,CO2为酸性气体,二者反应生成(NH4)2CO3 |
| D | 溶液中:Al3+、Na+、SO42-、HCO3- | 可以共存 | 不能发生反应 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
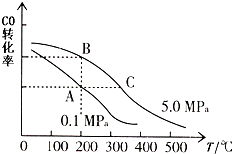 (1)在电化学中,常用碳作电极:
(1)在电化学中,常用碳作电极:查看答案和解析>>
科目:高中化学 来源: 题型:
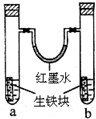 如图装置中,U型管内为红墨水,a、b试管内分别盛有食盐水和氯化铵溶液,各加入一块生铁,放置一段时间.下列有关描述错误的是( )
如图装置中,U型管内为红墨水,a、b试管内分别盛有食盐水和氯化铵溶液,各加入一块生铁,放置一段时间.下列有关描述错误的是( )| A、两边生铁块中的碳均为各自形成的原电池的正极 |
| B、a试管中发生了吸氧腐蚀,b试管中发生了析氢腐蚀 |
| C、两试管中相同的电极反应式是:Fe-2e-=Fe2+ |
| D、红墨水柱两边的液面变为左低右高 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、500 mL 1 mol/L的KNO3溶液 |
| B、500 mL 1 mol/L的Ba(NO3)2溶液 |
| C、100 mL 0.5 mol/L的Mg(NO3)2溶液 |
| D、1 L 0.5 mol/L的Fe(NO3)3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、还原剂只有锂 |
| B、SOCl2中既有离子键,也有共价键 |
| C、氧化产物包括LiCl和SO2 |
| D、标准状况下生成1.12LSO2时,反应转移电子为0.1mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com