
【题目】已知:氢氧化镁能溶于浓度均为3mol/L的①盐酸②NH4Cl溶液③醋酸铵溶液(中性),下列说法正确的是( )
A. c(NH4+):③>②
B. pH:①>②>③
C. Mg(OH)2溶于②的主要原因是由于NH4+水解使溶液显酸性,导致平衡Mg(OH)2(s)![]() Mg2+(aq)+2OH-(aq)向溶解方向移动
Mg2+(aq)+2OH-(aq)向溶解方向移动
D. 等体积①和③混合溶液中c(Cl-)>c(NH4+)>c(H+)>c(CH3COO-)>c(OH-)
【答案】D
【解析】试题分析:A、NH4Cl溶液和醋酸铵溶液均存在NH4+水解,但醋酸铵溶液中还存在醋酸根的水解,促进NH4+水解,导致c(NH4+):③ <② ,错误;B、pH:① < ②< ③,错误;C、由题意知,Mg(OH)2溶于②的主要原因是由于NH4+与Mg(OH)2(s)溶解产生的OH-反应生成一水合氨,使OH-浓度降低,导致平衡Mg(OH)2(s)![]() Mg2+ (aq) + 2OH- (aq)向溶解方向移动,错误;D、等浓度、等体积盐酸和醋酸铵溶液混合,二者恰好完全反应生成醋酸和氯化铵,且二者浓度相等均为3mol/L,溶液显酸性,c(H+) >c(OH-),NH4+水解消耗一部分,c(Cl-) >c(NH4+) ,H+来自醋酸的电离NH4+水解,c(H+) > c(CH3COO-)电离和水解是微弱的,c(NH4+) > c(H+),综上所述溶液中 c(Cl-) >c(NH4+) > c(H+) > c(CH3COO-) > c(OH-) ,正确。故选D。
Mg2+ (aq) + 2OH- (aq)向溶解方向移动,错误;D、等浓度、等体积盐酸和醋酸铵溶液混合,二者恰好完全反应生成醋酸和氯化铵,且二者浓度相等均为3mol/L,溶液显酸性,c(H+) >c(OH-),NH4+水解消耗一部分,c(Cl-) >c(NH4+) ,H+来自醋酸的电离NH4+水解,c(H+) > c(CH3COO-)电离和水解是微弱的,c(NH4+) > c(H+),综上所述溶液中 c(Cl-) >c(NH4+) > c(H+) > c(CH3COO-) > c(OH-) ,正确。故选D。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】已知某温度时CH3COOH的电离平衡常数为K。该温度下向20 mL 0.1 mol·L-1 CH3COOH溶液中逐滴加入0.1 mol·L-1 NaOH溶液,pH变化曲线如图所示(忽略温度),以下叙述正确的是
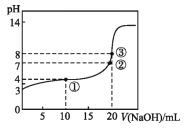
A.根据图中数据可计算出K值约为1×10-5
B.①②③点水的电离程度由大到小的顺序为:②>③>①
C.点①所示溶液中:c(CH3COO-)+c(OH-)=c(CH3COOH)+c(H+)
D.点③时c(CH3COOH)+c(CH3COO-)=0.1 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中的一定量混合气体发生反应:xA(g)+yB(g)![]() zC(g)平衡时测得A的浓度为0.50 mol/L,保持温度不变,将容器的容积扩大到原来的二倍,再达平衡时,测得A的浓度降低为0.24 mol/L。下列有关判断错误的是
zC(g)平衡时测得A的浓度为0.50 mol/L,保持温度不变,将容器的容积扩大到原来的二倍,再达平衡时,测得A的浓度降低为0.24 mol/L。下列有关判断错误的是
A.x+y<z B.B的转化率降低
C.平衡向正反应方向移动 D.C的体积分数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向1L的密闭容器中加入1molX、3molZ和一定量的Y三种气体。一定条件下发生反应,各物质的浓度随时间变化如图一所示。图二为t2时刻后改变反应条件,平衡体系中反应速率随时间变化的情况,且四个阶段都各改变一种不同的条件。下列说法不正确的是
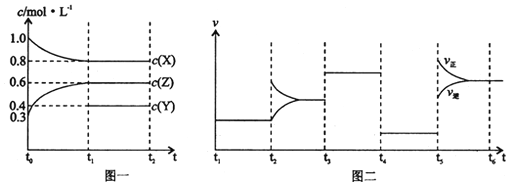
A. Y的起始物质的量为0.5mol
B. 该反应的化学方程式为:2X(g)+Y(g)![]() 3Z(g)ΔH<0
3Z(g)ΔH<0
C. 若t0=0,t1=10s,则t0-t1阶段的平均反应速率为v(z)=0.03mol/(L﹒s)
D. 反应物X的转化率t6点比t3点高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 可用铝罐贮运浓硝酸 B. 弱酸一定不能制备强酸
C. 复分解反应可能也是氧化还原反应 D. 炼铁高炉的高度越髙,尾气中CO的含量越少
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是
A.向盐酸中滴加氨水:H++OH-=H2O
B.氯化钙与碳酸氢钾溶液混合:Ca2++CO32-=CaCO3↓
C.氢氧化铝中和胃酸:Al(OH)3+3H+=Al3++3H2O
D.Ca(HCO3)2溶液中加入过量KOH溶液:Ca2++HCO3﹣+OH﹣═CaCO3↓+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用二氧化硅和金属氧化物的形式表示硅酸盐的形成,不正确的是
A. 正长石[KAlSi3O8]:K2O·Al2O3·3SiO2
B. 镁橄榄石[Mg2SiO4]:2MgO·SiO2
C. 钙沸石[CaAl2Si3O10·3H2O]: CaO·Al2O3·3SiO2·3H2O
D. 高岭石[Al2(Si2O5)(OH)4]:Al2O3·2SiO2·2H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com