
某氮肥NH4HCO3中混有少量(NH4)2CO3,现采用下列方案测定该氮肥中(NH4)2CO3的质量分数:称取5.7 g样品与2.0 mol·L-1 NaOH溶液混合,完全溶解后,低温加热使其充分反应(该温度下铵盐不分解),并使生成的氨气全部被硫酸吸收,测得氨气的质量与所用NaOH溶液体积的关系如图所示。请回答下列问题: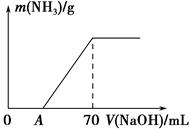
(1)A点前样品与NaOH反应的离子方程式为 。
(2)为使生成的氨气被硫酸吸收时不发生倒吸,可以选用下列装置中的 (填字母序号)。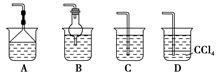
(3)样品中(NH4)2CO3的质量分数是 %(保留一位小数)。
(4)当V(NaOH)=50 mL时,生成NH3的质量为 。
 天天练口算系列答案
天天练口算系列答案科目:高中化学 来源: 题型:单选题
用1molMnO2和含HCl为4mol的浓盐酸充分反应(共热),在不考虑HCl挥发的情况下,得到的氯气的物质的量
| A.等于2mol | B.等于1mol | C.小于1 mol | D.大于2 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
A气体极易溶于水,其相对分子质量为a,在0℃、1.01×105Pa时,测得其饱和溶液的物质的量浓度为b mol/L,该溶液的密度为c g/cm3,求:
(1)A饱和溶液中溶质的质量分数;
答:c%=
(2)0℃、1.01×105帕时,1体积水中可溶解多少体积的A气体?
答:V=
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
推进器中盛有强还原剂肼(N2H4)和强氧化剂液态双氧水。当它们混合反应时,即产生大量氮气和水蒸气,并放出大量热。已知0.4mol液态肼与足量液态双氧水反应,生成氮气和水蒸气,放出256.652KJ的热量。
(1)写出过氧化氢的电子式 。
(2)该反应的热化学方程式为 。
1mol肼完全反应转移电子数 。
(3)此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是 。
(4)又已知H2O(l)==H2O(g);△H = +44kJ?mol-1,由16g液态肼与液态双氧水反应生成液态水时放出的热量是 kJ。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(14)A、B、C、D、E、F是常见单质,其中A是用量最大,应用最广泛的金属;元素D是地壳中含量最多的金属元素;D元素和E元素在周期表中相邻。G、H、I、J、K、L是常见化合物,其中G在常温下是无色液体,H是黑色固体。以上物质相互间的转化关系如图所示: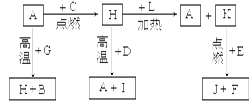
请回答下列问题:
(1)元素A在元素周期表中的位置为 周期 族。
(2)写出K的电子式 。
(3)写出H和D反应的化学方程式 。
(4)D能与氢氧化钠溶液反应,请写出该反应的离子方程式 。
(5)写出A与G反应的化学方程式 。
(6)K与E反应时产生的现象有 ;该反应的化学方程式为 ___________________。
(7)已知F的燃烧热为akJ/mol,L的燃烧热为bkJ/mol,试写出F生成L的热化学方程式_________________
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
将CO2通入NaOH溶液中,所得产物随通入的CO2的物质的量的不同而不同。完成下列填空。
(1)250 mL 1 mol/L的NaOH溶液,最多可吸收CO2 L(标准状况下)。
(2)向250 mL 2 mol/L的NaOH溶液中通入一定量CO2,溶液增重4.4 g,将所得溶液蒸干,计算所得固体中各成分的物质的量。
向未知浓度、体积为V L的 NaOH溶液中缓缓通入一定体积(标准状况下)的CO2,充分反应后,在减压低温的条件下蒸发溶液,得到白色固体。
(3)若反应中CO2和NaOH均无剩余,反应后向溶液中加入过量的澄清石灰水生成m1 g 白色沉淀。
①根据以上数据,用代数式表示CO2的体积V(CO2)= 。
②根据以上数据,推理计算出NaOH溶液的浓度范围。
(4)写出确定NaOH浓度的实验步骤,并用代数式表示NaOH溶液的浓度。(设计实验方案时,只能用题中提供的CO2和NaOH溶液,不得使用其它化学试剂。)
实验步骤: 。c(NaOH)= 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
尽管氮元素在地壳中的丰度较低(主要以硝酸盐的形式存在),在所有元素中仅排31位,但是大气中有丰富的氮气,这为氨和硝酸的广泛应用提供了可能。
(1)氮气的电子式为 ,雷电作用能进行氮的固定,写出反应方程式 。
(2)食物蕴含的营养物质中,含氮的高分子化合物是 (填名称),其水解的最终产物为 。
(3)土壤中的NH4+在硝化细菌的催化作用下可转化为NO3﹣,写出其离子方程式: 。
(4)某铜铝合金用足量稀硝酸完全溶解,得到标准状况下NO 11.2 L,再向溶液中加入过量氨水,充分反应后过滤。①滤液显深蓝色是因为含有的离子(填化学式). 。②若沉淀质量为7.8g,则合金的质量为 g。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
将一支盛有a mL NO 和b mL NO2气体的试管倒立于水槽中,然后通过a mL O2,请回答以下小题:
(1)若a=b,则充分反应后试管内气体体积为_________mL。
(2)若a<b,则充分反应后试管内气体体积为_________mL。
(3)若a>b,则充分反应后试管内气体体积为_________mL。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
无机化合物A中含有金属Li元素,遇水强烈水解,主要用于有机合成和药物制造,是具有良好前景的储氢材料。在一定条件下,2.30g固体A与5.35gNH4Cl固体恰好完全反应,生成固体B和4.48L气体C (标准状况)。已知气体C极易溶于水得到碱性溶液, 电解无水B可生成金属单质D和氯气。
回答下列问题:
(1)A的化学式是 , C的电子式是 。
(2)写出化合物A与盐酸反应的化学方程式: 。
(3)某同学通过查阅资料得知物质A的性质:
Ⅰ.工业上可用金属D与液态的C在硝酸铁催化下反应来制备A物质,纯净的A物质为白色固体,但制得的粗品往往是灰色的。
Ⅱ.物质A熔点390℃,沸点430℃,密度大于苯或甲苯,不溶于煤油,遇水反应剧烈,也要避免接触酸和酒精。在空气中化合物A缓慢分解,对其加强热则猛烈分解,但不会爆炸.在750~800℃分解为化合物E和气体C。
①物质A在750~800℃分解的方程式为: 。
②久置的物质A可能大部分变质而不能使用,需将其销毁。遇到这种情况,可用苯或甲苯将其覆盖,然后缓慢加入用苯或甲苯稀释过的无水乙醇,试解释其化学原理 。
(4)工业制备单质D的流程图如下:
①步骤①中操作名称: 。
②试用平衡原理解释步骤②中减压的目的: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com