
ЁОЬтФПЁПЩшAЁЂBЁЂCДњБэШ§жждЊЫиЃЌвбжЊЂйB2ЈDКЭAЃЋСНжжРызгОпгаЯрЭЌЕФЕчзгВуНсЙЙЃЌЂкCдЊЫиЕФдзгКЫФкжЪзгЪ§БШBдЊЫиЕФдзгКЫФкжЪзгЪ§Щй8ИіЃЌЂлBКЭCСНжждЊЫиПЩаЮГЩ5ИідзгКЫЃЈвЛАуМђГЦ5КЫЃЉ50ИіЕчзгЕФИКЖўМлвѕРызгЃЈЬсЪОЮЊЃКBC42ЈDЛђЮЊЃКCB42ЈDЃЉЁЃОнДЫЬюПеЃК
ЃЈ1ЃЉаДГіBКЭCЕФдЊЫиУћГЦЃКBЮЊ_____________ЃЌCЮЊ_____________ЁЃ
ЃЈ2ЃЉгаAЁЂBЁЂCШ§жждЊЫиаЮГЩЕФКЌ78ИіЕчзгЕФбЮРрЛЏКЯЮяЕФЛЏбЇЪНЪЧ______________ЁЃ
ЃЈ3ЃЉФГдЊЫиXЕФдзггыAдЊЫиаЮГЩЕФЛЏКЯЮяЕФЛЏбЇЪНЮЊЃКAXЃЌЭЈЙ§ВтСПЗЂЯжЕФЪНСПЮЊ76ЃЌXдзгКЫФкжазгЪ§ЮЊ20ЃЌдђXЪєгкЕФдЊЫиУћГЦЪЧ_____________ЃЌгУЛЏбЇЗћКХБэЪОXдзггІИУЪЧ______________ЁЃ
ЁОД№АИЁПСђ бѕ K2SO3 ТШдЊЫи ![]()
ЁОНтЮіЁП
ЂйЩшAдЊЫиЕФдзгКЫФкжЪзгЪ§ЮЊaЃЌBдЊЫиЕФдзгКЫФкжЪзгЪ§ЮЊbЃЌЧвB2ЈDКЭAЃЋСНжжРызгОпгаЯрЭЌЕФЕчзгВуНсЙЙЃЌдђa-b=3ЃЛ
ЂкCдЊЫиЕФдзгКЫФкжЪзгЪ§БШBдЊЫиЕФдзгКЫФкжЪзгЪ§Щй8ИіЃЌдђcдЊЫиЕФдзгКЫФкжЪзгЪ§ЮЊb-8ЃЛ
ЂлBКЭCСНжждЊЫиПЩаЮГЩ5ИідзгКЫ(вЛАуМђГЦ5КЫ)50ИіЕчзгЕФИКЖўМлвѕРызгЃЌШєРызгЮЂСЃЮЊBC42ЈDЃЌдђb+4(b-8)+2=50ЃЌНтЕУЃКb=16ЃЌМДBЮЊСђдЊЫиЃЛДЫЪБAдЊЫиЕФдзгКЫФкжЪзгЪ§ЮЊ16+3=19ЃЌЮЊМидЊЫиЃЛCЕФжЪзгЪ§ЮЊ8ЃЌЮЊбѕдЊЫиЃЛ
ШєРызгЮЂСЃЮЊCB42ЈDЃЌдђ(b-8)+4b+2=50ЃЌb=11.2ЃЌжЪзгЪ§ОљЮЊећЪ§жЕЃЌВЛЗћКЯЃЌЩсШЅЁЃ
гЩЗжЮіжЊЃКAЮЊKдЊЫиЃЌBЮЊSдЊЫиЃЌCЮЊOдЊЫиЃЛ
(1)BЮЊСђдЊЫиЃЌCЮЊбѕдЊЫиЃЛ
(2)вбжЊдзгКЫФкжЪзгЪ§ЕШгкдзгКЫЭтЕчзгзмЪ§ЃЌдђгаKЁЂSЁЂOШ§жждЊЫизщГЩЕФГЃМћбЮгаK2SO4ЁЂK2SO3ЃЌЦфжаK2SO3ЙВКЌга78ИіЕчзгЃЛ
(3)ФГдЊЫиXЕФдзггыKдЊЫиаЮГЩЕФЛЏКЯЮяЕФЛЏбЇЪНЮЊЃКKXЃЌЭЈЙ§ВтСПЗЂЯжЕФЪНСПЮЊ76ЃЌдђXЕФЯрЖддзгжЪСПЮЊ37ЃЌжЪСПЪ§ЮЊ37ЃЌгЩ XдзгКЫФкжазгЪ§ЮЊ20ЃЌПЩжЊXдЊЫиЕФдзгКЫФкжЪзгЪ§ЮЊ37-20=17ЃЌдђXдЊЫиЮЊТШдЊЫиЃЌгУЛЏбЇЗћКХБэЪОXдзггІИУЪЧ![]() ЁЃ
ЁЃ


 ПЊаФЭмзДдЊВтЪдОэЯЕСаД№АИ
ПЊаФЭмзДдЊВтЪдОэЯЕСаД№АИ
| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁП2.0molPCl3КЭ1.0molCl2ГфШыЬхЛ§ВЛБфЕФУмБеШнЦїжаЃЌдквЛЖЈЬѕМўЯТЗЂЩњЯТЪіЗДгІЃКPCl3(g)+Cl2(g)PCl5(g)ДяЦНКтЪБЃЌPCl5ЮЊ0.4molЃЌШчЙћДЫЪБвЦзп1.0molPCl3КЭ0.50molCl2ЃЌдкЯрЭЌЮТЖШЯТдйДяЦНКтЪБPCl5ЕФЮяжЪЕФСПЪЧЃЈ ЃЉ
A. 0.4mol
B. 0.2mol
C. аЁгк0.2mol
D. Дѓгк0.2molЃЌаЁгк0.4mol
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЖЬжмЦкдЊЫизщГЩЕФЕЅжЪX2ЁЂYЃЌБъзМзДПіЯТX2ЕФУмЖШЮЊ3.17gL-1ЃЌГЃЮТЯТЃЌYЮЊЧГЛЦЩЋЙЬЬхЁЃZЪЧвЛжжЛЏКЯЮяЃЌбцЩЋЗДгІГЪЧГзЯЩЋ![]() ЭИЙ§юмВЃСЇ
ЭИЙ§юмВЃСЇ![]() ЃЛ0.1molL-1ZЕФЫЎШмвКpH=13ЁЃX2ЁЂYКЭZжЎМфгаШчЯТзЊЛЏЙиЯЕ
ЃЛ0.1molL-1ZЕФЫЎШмвКpH=13ЁЃX2ЁЂYКЭZжЎМфгаШчЯТзЊЛЏЙиЯЕ![]() ЦфЫћЮоЙиЮяжЪвбТдШЅ
ЦфЫћЮоЙиЮяжЪвбТдШЅ![]() ЃК
ЃК
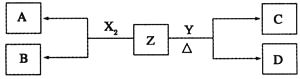
(1)аДГіЕЅжЪX2гыZЗДгІЕФРызгЗНГЬЪНЃК______________________________________ЁЃ
(2)вбжЊ16gЕЅжЪYЭъШЋШМЩеЗХГі148kJШШСПЁЃаДГіШШЛЏбЇЗНГЬЪНЃК________________ЁЃ
(3)вбжЊCФмгыНЯХЈбЮЫсЗДгІЩњГЩФмЪЙЦЗКьШмвКЭЪЩЋЕФЦјЬх
ЂйDЕФЛЏбЇЪНЪЧЃК_________ЃЛDЕФЫЎШмвКpH>7ЃЌдвђЪЧ![]() гУРызгЗНГЬЪНБэЪО
гУРызгЗНГЬЪНБэЪО![]() ЃК_____________ЁЃ
ЃК_____________ЁЃ
Ђк0.1molL-1ЕФDШмвКжаИїРызгХЈЖШгЩДѓЕНаЁЕФЫГађЮЊ_______________________ЁЃ
ЂлНЋ20mL0.5molL-1ШмвКж№ЕЮМгШыЕН20mL0.2molL-1 KMnO4ШмвК![]() СђЫсЫсЛЏ
СђЫсЫсЛЏ![]() жаЃЌШмвКЧЁКУЭЪЮЊЮоЩЋЁЃаДГіЗДгІЕФРызгЗНГЬЪНЃК_________________________________ЁЃ
жаЃЌШмвКЧЁКУЭЪЮЊЮоЩЋЁЃаДГіЗДгІЕФРызгЗНГЬЪНЃК_________________________________ЁЃ
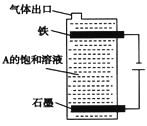
(4)ЂйЪЏФЋКЭЬњзіЕчМЋЃЌгУИєФЄЕчНтВлЕчНтAЕФШмвКЃЌбєМЋПЩВњЩњX2ЁЃдђЬњзі_________МЋЁЃ
ЂкАДЯТЭМЕчНтAЕФБЅКЭШмвКЃЌаДГіИУЕчНтГижаНЯГЄЪБМфФкЗЂЩњЗДгІЕФзмЗДгІЗНГЬЪНЃК ________ЁЃНЋГфЗжЕчНтКѓЫљЕУШмвКж№ЕЮМгШыЕНЗгЬЊЪдвКжаЃЌЙлВьЕНЕФЯжЯѓЪЧ_________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПФГЭЌбЇХфжУ450КСЩ§ 1mol/LЕФСђЫсШмвК
ЃЈ1ЃЉгІИУбЁдё________ЕФШнСПЦП A 250КСЩ§ B 500КСЩ§ C 1000КСЩ§
ЃЈ2ЃЉашвЊСПШЁ98%,Іб=1.84g/cm3ХЈСђЫс__________КСЩ§
ЃЈ3ЃЉНЋЫљШЁХЈСђЫсж№ЕЮМгШыЪЂгаЫЎЕФЩеБжаЃЌБпМгБпНСАш
ЃЈ4ЃЉНЋИУШмвКзЂШыШнСПЦП
ЃЈ5ЃЉдкШнСПЦПжаМгЫЎжС___________ДІЃЌИФгУ__________МгЫЎжС_______гыПЬЖШЯпЯрЧа
ЃЈ6ЃЉШћКУЦПШћЃЌЗДИДвЁдШ
ЃЈ7ЃЉвЁдШКѓЗЂЯжЃЌШмвКЬхЛ§ЫѕаЁЃЌМЬајМгЫЎжСПЬЖШЯп
ЃЈ8ЃЉИУЭЌбЇЕФВйзїЪЧЗёгаВЛЕБжЎДІЃЌЧыжИГі(ВЛБиШЋВПЬюТњ)
a__________________ИУДэЮѓВйзїНЋЪЙЫљХфШмвКЕФХЈЖШ_______(ЁАБфДѓЁБЛђЁАБфаЁЁБ)
b____________ИУДэЮѓВйзїНЋЪЙЫљХфШмвКЕФХЈЖШ_______(ЁАБфДѓЁБЛђЁАБфаЁЁБ)
c_______________ИУДэЮѓВйзїНЋЪЙЫљХфШмвКЕФХЈЖШ_______(ЁАБфДѓЁБЛђЁАБфаЁЁБ)
d____________ИУДэЮѓВйзїНЋЪЙЫљХфШмвКЕФХЈЖШ_______(ЁАБфДѓЁБЛђЁАБфаЁЁБ)
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПH2SЃЈГЃЮТЯТЃЌЧтСђЫсЕФKa1=5.7ЁС10-8ЃЌKa2=1.2ЁС10-15ЃЉЙуЗКДцдкгкЬьШЛЦјЁЂКЯГЩАБдСЯЦјЁЂСЖГЇЦјЕШЃЌЩњВњжаашЭбСђДІРэЁЃЛиД№ЯТСаЮЪЬт
ЃЈ1ЃЉжјУћЕФ VanvielЗДгІЮЊ2nH2S+nCO2![]() ЃЈCH2OЃЉn+nH2O+2nSЁ§ЃЌИУЗДгІФмСПзЊЛЏаЮЪНЪЧ________ЁЃ
ЃЈCH2OЃЉn+nH2O+2nSЁ§ЃЌИУЗДгІФмСПзЊЛЏаЮЪНЪЧ________ЁЃ
ЃЈ2ЃЉЭбГ§ЬьШЛЦјжаH2SЕФЙЄвеСїГЬШчЯТ
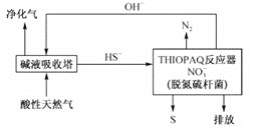
ЂйГЃЮТЯТЃЌЁАМювКЮќЪеЫўЁБжаЗДгІHS-+OH- ![]() S2-+H2OЕФЦНКтГЃЪ§K=________ЁЃ
S2-+H2OЕФЦНКтГЃЪ§K=________ЁЃ
ЂкЁА THIOPAOЁБЗДгІЦїжаЃЌдкЭбЕЊСђИЫОњЕФзїгУЯТЃЌHS-бѕЛЏЮЊSЕФРызгЗНГЬЪНЮЊ________ЁЃ
ЃЈ3ЃЉЭЃЈЂђЃЉГСЕэМАЭЃЈЂђЃЉЪЊЪНбѕЛЏЭбçѐˏЧтВЂПЩЛиЪеСђЛЧЃЌжївЊВНжшШчЯТ
ЃЈaЃЉЮќЪеH2S
ЃЈbЃЉЩњГЩCuSГСЕэ
ЃЈcЃЉCuCl2бѕЛЏCuSЩњГЩЕЅжЪSКЭCuCl2-
ЃЈdЃЉЭЈO2дйЩњ
ЂйГЃЮТЯТЃЌГСЕэЗДгІжЎвЛЃКHS-+Cu2+![]() CuS+H+ЕФЦНКтГЃЪ§K= ________ЃЈвбжЊГЃЮТЯТЃЌKSPЃЈCuSЃЉ=4ЁС10-35ЃЉЁЃ
CuS+H+ЕФЦНКтГЃЪ§K= ________ЃЈвбжЊГЃЮТЯТЃЌKSPЃЈCuSЃЉ=4ЁС10-35ЃЉЁЃ
ЂкCuCl2бѕЛЏCuSЕФРызгЗНГЬЪНЮЊ ________ЁЃ
ЂлЭЈO2дйЩњЪБЕФРызгЗНГЬЪНЮЊ________ ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЪЕбщЙ§ГЬжаЃЌЪМжеЮоУїЯдЯжЯѓЕФЪЧЃЈ ЃЉ
A.NO2ЭЈШыFeSO4ШмвКжа
B.SO2ЭЈШывбЫсЛЏЕФBa(NO3)2ШмвКжа
C.NH3ЭЈШыAlCl3ШмвКжа
D.CO2ЭЈШыCaCl2ШмвКжа
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаИїБэЪігыЪОвтЭМвЛжТЕФЪЧ
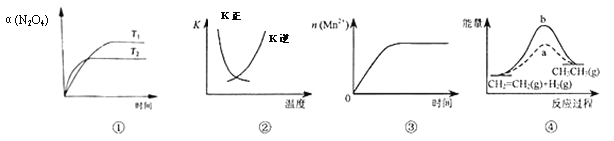
A. ЭМЂйБэЪОN2O4(g)![]() 2NO2(g) ІЄHЃО0ЃЌN2O4зЊЛЏТЪЫцЮТЖШЁЂЪБМфЕФБфЛЏ
2NO2(g) ІЄHЃО0ЃЌN2O4зЊЛЏТЪЫцЮТЖШЁЂЪБМфЕФБфЛЏ
B. ЭМЂкжаЧњЯпБэЪОЗДгІ2SO2(g)+O2(g)![]() 2SO3(g) ІЄHЃМ0ЃЌе§ЁЂФцЗДгІЕФЦНКтГЃЪ§KЫцЮТЖШЕФБфЛЏ
2SO3(g) ІЄHЃМ0ЃЌе§ЁЂФцЗДгІЕФЦНКтГЃЪ§KЫцЮТЖШЕФБфЛЏ
C. ЭМЂлБэЪО10 mL0.01 mol/LKMnO4ЫсадШмвКгыЙ§СП0.1mol/LH2C2O4ШмвКЛьКЯЪБЃЌn(Mn2+)ЫцЪБМфЕФБфЛЏ
D. ЭМЂмжаaЁЂbЧњЯпЗжБ№БэЪОЗДгІCH2ЃНCH2(g)+H2(g)![]() CH3CH3(g) ІЄHЃМ0ЃЌЪЙгУКЭЮДЪЙгУДпЛЏМСЪБЃЌЗДгІЙ§ГЬжаЕФФмСПБфЛЏ
CH3CH3(g) ІЄHЃМ0ЃЌЪЙгУКЭЮДЪЙгУДпЛЏМСЪБЃЌЗДгІЙ§ГЬжаЕФФмСПБфЛЏ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЖдгкЗДгІ2A+B![]() 3C+4DЃЌБэЪОЗДгІЫйТЪзюПьЕФЪЧ
3C+4DЃЌБэЪОЗДгІЫйТЪзюПьЕФЪЧ
A.VA=0.75mol/(LЁЄs)B.VB=0.5mol/(LЁЄs)C.VC=1.0mol/(LЁЄs)D.VD=1.5mol/(LЁЄs)
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПСђЫсяШ(SrSO4)дкЫЎжаЕФГСЕэШмНтЦНКтЧњЯпШчЯТ.ЯТСаЫЕЗЈе§ШЗЕФЪЧЃЈ ЃЉ
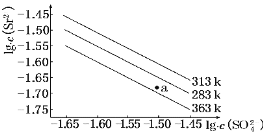
A.ЮТЖШвЛЖЈЪБЃЌKsp(SrSO4)Ыцc(SO42-)ЕФдіДѓЖјМѕаЁ
B.Ш§ИіВЛЭЌЮТЖШжаЃЌ313KЪБKsp(SrSO4)зюаЁ
C.283KЪБЃЌЭМжаaЕуЖдгІЕФШмвКЪЧВЛБЅКЭШмвК
D.283KЯТЕФSrSO4БЅКЭШмвКЩ§ЮТЕН363KКѓБфЮЊВЛБЅКЭШмвК
ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com