
【题目】下列各离子①H+ ②Cl- ③Al3+ ④K+ ⑤S2- ⑥OH- ⑦NO3- ⑧NH4+中,不影响水的电离平衡的是( )
A.①③⑤⑦⑧B.②④⑦C.①⑥D.②④⑥⑧
【答案】B
【解析】
在任何溶液中存在水的电离平衡:H2O![]() H++OH-,
H++OH-,
①加入H+,使c(H+)增大,水的电离逆向逆向移动,影响水的电离平衡,①不符合题意;
②加入Cl-,由于不产生H+、OH-,也不消耗H+、OH-,对水的电离平衡无影响,②符合题意;
③Al3+会与水电离产生的OH-结合形成Al(OH)3,使水的电离平衡正向移动,促进了水的电离,③不符合题意;
④加入K+,由于不产生H+、OH-,也不消耗H+、OH-,对水的电离平衡无影响,④符合题意;
⑤S2-会与水电离产生的H+结合形成H2S,使水的电离平衡正向移动,促进了水的电离,⑤不符合题意;
⑥加入OH-,使c(OH-)增大,水的电离逆向移动,影响水的电离平衡,⑥不符合题意; ⑦加入NO3-,不产生H+、OH-,也不消耗H+、OH-,对水的电离平衡无影响,⑦符合题意;
⑧加入NH4+,会与水电离产生的OH-结合形成NH3·H2O,使水的电离平衡正向移动,促进了水的电离,⑧不符合题意;
综上所述可知:②④⑦符合题意,故合理选项是B。


 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】夏日的夜晚,常看到儿童手持荧光棒嬉戏,荧光棒发光原理是利用![]() 氧化草酸二酯(
氧化草酸二酯(![]() )产生能量,该能量被传递给荧光物质后发出荧光。草酸二酯的结构简式如图所示,下列有关草酸二酯的说法不正确的是( )
)产生能量,该能量被传递给荧光物质后发出荧光。草酸二酯的结构简式如图所示,下列有关草酸二酯的说法不正确的是( )
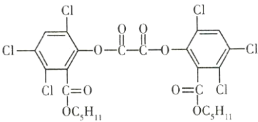
A.1mo草酸二酯与![]() 完全加成,需要消耗6mol
完全加成,需要消耗6mol![]()
B.草酸二酯的分子式为![]()
C.草酸二酯能发生取代反应
D.1mol草酸二酯最多可与4mol![]() 反应
反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溴乙烷是一种重要的有机化工原料,其沸点为38.4℃。制备溴乙烷的一种方法是乙醇与氢溴酸反应。
(1)该反应的化学方程式是:___。
实际通常是用溴化钠与一定浓度的硫酸和乙醇反应.某课外小组欲在实验室制备溴乙烷的装置如图。
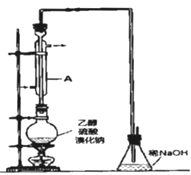
实验操作步骤如下:
①检查装置的气密性;
②在圆底烧瓶中加入95%乙醇、80%硫酸,然后加入研细的溴化钠粉末和几粒碎瓷片;
③小心加热,使其充分反应.
请问答下列问题:
(2)装置A的作用是__。
(3)反应时若温度过高,观察到还有一种红棕色气体(Br2)产生,反应结束后,得到的粗产品呈棕黄色。为了除去粗产品中的杂质,可选择下列试剂中的____(填写上正确选项的字母)。
a.稀氢氧化钠溶液 b.乙醇 c.四氯化碳 d.Na2SO3溶液
(4)要进一步制得纯净的溴乙烷,可继续用蒸馏水洗涤,分液后,再加入无水CaCl2,然后进行的实验操作是____(填写正确选项的字母)。
a.分液 b.蒸馏 c.萃取
(5)为了检验溴乙烷中含有溴元素,不能直接向溴乙烷中滴加硝酸银溶液来检验,通常采用的方法是取少量溴乙烷,然后___(按实验的操作顺序选填下列序号).
①加热 ②加入AgNO3溶液 ③加入稀HNO3酸化 ④加入NaOH溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z是原子序数依次增大的四种短周期主族元素,X与Y位于同一主族,X与W能够形成多种化合物,其中一种为红棕色气体,Y与Z形成的一种化合物Y2Z2的分子结构模型为![]() 。下列叙述正确的是( )
。下列叙述正确的是( )
A.X与W、Y及Z均能组合成多种化合物B.简单离子半径:Y>Z>X>W
C.W的氧化物的水化物一定为强酸D.化合物Y2Z2中Y不满足8电子稳定结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒压、NO和O2的起始浓度一定的条件下发生反应,在相同时间内,测得不同温度下NO转化为NO2的转化率如图中实线所示(图中虚线表示相同条件下NO的平衡转化率随温度的变化)。下列说法不正确的是( )

A.反应2NO(g) + O2(g) = 2NO2(g)的H<0
B.图中X点所示条件下,由于测定时间较短,反应未达到平衡
C.从 X→Y 过程中,平衡逆向移动,O2反应量减少
D.380℃下,c 平衡(O2)=5.0×104 mol·L1,NO 平衡转化率为 50%,则平衡常数 K=2000
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有结构简式如图所示的某有机物,它是药物生产的中间体,关于该有机物叙述正确的是
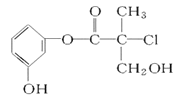
A.该有机物能与Na2CO3发生反应
B.该有机物与浓硫酸混合加热可发生消去反应
C.1mol该有机物与足量NaOH溶液反应最多消耗3molNaOH
D.该有机物经催化氧化后能发生银镜反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚邻苯二甲酸二烯丙酯(β聚合物)是一种优良的热固性树脂,这种材料可以采取下列路线合成:

已知:![]()
(1)反应类型:反应①___;反应⑤___。
(2)写出有关反应的方程式:
②__;④__。
(3)G是E的同分异构体,G具有如下性质:
①能发生银镜反应且1molG与银氨溶液反应时最多可得到4molAg;
②遇FeCl3溶液呈紫色;③能够发生水解反应;
符合上述条件的G最多有__种,写出其中苯环上取代基位置均相邻的所有可能的结构简式:___。
(4)工业上可由A为原料经过三步反应制得甘油(![]() ),根据已有知识并结合相关信息,表示出这一合成过程___。
),根据已有知识并结合相关信息,表示出这一合成过程___。
合成路线流程图示例如下:CH3CH2Br![]() CH3CH2OH
CH3CH2OH![]() CH3COOCH2CH3。
CH3COOCH2CH3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)粗制CuSO4·5H2O晶体中常含有杂质Fe2+。
①在提纯时为了除去Fe2+,常加入合适氧化剂,使Fe2+氧化为Fe3+,下列物质最好选用的是________。
A.KMnO4 B.H2O2 C.氯水 D.HNO3
②然后再加入适当物质调整溶液至pH=4,使Fe3+转化为Fe(OH)3,调整溶液pH可选用下列中的_______。
A.NaOH B.NH3·H2O C.CuO D.Cu(OH)2
(2)在25 ℃下,向浓度均为0.1 mol·L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成________沉淀(填化学式),生成该沉淀的离子方程式为________。已知25 ℃时Ksp[Mg(OH)2]=1.8×10-11,Ksp[Cu(OH)2]=2.2×10-20。
(3)向BaCl2溶液中加入AgNO3和KBr,当两种沉淀共存时,![]() =____。已知Ksp(AgBr)=5.4×10-13,Ksp(AgCl)=2.0×10-10。
=____。已知Ksp(AgBr)=5.4×10-13,Ksp(AgCl)=2.0×10-10。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,容积不变的密闭容器中发生反应:![]() ,下列不能说明该可逆反应已经达到平衡状态的是( )
,下列不能说明该可逆反应已经达到平衡状态的是( )
A. 混合气体压强不再发生变化B. 混合气体质量不再发生变化
C. 反应中CO与![]() 的物质的量之比为1:1D. 生成n mol CO的同时生成n mol
的物质的量之比为1:1D. 生成n mol CO的同时生成n mol ![]() (g)
(g)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com