
【题目】下列离子方程式中,属于水解反应的是( )
A.HCOOH+H2OHCOO﹣+H3O+
B.CO2+H2OHCO3﹣+H+
C.CO32﹣+H2OHCO3﹣+OH﹣
D.HS﹣+H2OS2﹣+H3O+
 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:
【题目】硫在空气中燃烧可以生成SO2 , SO2在催化剂作用下可以被氧化为SO3 , 其热化学方程式可表示为:S(g)+O2(g)═SO2(g)△H=﹣297kJ/mol,SO2(g)+ ![]() O2(g)SO3(g);△H=﹣98.3kJ/mol.如图是上述两个反应过程与能量变化的关系图,其中Ⅰ表示0.4mol SO2(g)、1.6mol SO3(g)、0.2mol O2(g)具有的能量,Ⅲ表示64gS(g)与96g O2(g)所具有的能量.
O2(g)SO3(g);△H=﹣98.3kJ/mol.如图是上述两个反应过程与能量变化的关系图,其中Ⅰ表示0.4mol SO2(g)、1.6mol SO3(g)、0.2mol O2(g)具有的能量,Ⅲ表示64gS(g)与96g O2(g)所具有的能量.
(1)Ⅰ→Ⅱ的反应是(填“吸热”,“放热”)反应.
(2)c为KJ.
(3)图示中b的大小对Ⅲ→Ⅱ反应的△H的影响是 .
A.△H随着b的增大而增大
B.△H随着b的增大而减小
C.△H随着b的减小而增大
D.△H不随b的变化而变化
(4)图中的d+e﹣b=KJ. 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2与H2的混合气体5g,在150℃时和足量的氧气混合,用电火花充分引燃,在相同状况下再将反应后所得混合气体通入到足量的Na2O2中,测得Na2O2固体增重的质量为3.4g,则原混合气体中CO2的物质的量分数为( )
A. 25% B. 75% C. 88% D. 32%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A. 因发生加成反应,苯可以使溴水褪色
B. 煤可以通过干馏、液化与气化等物理变化转化为清洁能源
C. 天然植物油常温下一般呈液态,难溶于水,有恒定的熔点、沸点
D. 分子式为C8H10且属于芳香烃的同分异构体有4种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】t℃时,某NaOH稀溶液中,c(H+)=10﹣amol/L,c(OH﹣)=10﹣bmol/L,已知a+b=12.
(1)该温度下,水的离子积常数Kw= .
(2)在该温度下,将100mL0.1mol/L的稀硫酸与100mL0.4mol/L的NaOH溶液混合后,溶液的pH= , 此时该溶液中由水电离的c(OH﹣)= .
(3)该温度下,若100体积pH1=a的某强酸溶液与1体积pH2=b的某强碱溶液混合后溶液呈中性,则混合前,该强酸的pH1与强碱的pH2之间应满足的关系是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组制取氯酸钾。制取实验结束后,取出生成了氯酸钾的试管冷却结晶、过滤、洗涤。请简述洗涤氯酸钾晶体的操作__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2的回收利用对减少温室气体排放、改善人类生存环境具有重要意义.利用CO2和CH4重整可制合成气(主要成分CO、H2),重整过程中部分反应的热化学方程式为: ①CH4(g)═C(s)+2H2(g)△H=75.0kJmol﹣1
②CO2(g)+H2(g)═CO(g)+H2O(g)△H=41.0kJmol﹣1
③CO(g)+H2(g)═C(s)+H2O(g)△H=﹣131.0kJmol﹣1
(1)反应CO2(g)+CH4(g)═2CO(g)+2H2(g)的△H= .
(2)固定n(CO2)=n(CH4),改变反应温度,CO2和CH4的平衡转化率见图1. 
①同温度下CO2的平衡转化率(填“大于”或“小于”)于CH4的平衡转化率,其原因是 .
②高温下进行该反应时常会因反应①生成“积碳”(碳单质),造成催化剂中毒,高温下反应①能自发进行的原因是 .
(3)一定条件下Pd﹣Mg/SiO2催化剂可使CO2“甲烷化”从而变废为宝,其反应机理如图2所示,该反应的化学方程式为 , 反应过程中碳元素的化合价为﹣2价的中间体是 . 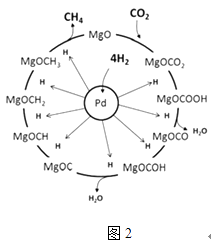
(4)卤水可在吸收烟道气中CO2的同时被净化,实现以废治废,其中涉及的一个反应是CaSO4+Na2CO3═CaCO3+Na2SO4 , 则达到平衡后,溶液中 ![]() = . [用Ksp(CaSO4)和Ksp(CaCO3)表示].
= . [用Ksp(CaSO4)和Ksp(CaCO3)表示].
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应是旧键断裂和新键形成的过程。共价键的键能是两种原子间形成1 mol共价键(或其逆过程)时释放(或吸收)的能量。已知下面化学键的键能: H—H Br—Br H—Br 键能(kJ·mol-1) 436 193 366,则Br2(g)+H2(g)=2HBr(g)的反应热ΔH等于( )
A. -183 kJ·mol-1B. 183 kJ·mol-1C. -103 kJ·mol-1D. 103 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镍是重要的有色金属之一,但粗镍中一般含有Fe、Cu及难与酸、碱溶液反应的不溶性杂质而影响使用.现对粗镍进行提纯,具体的反应流程如下: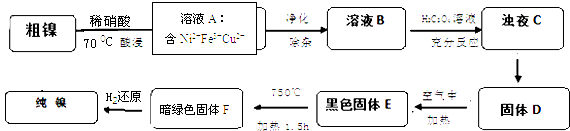
已知:
①2Ni2O3(黑色) ![]() 4NiO(黑色)+O2↑
4NiO(黑色)+O2↑
②
物质 | CuS | Cu(OH)2 | Ni(OH)2 | NiS |
Ksp | 8.8×10﹣38 | 2.2×10﹣20 | 5.48×10﹣18 | 3.2×1018 |
根据信息回答:
(1)28Ni在周期表中的第周期;镍与稀硝酸反应的离子方程式为 . 实验表明镍的浸出率与温度有关,随着温度升高镍的浸出率增大,但当温度高于70℃时,镍的浸出率又降低,浸出渣中Ni(OH)2含量增大,其原因为;
(2)在溶液A的净化除杂中,先调节PH=5.5,加热煮沸5min,静置一段时间后,过滤出Fe(OH)3 . 为了得到纯净的溶液B还需要加入以下物质进行除杂(填正确答案标号).
A.NaOH
B.Na2S
C.H2S
D.NH3﹒H2O
(3)已知以下三种物质的溶解度关系:NiC2O4>NiC2O4H2O>NiC2O42H2O.由浊液C得到固体D的操作包括过滤、、(填操作名称); D生成E的化学方程式为
(4)1molE经上述流程得到纯镍,理论上参加反应的氢气为 mol.
(5)测定样品中的镍含量的基本思路是将Ni2+转化为沉淀,通过测量沉淀的质量进一步推算Ni含量.已知Ni2+能与CO32﹣ , C2O42﹣、S2﹣等离子形成沉淀,但测定时常选用丁二酮肟(C4H8N2O2)作沉淀剂,生成分子式为C8H14N4O4Ni的鲜红色沉淀.从实验误差角度分析主要原因为: .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com