
【题目】下列反应属于吸热反应的是
A. 酒精在氧气中燃烧 B. 氢气在氧气中燃烧
C. 氢氧化钡晶体与氯化铵晶体反应 D. 氢氧化钾溶液和硫酸中和
科目:高中化学 来源: 题型:
【题目】请按要求回答下列问题:
Ⅰ.硫酸铜晶体的溶解度虽大,但溶解过程较慢,实验室常用热水配制以加快溶解速率,但常常会产生浑浊,请用文字简要说明原因_____________,如何才能用热水配制出澄清的较浓的CuSO4溶液_______________;
Ⅱ.依据反应:MnO4-+5Fe2++8H+ = Mn2++5Fe3++4H2O,采用滴定的方法测定FeSO4的质量分数,实验步骤如下:
滴定前的准备:
①→ 用蒸馏水清洗 → 用待装溶液润洗 → 装液→ ② → 调节液面在零刻度或零刻度以下 → 记录初始读数
①称量绿矾样品质量为m g,配成100 mL待测溶液,②取体积为10.00mL的待测液置于锥形瓶中,并加入一定量的硫酸,③将标准浓度为1.0molL﹣1的KMnO4溶液装入滴定管中,调节液面至a mL处,④滴定待测液至滴定终点时,滴定管的液面读数b mL,⑤重复滴定2~3次。
请回答下列问题:
(1)将步骤1中的操作补充完整:
①__________________________,②__________________________
(2)KMnO4(H+)溶液应装入______式滴定管进行滴定;如何知道滴定到达终点?___________
(3)下列操作会导致测定结果偏低的是____________________
A.盛标准溶液的滴定管用蒸馏水洗涤后未用标准液润洗就装液滴定
B.锥形瓶用蒸馏水洗涤后未用待测液润洗
C.读取标准液读数时,滴定前平视,滴定到终点后俯视
D.滴定后滴定管尖嘴处悬有溶液未滴落
(4)实验测得FeSO4的质量分数为____________(用含a、b的代数式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】北魏贾思勰《齐民要术·作酢法》这样描述苦酒:“乌梅苦酒法:乌梅去核,一升许肉,以五升苦酒渍数日,曝干,捣作屑。欲食,辄投水中,即成醋尔。”下列有关苦酒主要成分的说法正确的是( )
A. 苦酒的主要溶质是非电解质 B. 苦酒的主要溶质是弱电解质
C. 苦酒的主要溶质是强电解质 D. 苦酒的溶液中只存在分子,不存在离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产、生活息息相关,下列有关说法错误的是
A. 大量燃烧化石燃料是造成雾霾天气的原因之一
B. 从海水中提取物质都必须通过化学反应才能实现
C. 燃料脱硫和减少汽车尾气排放都能减少酸雨的产生
D. 用食醋可以除去热水壶内壁的水垢
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关硅及其化合物的叙述中,错误的是
A.单质硅是良好的半导体材料
B.硅和碳是都是第ⅣA族的元素
C.二氧化硅用来制造通讯材料(光导纤维)
D.二氧化硅溶于水生成硅酸,它是挥发性酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用pH=m的盐酸滴定20mLpH=n的MOH溶液,且m+n=14,混合溶液的pH与盐酸体积(V)的关系如图所示。下列说法正确的是
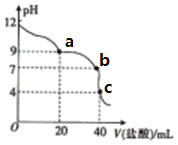
A. Kb(MOH)的数量级为10-11
B. 由c点可算得m=14/3
C. b点溶液呈中性,此时c(Cl-)=c(M+)
D. a点:c(Cl-)>c(M+)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】绿水青山就是金山银山,我国科研人员在探究如何降低大气中氮氧化物与碳氧化物的含量方面做出了巨大贡献,并取得了显著的成绩。
(1)下列关于氮氧化物与碳氧化物的说法中正确的是_____(填字母)。
A.CO2、NO2均属于酸性氧化物
B.NO、CO均不能用排空气法收集
C.除去NO中混有的NO2的方法是将混合气体通入足量氢氧化钠溶液中
D.除去CO中混有的CO2的方法是将混合气体通入足量氢氧化钠溶液中
(2)已知:N2(g)+O2(g)![]() 2NO(g)ΔH1=+180.5kJ/mol;
2NO(g)ΔH1=+180.5kJ/mol;
CO(g)![]() C(s)+1/2O2(g)ΔH2=+110.5kJ/mol;
C(s)+1/2O2(g)ΔH2=+110.5kJ/mol;
C(s)+O2(g)![]() CO2(g)ΔH3=-393.5kJ/mol。
CO2(g)ΔH3=-393.5kJ/mol。
则反应2NO(g)+2CO(g)![]() N2(g)+2CO2(g)ΔH=__________
N2(g)+2CO2(g)ΔH=__________
(3)反应2NO(g)+2CO(g)![]() 2CO2(g)+N2(g)可用于净化汽车尾气,已知570K时该反应的反应速率极慢,平衡常数极大。由此可知,提高尾气净化效率的最佳途径是_________;若要净化汽车尾气的同时提高该反应的反应速率和NO的转化率,且只改变一个反应条件,则应采取的措施是_________。
2CO2(g)+N2(g)可用于净化汽车尾气,已知570K时该反应的反应速率极慢,平衡常数极大。由此可知,提高尾气净化效率的最佳途径是_________;若要净化汽车尾气的同时提高该反应的反应速率和NO的转化率,且只改变一个反应条件,则应采取的措施是_________。
(4)某科研小组根据反应2NO(g)+2CO(g)![]() N2(g)+2CO2(g)来探究起始反应物的碳氨比[n(CO)/n(NO)]对污染物去除率的影响。T℃时,向体积为1L的恒容密闭容器中充入总物质的量为4mol的NO和CO混合气体,并加入一定量的固体催化剂进行反应,实验测得平衡体系中气体组分的转化率和氯气的体积分数的变化如图所示.
N2(g)+2CO2(g)来探究起始反应物的碳氨比[n(CO)/n(NO)]对污染物去除率的影响。T℃时,向体积为1L的恒容密闭容器中充入总物质的量为4mol的NO和CO混合气体,并加入一定量的固体催化剂进行反应,实验测得平衡体系中气体组分的转化率和氯气的体积分数的变化如图所示.

①根据图像推测曲线转化率1表示的是______ (填“CO”或“NO”)。
②A点时,n(CO)/n(NO)=_________,此时反应的平衡常数K= __________(请填写数值与单位)。
(5)煤炭在O2/CO2的气氛中燃烧会产生CO,有人提出,可以设计反应2CO(g)=2C(s)+O2(g)来消除CO的污染。该提议_______(填“可行”或“不可行”), 理由是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知草酸晶体(H2C2O4·XH2O)可溶于水,并可与酸性高锰酸钾溶液完全反应:2KMnO4+5H2C2O4+3H2SO4==K2SO4+2MnSO4+10CO2↑+8H2O。现用氧化还原滴定法测定草酸晶体的结晶水分子数X,步骤如下:
①用分析天平称取草酸晶体1.260g,将其配制成100.00mL待测草酸溶液
②用移液管移取25.00mL待测草酸溶液于锥形瓶中,并加入适量硫酸酸化
③用浓度为0.1000mol/L的KMnO4标准溶液进行滴定,三次结果如下:
第一次滴定 | 第二次滴定 | 第三次滴定 | |
待测溶液体积(mL) | 25.00 | 25.00 | 25.00 |
标准溶液体积(mL) | 9.99 | 10.01 | 10.00 |
已知H2C2O4的相对分子质量为90,请回答下列问题:
(1)滴定时,KMnO4标准溶液应该装在________(填酸式或碱式)滴定管中。
(2)在整个实验过程中,不需要的仪器或用品是______(填序号)。
①100mL容量瓶②烧杯③滴定管夹④漏斗⑤玻璃棒⑥托盘天平
(3)到达滴定终点的标志是____________________________________________。
(4)根据上述数据计算X=________________。
(5)误差分析(填偏高、偏低或无影响):
①若滴定开始时仰视滴定管刻度,滴定结束时俯视滴定管刻度,则X值________;
②若KMnO4标准溶液浓度偏低,则X值_________;
③若锥形瓶洗净后瓶内还残留有少量蒸馏水,则X值____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在恒容密闭容器中,能表示反应X(g)+2Y(g) ![]() 2Z(g)一定达到化学平衡状态的是( )
2Z(g)一定达到化学平衡状态的是( )
①X、Y、Z的物质的量之比为1∶2∶2
②X、Y、Z的浓度不再发生变化
③容器中的压强不再发生变化
④单位时间内生成n mol Z,同时生成2n mol Y
A. ①② B. ①④ C. ②③ D. ③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com