
【题目】工业上用甲苯生产邻羟基苯甲酸甲酯: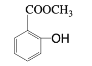 ,下列反应① ~⑥ 是其合成过程,其中某些反应条件及部分反应物或生成物未注明。
,下列反应① ~⑥ 是其合成过程,其中某些反应条件及部分反应物或生成物未注明。
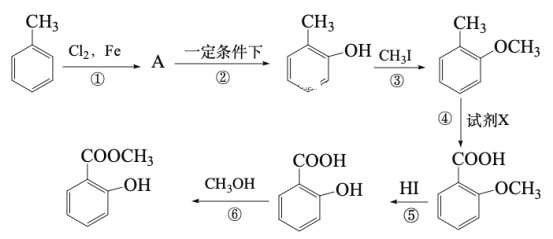
回答下列问题:
(1)有机物A的结构简式为___________________,习惯命名法A的名称为______________。
(2)反应②的化学方程式是________________________________________。
(3)试剂X是___________________。
(4)反应⑥ 的化学方程式是___________________________________。
(5)合成路线中设计③ 、⑤ 两步反应的目的是_____________________________。
(6)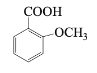 的同分异构体中,既能与NaHCO3发生反应,又能与FeCl3溶液发生显色反应的共有_________种,其中核磁共振氢谱为5组峰,且峰面积比为2:2:2:1:1的有机物结构简式为________________。
的同分异构体中,既能与NaHCO3发生反应,又能与FeCl3溶液发生显色反应的共有_________种,其中核磁共振氢谱为5组峰,且峰面积比为2:2:2:1:1的有机物结构简式为________________。
【答案】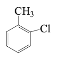 邻氯甲苯
邻氯甲苯  酸性KMnO4
酸性KMnO4 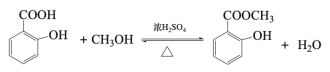 保护酚羟基,使之不被氧化 13
保护酚羟基,使之不被氧化 13 
【解析】
反应①是甲苯与Cl2在铁粉作催化剂的条件下发生苯环上的取代反应,从反应②的产物可知反应②是一个氯代烃的水解反应,可推出①发生邻位取代,则有机物A为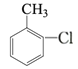 ,反应③是酚羟基中氢被甲基取代,反应⑤是将甲氧基又变为酚羟基,比较
,反应③是酚羟基中氢被甲基取代,反应⑤是将甲氧基又变为酚羟基,比较 和
和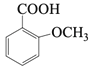 的结构可知,反应④是将甲基氧化成羧基的反应,所以试剂X为酸性高锰酸钾溶液,④是氧化反应,反应③和⑤的目的是保护酚羟基,防止酚羟基被酸性高锰酸钾溶液氧化;
的结构可知,反应④是将甲基氧化成羧基的反应,所以试剂X为酸性高锰酸钾溶液,④是氧化反应,反应③和⑤的目的是保护酚羟基,防止酚羟基被酸性高锰酸钾溶液氧化;
(1)分析知,有机物A的结构简式为 ,习惯命名法A的名称为邻氯甲苯;
,习惯命名法A的名称为邻氯甲苯;
(2) 反应②是一个氯代烃的水解反应,发生反应的化学方程式是 ;
;
(3) 反应④是将甲基氧化成羧基的反应,则试剂X为酸性高锰酸钾溶液;
(4)反应⑥是与甲醇的酯化反应,发生反应的化学方程式是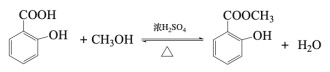 ;
;
(5) 合成路线中设计③、⑤两步反应的目的是保护酚羟基,使之不被氧化;
(6)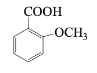 的同分异构体中,既能与NaHCO3发生反应,又能与FeCl3溶液发生显色反应,说明分子结构中含有酚羟基和羧基,则:苯环上有1个酚羟基、1个-COOH和1个甲基,共有10种;苯环上有1个酚羟基、1个-CH2COOH,共3种,满足条件的同分异构体共有13种;其中核磁共振氢谱为5组峰,,且峰面积比为2:2:2:1:1的有机物结构简式为
的同分异构体中,既能与NaHCO3发生反应,又能与FeCl3溶液发生显色反应,说明分子结构中含有酚羟基和羧基,则:苯环上有1个酚羟基、1个-COOH和1个甲基,共有10种;苯环上有1个酚羟基、1个-CH2COOH,共3种,满足条件的同分异构体共有13种;其中核磁共振氢谱为5组峰,,且峰面积比为2:2:2:1:1的有机物结构简式为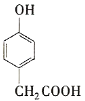 。
。


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:
【题目】实验室常用浓盐酸的质量分数为![]() ,密度为
,密度为![]() 。
。
(1)此盐酸的物质的量浓度为____________。
(2)需要![]() 的盐酸,配制时需以上浓盐酸的体积为_____
的盐酸,配制时需以上浓盐酸的体积为_____![]() 。
。
(3)上述实验中所用到的玻璃仪器有烧杯、玻璃棒、量筒以及____________(两种仪器)。
(4)用浓盐酸配制![]() 稀盐酸,操作步骤的正确顺序是__________(填字母代号)。
稀盐酸,操作步骤的正确顺序是__________(填字母代号)。
a.计算需要浓盐酸的体积
b.用量筒量取浓盐酸
c.将烧杯中的溶液注入所需容积的容量瓶中,并用少量蒸馏水洗涤烧杯和玻璃棒2~3次,洗涤液也注入容量瓶
d.把量好体积的浓盐酸倒入烧杯中,加适量蒸馏水稀释,冷却
e.盖好瓶塞,反复上下颠倒,摇匀
f.继续向容量瓶中加蒸馏水至刻度线下1~2cm处,改用某仪器小心滴加蒸馏水至凹液面与刻度线相平
(5)下列操作使溶液物质的量浓度偏高的是:____________。
A.量取浓盐酸时仰视刻度线
B.容量瓶洗净后未经干燥处理
C.未冷却至室温就转移定容
D.没有将洗涤液转移到容量瓶中
E.定容时俯视刻度线
F.摇匀后立即观察,发现溶液未达到刻度线,再加几滴蒸馏水至刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将两份过量的锌粉 a、b 分别加入定量的稀硫酸,同时向 a 中加入少量的 CuSO4 溶液,产生H2 的体积 V(L)与时间 t(min)的关系正确的是( )。
A.
B.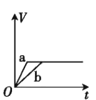
C.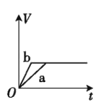
D.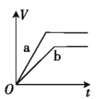
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某Na2CO3、NaAlO2的混合溶液中逐滴加入1molL1的盐酸,测得溶液中的CO32、HCO3、AlO2、Al3+的物质的量与加入盐酸溶液的体积变化关系如图所示。则下列说法正确的是( )(已知:H2CO3的电离平衡常数K1 = 4.3×107,K2 = 5.6×1011;Al(OH)3的酸式电离平衡常数K=6.3×1013)

A. a曲线表示的离子方程式为:AlO2+4H+ = Al3+ + 2H2O
B. M点时生成的CO2为0.05 mol
C. 原混合溶液中的CO32与AlO2的物质的量之比为1:2
D. V1:V2=1:4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依据氧化还原反应:2Ag+(aq) +Cu(s) =Cu2+(aq) +2Ag(s)设计的原电池如图所示。请回答下列问题:
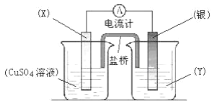
(1)电极 X 的材料是_____; 电解质溶液 Y 是________;
(2)银电极为电池的_____极,发生的电极反应为____________X 电极上发生的电极反应为__________
(3)外电路中的电子是从_____电极流向_____电极。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请运用原电池原理设计实验,验证 Cu2+、Fe3+氧化性的强弱。请写出电极反应式。
(1)负极 __________________________
(2)正极 __________________________________
(3)并在方框内画出实验装置图,要求用烧杯和盐桥,并标出外电路中电子流向。________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现将1.92gCu投入到一定量的浓HNO3中,Cu完全溶解,生成气体颜色越来越浅,共收集到标准状况下672mL的NOX混合气体,将盛有此气体的容器倒扣在水槽中,通入标准状况下一定体积的O2,恰好使气体完全溶于水,则通入标准状况下的O2的体积为( )
A. 504mLB. 336mLC. 224mLD. 168mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计如图装置(气密性已检查)制备Fe(OH)2白色沉淀。

请回答:
(1) 仪器1的名称________。装置5的作用________。
(2) 实验开始时,关闭K2,打开K1,反应一段时间后,再打开K2,关闭K1,发现3中溶液不能进入4中。请为装置作一处改进,使溶液能进入4中________。
(3) 装置改进后,将3中反应后溶液压入4中,在4中析出了灰绿色沉淀。从实验操作过程分析没有产生白色沉淀的原因________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com