
【题目】将两份过量的锌粉 a、b 分别加入定量的稀硫酸,同时向 a 中加入少量的 CuSO4 溶液,产生H2 的体积 V(L)与时间 t(min)的关系正确的是( )。
A.
B.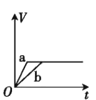
C.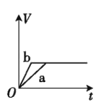
D.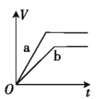
【答案】B
【解析】
两份锌粉a、b,分别加入稀H2SO4中,锌会置换出硫酸中的氢,生成氢气;同时向a中放入少量的CuSO4溶液,则会发生:Zn+Cu2+=Zn2++Cu,会形成原电池,反应速率增大,则a的曲线斜率大于b的斜率;由于锌过量,所以生成的氢气的体积与稀硫酸的物质的量成正比,由信息可知,生成的氢气的体积应该相等,由此结合选项判断。
过量的两份锌粉a、b,分别加入稀H2SO4中,同时向a中放入少量的CuSO4溶液,则a中还发生的反应为:Zn+Cu2+=Zn2++Cu,铜-锌-稀硫酸形成原电池,反应速率增大,反应用时少于b,由于锌过量,所以生成的氢气的体积由硫酸的物质的量决定,稀硫酸的量相同,所以最终两者产生的氢气体积相等,答案选B。


科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.由单质A转化为单质B是一个吸热过程,由此可知单质B比单质A稳定
B.500℃、30M Pa下,将0.5 mol N2和1.5 mol H2置于密闭容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为:N2(g)+3H2(g) ![]() 2NH3(g) ΔH = -38.6 kJ/mol
2NH3(g) ΔH = -38.6 kJ/mol
C.已知热化学方程式:2SO2(g)+O2(g) ![]() 2SO3(g) ΔH = -Q kJ/mol ,若将一定量的SO2(g)和O2(g)置于密闭容器中充分反应后放出热量Q kJ,则此过程中有2 mol SO2(g)被氧化
2SO3(g) ΔH = -Q kJ/mol ,若将一定量的SO2(g)和O2(g)置于密闭容器中充分反应后放出热量Q kJ,则此过程中有2 mol SO2(g)被氧化
D.X(g)+Y(g)![]() Z(g) ΔH >0,恒温恒容条件下达到平衡后加入X,上述反应ΔH增大
Z(g) ΔH >0,恒温恒容条件下达到平衡后加入X,上述反应ΔH增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钛铁矿是铁和钛的氧化物矿物,成分可表示为FeTiO3(Ti为+4价)。钛白粉(TiO2)涂料、塑料、油墨、造纸行业具有广泛的用途,制备流程如图:
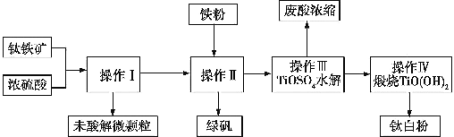
(1)钛铁矿与硫酸反应时可表示为FeTiO3+H2SO4→TiOSO4+X+H2O,其中X的化学式为 ______,该反应为______ (填“氧化还原反应”或“非氧化还原反应”)。
(2)某钛铁矿中FeTiO3的含量为76%,该钛铁矿与硫酸反应时Ti转化率为92%,操作I到操作IV的过程中Ti的转化率为96%,则1t该钛铁矿可生产钛白粉 ______ t(所有计算结果保留两位有效数字),能否计算绿矾的产量______?(若能则计算数值,否则说明理由)。
(3)操作I的名称是 ______,操作II包括搅拌、结晶、______,操作II中加入铁粉的目的是______(用离子方程式表示)。
(4)写出操作III中TiOSO4水解的化学方程式: ______ 。
(5)该生产过程中产生的尾气SO2、SO3的处理方法是 ______ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数值,下列说法正确的是( )
A.46gNO2和N2O4混合气体中含有原子数为3.5NA
B.50g质量分数为46%的乙醇水溶液中氧原子数为2NA
C.用惰性电极电解H2SO4溶液,若阳极产生5.6L气体,则电路中通过0.5NA电子
D.常温下,1LpH=3的醋酸溶液稀释到10L时,溶液中H+的数目大于0.01NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素X、Y、Z、W的原子序数依次增大。四种元素形成的单质依次为m、n、p、q; r、t、u是这些元素组成的二元化合物,其中u为葡萄酒中抑菌成分;25℃时,0.01mol/L的v溶液中: =1.0×10-10。上述物质的转化关系如图所示。下列说法正确的是( )
=1.0×10-10。上述物质的转化关系如图所示。下列说法正确的是( )
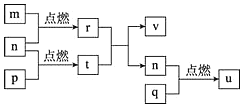
A.原子半径的大小:X<Y<Z<W
B.元素的非金属性:Y>W>X
C.t中只含离子键
D.v能抑制水的电离而u能促进水的电离
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能源开发、环境保护、资源利用等是当今社会的热门话题。请根据所学化学知识回答下列问题:
(1)汽车上安装催化转化器,可使汽车尾气中的主要污染物(CO、NOx、碳氢化合物)进行相互反应,生成无毒物质,减少汽车尾气污染。
已知:N2(g) + O2(g)=2NO(g) △H=+180.5 kJ·mol-1;
2C(s)+ O2(g)=2CO(g) △H=-221.0 kJ·mol-1;
C(s)+ O2(g)=CO2(g) △H=-393.5 kJ·mol-1;
则尾气转化反应2NO(g) +2CO(g)=N2(g)+2CO2(g)的△H=________________。
(2)某硝酸厂利用甲醇处理废水。在一定条件下,向废水中加入CH3OH,将HNO3还原成N2。若该反应消耗32 g CH3OH转移6 mol电子,则参加反应的还原剂和氧化剂的物质的量之比为______________。
(3)煤的间接液化是先转化为CO和H2,再在催化剂作用下合成甲醇。若在一定温度下,向1 L密闭容器中加入CO和H2,发生反应CO(g)+2H2(g)CH3OH(g),经10 min反应达到平衡时测得各组分的浓度如下:
物质 | CO | H2 | CH3OH |
浓度/(mol·L-1) | 1.2 | 1.0 | 0.6 |
①该反应的平衡常数表达式为:K=_____________________。
②该时间内反应速率υ(H2)=_________________。
③平衡时CO的转化率为_________________(保留1位小数)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有a、b、c、d四个金属电极,有关的反应装置及部分反应现象如下:
实验装置 | 部分实验现象 |
| a极质量减小,b极质量增加 |
| b极有气体产生,c极无变化 |
| d极溶解,c极有气体产生 |
| 电流计指示在导线中电流从a极流向d极 |
由此可判断这四种金属的活动性顺序是( )
A.a>b>c>dB.b>c>d>aC.d>a>b>cD.a>b>d>c
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用甲苯生产邻羟基苯甲酸甲酯: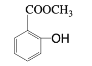 ,下列反应① ~⑥ 是其合成过程,其中某些反应条件及部分反应物或生成物未注明。
,下列反应① ~⑥ 是其合成过程,其中某些反应条件及部分反应物或生成物未注明。
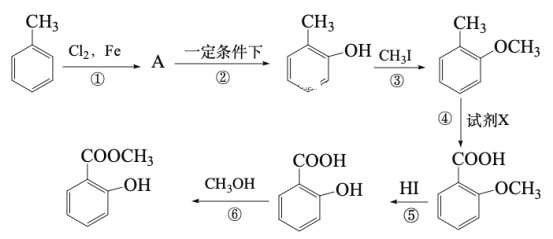
回答下列问题:
(1)有机物A的结构简式为___________________,习惯命名法A的名称为______________。
(2)反应②的化学方程式是________________________________________。
(3)试剂X是___________________。
(4)反应⑥ 的化学方程式是___________________________________。
(5)合成路线中设计③ 、⑤ 两步反应的目的是_____________________________。
(6)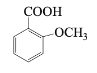 的同分异构体中,既能与NaHCO3发生反应,又能与FeCl3溶液发生显色反应的共有_________种,其中核磁共振氢谱为5组峰,且峰面积比为2:2:2:1:1的有机物结构简式为________________。
的同分异构体中,既能与NaHCO3发生反应,又能与FeCl3溶液发生显色反应的共有_________种,其中核磁共振氢谱为5组峰,且峰面积比为2:2:2:1:1的有机物结构简式为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物M具有广谱抗菌活性,合成M的反应可表示如下:
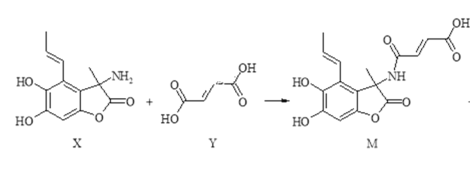 +H2O
+H2O
下列说法正确的是( )
A.X分子中有5种官能团
B.Y分子中所有原子不可能在同一平面内
C.可用FeCl3溶液或NaHCO3溶液鉴别X和M
D.在NaOH溶液中,1molX最多可与4molNaOH发生反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com