
����Ŀ��������Ԫ��W��X��Y��Z��ԭ��������������m��p��q��r��s������ЩԪ����ɵĶ�Ԫ��������³�ѹ��rΪҺ�壬�����Ϊ��ɫ���壬m��Ħ������Ϊp��2����n��Ԫ��Y�ĵ��ʣ�q��ʹƷ����Һ��ɫ��������ת����ϵ��ͼ��ʾ������˵���в���ȷ����
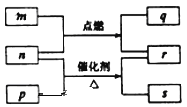
A. ԭ�Ӱ뾶��W<Y<X
B. �ǽ����ԣ�Y>X>W
C. m��q��n��s�����ܹ���
D. ��n������q�����Լ���ȼ��
���𰸡�D
�����������³�ѹ��rΪҺ��,ӦΪˮ,q��ʹƷ����Һ��ɫ,ӦΪ��������,��mӦΪ����,nΪ����,YΪOԪ��,m��Ħ������Ϊp��2��,����֪��pӦΪ������sΪNO,�ɴ˿���֪��WΪH,XΪN,ZΪS,�Դ˽�������
ͬһ���ڴ����ң�ԭ�Ӱ뾶��С����ԭ�Ӱ뾶��С���������Ϸ�������֪��XΪN��YΪO��WΪH����ԭ�Ӱ뾶N>O>H��A��ȷ��ͬ����Ԫ�طǽ�����O>N��H�ķǽ�������С��B��ȷ��mΪ����,���������������Ӧ���ɵ�������������NO������Ӧ���ɶ�������,���ܹ�����C��ȷ��������������������ȼ����D������ȷѡ��D��


 ��ѧ����ͬ����ϰϵ�д�
��ѧ����ͬ����ϰϵ�д� ��ǰ�κ�ͬ����ϰϵ�д�
��ǰ�κ�ͬ����ϰϵ�д� ����С��ҵϵ�д�
����С��ҵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���뵼�����(Si��Ge��)��ڶ����뵼�����(GaAs��InSb��)һ�𣬽������ƽ�����Ϣʱ��������������̼����(SiC)��������(GaN)Ϊ�����ĵ������뵼����ϵij��֣�������������Դ����Դ��Լ�������·�չ��Ҳ��Ϊ�˿�ѧ���о����ȵ㡣
��1��N��P��ASλ��ͬһ���壬��̬��ԭ�ӵĺ����___�ֲ�ͬ�˶�״̬�ĵ��ӣ�N2O�Ŀռ乹��Ϊ_______��
��2��̪ݼ�ܽ������ڹ����ϡ������Թ�ѧ���ϡ����ѧ�еĹ������������ȷ���õ��㷺��Ӧ�ã���ṹ��ͼ��ʾ����������Ϊ�����ӡ�̪ݼ����̼ԭ�ӵ��ӻ��������Ϊ___����������ͨ����λ����ϵĵ�ԭ�ӵı����_______��

��3��C��N����ͬ��������Ԫ�أ�C�γɵ�һ����Ҫ���ʿ�ȼ������Ȼ��ˮ����������νṹ��ͼA(�����С����ˮ���ӣ��ڲ��Ĵ����Ǽ������)��ͼA����С�Ļ������ӵ�ԭ��������_______����ȼ��������ж�����״�ṹ������һ����1��ͼA��ʾ���ֱ���2����������������ͬ����������ɣ����м���ʵ��ռ��____��ˮ���ӡ�

��4����֪PH3���ӵļ���ԼΪ94%����AsH3���ӵļ���ԼΪ91.8�������ü۲���ӶԻ������۽���PH3�ļ��DZ�AsH3�ļ��Ǵ��ԭ��________________��
��5��������������Ԫ���У�����һ�����ܴ�С����һ������������֮���Ԫ����____��
��6�������𡢵������������صĽṹ�����ڽ��ʯ���۵��������ʾ���Դӽṹ�ĽǶȷ��������۵㲻ͬ��ԭ��__________________��
���� | BN | AIN | GaN |
�۵�/�� | 3000 | 2200 | 1700 |
��7������������ͼ��ʾ����������ԭ��֮����������Ϊdpm��NA���������ӵ�������ֵ��������������ܶ�p=_____g/cm3��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������������DZͧ�ϵĺ˷�Ӧ����ʹ����Һ�����ƺϽ������Ƚ��ʣ����й���Al��Naԭ�ӽṹ�ķ�������ȷ����( )
A. ԭ�Ӱ뾶��Al��Na
B. ��һ�����ܣ�Al��Na
C. �縺�ԣ�Na��Al
D. ��̬ԭ��δ�ɶԵ�������Na��Al
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ����Ҫ��18mol/L��Ũ����ȷ����100mL2mol/L��ϡ���ᣬ��������������������ʹ�õ�
A.100 mL����ƿB.��ͷ�ι�C.�Թ�D.��Ͳ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��������ֻ�����ƺ�������Ԫ�أ���������������ˮ�з�Ӧ�����������壬�����������ֿ�����һ�������·�Ӧ����ˮ����ԭ�������ʵ�����ǣ� ��
A.Na2O2��Na2O
B.Na2O2
C.Na2O2��Na
D.Na��Na2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
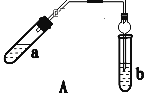
����Ŀ��ʵ������������������Ҫװ����ͼA��ʾ����Ҫ�������a�Թ��а�2��3��2�����������Ũ���ᡢ�Ҵ�������Ļ����ڰ�Aͼ����װ�ã�ʹ����������������ͨ��b�Թ���ʢ�ı���̼������Һ(���뼸�η�̪��Һ)�У���С�����a�Թ��еĻ��Һ���ܵ�b�Թ����ռ���Լ2 mL����ʱֹͣ���ȡ�����b�Թܲ�������Ȼ���ô�����Һ��ֲ㣻�ݷ��������������������
��ش��������⣺
(1) ������пɹ۲쵽b�Թ�����ϸС������ð����д���÷�Ӧ�����ӷ���ʽ��___��
(2) Aװ����ʹ�����ιܳ������������⣬��һ��Ҫ������___��������з���������������ʹ�õ�һ��������___��
(3) Ϊ֤��Ũ�����ڸ÷�Ӧ�����˴�������ˮ�������ã�ijͬѧ������ͼA��ʾװ�ý���������4��ʵ�顣ʵ�鿪ʼ���þƾ�����3min���ټ���ʹ֮����3min��ʵ�����������С�Թ�b�ٲ��л���ĺ�ȣ�ʵ���¼���£�
ʵ�� ��� | �Թ�a���Լ� | �Թ�b���Լ� | ����л���ĺ��/cm |
A | 3 mL�Ҵ���2 mL���ᡢ1mL 18mol��L-1Ũ���� | ����Na2CO3��Һ | 5.0 |
B | 3 mL�Ҵ���2 mL���� | 0.1 | |
C | 3 mL�Ҵ���2 mL���ᡢ6 mL 3mol��L-1H2SO4 | 1.2 | |
D | 3 mL�Ҵ���2 mL���ᡢ���� | 1.2 |
��ʵ��D��Ŀ������ʵ��C����գ�֤��H+��������Ӧ���д����á�ʵ��D��Ӧ��������������Ũ�ȷֱ���__mL��___mol��L-1��
�ڷ���ʵ��___(��ʵ����)�����ݣ������Ʋ��ŨH2SO4����ˮ����������������IJ��ʡ�Ũ�������ˮ���ܹ���������������ʵ�ԭ����___��
�ۼ���������������������IJ��ʣ���ʵ�鷢���¶ȹ������������IJ��ʷ������ͣ����ܵ�ԭ����___��
�ܷ�����������������ϴ�ӣ�Ϊ�˸�������������ѡ�õĸ����Ϊ__ (����ĸ)��
A.P2O5B.��ˮNa2SO4C.��ʯ��D.NaOH����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������û�������������������ų��ķ�������Ҫ��ѧ�ɷ�ΪSiO2(Լ45%)��Fe2O3(Լ40%)��Al2O3 (Լ10%)��MgO(Լ5%)����ͬѧ��������·�����������Ʒ�и��ֽ���Ԫ�ء�
��֪: Fe(OH)3��Ksp=4.0��10-38����ش��������⡣
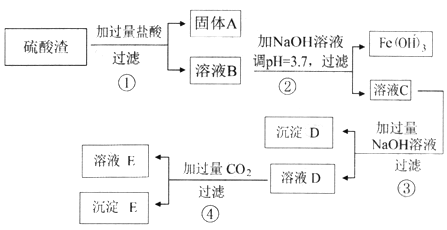
(1) ����A��һ�ֹ�ҵӦ��________������D�ĵ���ʽ___________��
(2) ��ҺB�������Ľ�����������___________��(д���ӷ���)
(3) ��������е�pH Ϊ3.0������ҺC�е�Fe3+ �Ƿ������ȫ��ͨ������˵��______��
(4) д���������ȫ����Ӧ�����ӷ���ʽ_______________��
(5) Ϊ�˷���ij����������Ԫ�صĺ������Ƚ�������Ԥ����������Ԫ����ԭ��Fe2+������KMnO4����Һ�����������½���������ԭ�ζ���
���жϵ���ζ��յ��������__________��
��ijͬѧ��ȡ2.000g��������Ԥ������������ƿ�����Ƴ�100mL ��Һ����ȡ25.00mL ������Һ����0.0050 mol/L KMnO4����Һ�ζ����ﵽ�ζ��յ�ʱ�����ı���Һ20.00mL�������������Ԫ�ص�����������_________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л��ϳ��У����Ὣ���������������ӣ�������ع����з�Ӧ���ͼ���ز��ﲻ�������ǣ�������
A.��ϩ �Ҷ����� 
B.������ �Ҵ���CH3CH2Br ![]() CH2�TCH2
CH2�TCH2 ![]() CH3CH2OH
CH3CH2OH
C.1���嶡�� 1��3������ϩ�� 
D.��ϩ ��Ȳ�� 
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±���Ԫ�����ڱ���һ���֡�
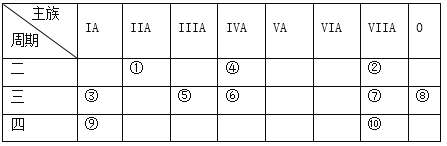
��Ա��еĢ١�����Ԫ�أ���Ԫ�ط��Ż�ѧʽ��ջش��������⣺
��1���ڢ١���Ԫ���У���������ǿ��Ԫ����_______������õķǽ���Ԫ����__________��
��2����ѧ��������õ�Ԫ����________����ԭ�ӵ�ԭ�ӽṹʾ��ͼΪ_________________��
��3��Ԫ�ص�����������Ӧ��ˮ������������ǿ����______________��������ǿ����___________�������Ե�����������____________��
��4���ڢڡ��ۡ���Ԫ���γɵļ������У����Ӱ뾶������________��
��5���ڢ����ĵ����У���ѧ���ʽϻ��õ���______������ʲô��ѧ��Ӧ˵������ʵ��д����Ӧ�Ļ�ѧ����ʽ����___________________________��
��6���ɢۺ͢���ɵĻ��������ˮ�Ƴɱ�����Һ����ʯīΪ�缫������Һ����д�������缫��Ӧʽ_________________________ ����������ѧʽ����_____________ ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com