
【题目】下表是元素周期表的一部分。
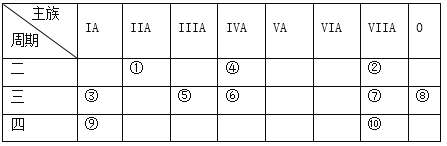
针对表中的①~⑩中元素,用元素符号或化学式填空回答以下问题:
(1)在①~⑩元素中,金属性最强的元素是_______,最活泼的非金属元素是__________。
(2)化学性质最不活泼的元素是________,其原子的原子结构示意图为_________________。
(3)元素的最高价氧化物对应的水化物中酸性最强的是______________,碱性最强的是___________,呈两性的氢氧化物是____________。
(4)在②、③、⑤元素形成的简单离子中,离子半径最大的是________。
(5)在⑦与⑩的单质中,化学性质较活泼的是______,可用什么化学反应说明该事实(写出反应的化学方程式):___________________________。
(6)由③和⑦组成的化合物,溶于水制成饱和溶液,用石墨为电极电解该溶液,请写出阳极电极反应式_________________________ ,阴极产物(填化学式)是_____________ 。
【答案】 K F Ar 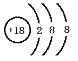 HClO4 KOH Al(OH)3 F- Cl2 Cl2+2NaBr=Br2+2NaCl 2Cl--2e- =Cl2↑ H2和NaOH
HClO4 KOH Al(OH)3 F- Cl2 Cl2+2NaBr=Br2+2NaCl 2Cl--2e- =Cl2↑ H2和NaOH
【解析】分析:由元素在周期表中的位置可以知道,(1)为Be,(2)为F,(3)为Na,(4)为C,(5)为Al,(6)为Si,(7)为Cl,(8)为Ar,(9)为K,(10)为Br。根据元素周期律进行解答。
(1)同周期自左而右金属性减弱、非金属性增强,同主族自上而下金属性增强、非金属性减弱,故上述元素中,金属性最强的元素是K,最活泼的非金属元素是F。因此,答案是:K;F。
(2)稀有气体Ar的化学性质最不活泼,其原子核外有18个电子,各层电子数为2、8、8,其原子结构示意图为: ,因此,答案是:Ar;
,因此,答案是:Ar; ;
;
(3)上述元素中除F(F没有正价)外Cl的非金属性最强,则最高价氧化物对应的水化物的酸性最强,该酸为HClO4,,K的金属性最强,则KOH的碱性最强,Al(OH)3为两性氢氧化物,因此,答案是: HClO4;KOH; Al(OH)3。
(4) ②为F、③为Na、⑤为Al,核外电子排布相同的粒子,核电荷数越大,粒子半径越小,所以F-离子半径最大;,因此,答案F-。
(5)同一主族从上到下非金属性减弱,单质的活泼性逐渐减弱,所以氯气的活泼性强于溴单质,可以通过水溶液中的置换反应来证明,反应方程式为: Cl2+2NaBr=Br2+2NaCl,因此答案是: Cl2; Cl2+2NaBr=Br2+2NaCl。
(6)由③为Na和⑦为Cl组成的化合物NaCl,溶于水制成饱和溶液,用石墨为电极电解该溶液,阳极电极反应式2Cl--2e- =Cl2↑,阴极电极反应式为:2H2O+4e-=H2↑+2OH-,所以阴极产物是H2和NaOH 。答案:2Cl--2e- =Cl2↑ H2和NaOH。


 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z的原子序数依次增大。m、p、q、r、s是由这些元素组成的二元化合物,常温常压下r为液体,其余均为无色气体,m的摩尔质量为p的2倍,n是元素Y的单质,q能使品红溶液褪色。上述的转化关系如图所示。下列说法中不正确的是
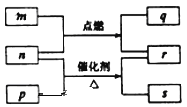
A. 原子半径:W<Y<X
B. 非金属性:Y>X>W
C. m与q、n与s均不能共存
D. 若n过量,q还可以继续燃烧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】10.8g某有机物A在纯氧中完全燃烧,仅生成二氧化碳30.8g,水7.2g,经过测定此有机物A相对分子质量为108.
(1)求此有机物A的分子式.
(2)若此有机物A跟FeCl3溶液作用显紫色,且有机物A与溴水反应,1mol 有机物A消耗3mol溴单质,写出此有机物A的结构简式以及A与溴水反应的化学方程式.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】席夫碱类化合物G有机合成、药物、新材料等方面有广泛应用。合成G的一种路线如下:
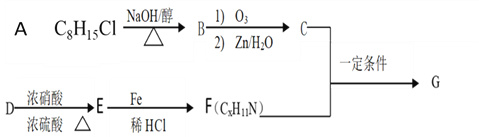
①![]()
②1molB经上述反应可生成2molC,且C不能发生银镜反应
③D属于单取代芳烃,其相对分子质量为106
④核磁共振氢谱显示F苯环上有两种化学环境的氢
⑤![]()
回答下列问题:
(1)B的化学名称_________________,A生成B的化学方程式___________________________________
(2)A 生成B , E 生成F的反应类型分别是__________,___________
C+F 生成G的化学方程式________________________________________________________________
(3)E的同分异构体中,含有苯环和氨基且能与碳酸氢钠反应生成CO2的共有_______种,其中核磁共振氢谱有五组峰,峰面积之比为1:2:2:2:2的结构简式为________________________(任意写一种)
(4)已知![]() 请以乙烯为原料,其他试剂任选,写出合成吸水材料聚丙烯酸钠的合成路线___________________________________________________________________________
请以乙烯为原料,其他试剂任选,写出合成吸水材料聚丙烯酸钠的合成路线___________________________________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X和Y是原子序数大于4的短周期元素,Xm+和Yn-两种离子的核外排布相同,下列说法中正确的是( )
A. X的原子半径比Y小 B. X和Y的核电荷数之差为m-n
C. 电负性X>Y D. 第一电离能X<Y
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,向10mL.0.1mol/LCaCl2溶液中滴加0.1mol/L的Na2CO3溶液。滴加过程中溶液中-1gc(Ca2+)与Na2CO3溶液体积(V)的关系如图所示,下列有关说法正确的是( )
(已知1g5=0.7)

A. x、y两点c(Ca2+)之比为2000:3 B. Ksp(CaCO3)=5×10-9
C. w点对应的分散系很稳定 D. x、y、z三点中,水的电离程度最大的为x点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢氧燃料电池是一种新型的化学电源,其构造如图一所示:a、b两个电极均由多孔碳制成,通入的气体由孔隙中逸出,并在电极表面放电。
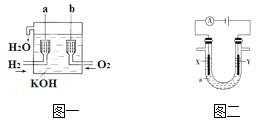
(1)a是________极,电极反应式是_______________________;b是________极.电极反应式是_______________________。
(2)该燃料电池生成了360 kg的水,则电路中通过了_____________mol的电子。
(3)用如图二所示电解方法精炼粗铜,电解液a选用CuSO4溶液,则:
①X电极的材料是________,电极反应式是___________________。
②Y电极的材料是______________,电极反应式是_____________________。(说明:杂质发生的电极反应不必写出)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化铝(AlN)广泛应用于电子、陶瓷等工业领域。在一定条件下,AlN的合成反应为:Al2O3+N2+3C=2AlN+3CO,该反应中发生氧化反应的物质是
A.Al2O3B.N2C.CD.Al2O3 和C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,0.1mol/L稀醋酸加水稀释,如图中的纵坐标y可以是( )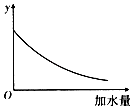
A.溶液的pH
B.醋酸的电离平衡常数
C.溶液中醋酸的物质的量浓度
D.醋酸的电离程度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com