
【题目】苯氧布洛芬是一种解热、阵痛、消炎药,其药效强于阿司匹林。可通过以下路线合成:
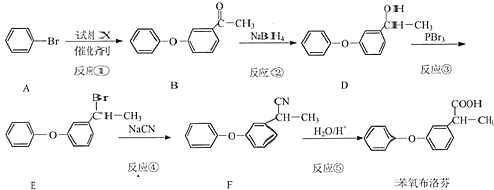
完成下列填空:
(1)反应①中加入试剂X的分子式为C8H8O2,X的结构简式为_______。
(2)反应①往往还需要加入KHCO3,加入KHCO3的目的是__________。
(3)在上述五步反应中,属于取代反应的是________(填序号)。
(4)B的一种同分异构体M满足下列条件:
Ⅰ.能发生银镜反应,其水解产物之一能与FeCl3溶液发生显色反应。
Ⅱ.分子中有6种不同化学环境的氢,且分子中含有两个苯环。则M的结构简式: ____。
(5)请根据上述路线中的相关信息并结合已有知识,写出以![]() 、CH2CHO。为原料制备
、CH2CHO。为原料制备![]() 的合成路线流程图(无机试剂任用)____。
的合成路线流程图(无机试剂任用)____。
合成路线流程图示例如下:CH3CH2OH![]() CH2=CH2
CH2=CH2![]()
![]()
【答案】![]() 中和生成的HBr ①③④
中和生成的HBr ①③④ ![]()
![]()
【解析】
反应①中加入试剂X的分子式为C8H8O2,对比溴苯与B的结构可知X为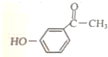 ,B中羰基发生还原反应生成D,D中羟基被溴原子取代生成E,E中-Br被-CN取代生成F,F水解得到苯氧布洛芬,据此解答。
,B中羰基发生还原反应生成D,D中羟基被溴原子取代生成E,E中-Br被-CN取代生成F,F水解得到苯氧布洛芬,据此解答。
(1)根据以上分析可知X的结构简式为 ,故答案为:
,故答案为: ;
;
(2)反应①属于取代反应,有HBr生成,加入KHCO3中和生成的HBr,
故答案为:中和生成的HBr;
(3)在上述五步反应中,反应①③④属于取代反应,故答案为:①③④;
(4)B的一种同分异构体M满足下列条件:Ⅰ.能发生银镜反应,说明含有醛基,其水解产物之一能与FeCl3溶液发生显色反应,含有甲酸与酚形成的酯基(-OOCH);Ⅱ.分子中有6种不同化学环境的氢,且分子中含有两个苯环,两个苯环相连,且甲基与-OOCH分别处于不同苯环中且为对位,则M的结构简式为:![]() ,
,
故答案为:![]() ;
;
(5)苯乙醛用NaBH4还原得到苯乙醇,在浓硫酸、加热条件下发生消去反应生成苯乙烯,苯乙烯与HBr发生加成反应得到![]() ,然后与NaCN发生取代反应得到
,然后与NaCN发生取代反应得到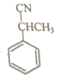 ,最后酸化得到
,最后酸化得到![]() ,合成路线流程图为:
,合成路线流程图为: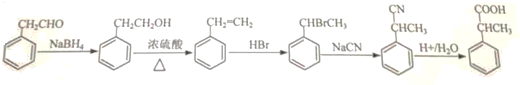 ,
,
故答案为: 。
。


科目:高中化学 来源: 题型:
【题目】(化学—有机化学基础)
3﹣对甲苯丙烯酸甲酯(E)是一种用于合成抗血栓药的中间体,其合成路线如下:
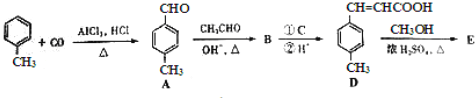
已知:HCHO+CH3CHO![]() CH2=CHCHO+H2O
CH2=CHCHO+H2O
(1)遇FeCl3溶液显紫色且苯环上有两个取代基的A的同分异构体有___________种,B中含氧官能团的名称为___________.
(2)试剂C可选用下列中的___________.
a、溴水
b、银氨溶液
c、酸性KMnO4溶液
d、新制Cu(OH)2悬浊液
(3)![]() 是E的一种同分异构体,该物质与足量NaOH溶液共热的化学方程式为___________.
是E的一种同分异构体,该物质与足量NaOH溶液共热的化学方程式为___________.
(4)E在一定条件下可以生成高聚物F,F的结构简式为___________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室以废铜为原料制取碱式碳酸铜(Cu2(OH)2CO3)的过程如下:
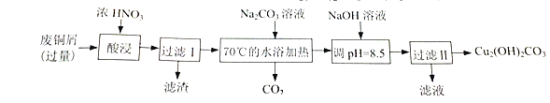
完成下列填空:
(1)酸浸中产生的气体是_________(填化学式)。
(2)检验过滤Ⅱ的沉淀是否洗净的方法是________。
(3)从实验流程中可看出影响产品生成的因素有多种,请写出其中两个:___________, 并任选其中一个因素,说明其原因___________。
(4)CuSO4溶液和纯碱溶液混合同样也可以制得Cu2(OH)2CO3,写出该反应的化学方程式:______。
(5)产品中Cu含量的测定步骤是:称取mg样品,用适量稀硫酸完全溶解,加水稀释,调节溶液为中性或弱酸性,再加入过量的KI-淀粉溶液后,用c mol/L的Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液v mL。实验中反应的离子方程式为2Cu2++4I-→2CuI(白色)↓+I2;I2+2S2O32-→2I-+S4O62-。
(i)样品溶于稀硫酸后,需加水稀释,控制溶液为中性或弱酸性,其原因是________。
(ii)产品中Cu的含量为__________________(用含m、c、v的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是由4个碳原子结合成的6种有机物(氢原子没有画出)
![]()
(1) 写出有机物(a)的系统命名法的名称___________________。
(2) 有机物(a)有一种同分异构体,试写出其结构简式__________________。
(3) 上述有机物中与(c)互为同分异构体的是________(填代号)。
(4) 任写一种与(e)互为同系物的有机物的结构简式____________。
(5) 上述有机物中不能与溴反应并使其褪色的有________(填代号)。
(6) (a)(b)(c)(d)四种物质中,4个碳原子一定处于同一平面的有________(填代号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,表中的每个字母表示一种短周期元素,回答下列问题:
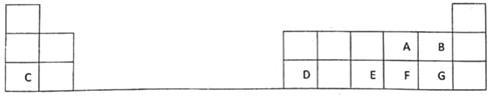
(1)画出A的原子结构示意图________。
(2)A、B、E、F、G五种元素所形成的气态氢化物最稳定的是________(填化学式)。
(3)D在元素周期表中的位置是第3周期________族。
(4)E、F元素的最高价氧化物对应水化物的酸性较强的是: ________(用化学式表示)。
(5)写出C和G形成化合物的电子式________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲~己元素在周期表中的相对位置如图。甲是形成化合物种类最多的元素,乙比甲原子序数多6,丁、戊、己属同周期元素,下列判断错误的是

A.乙的单质在空气中燃烧生成的化合物只含离子键
B.丙、己位于金属与非金属过渡线附近
C.丁与已核外电子数相差12
D.戊和己是过渡元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对如图两种化合物的结构或性质描述正确的是
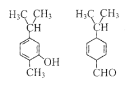
A.不是同分异构体
B.分子中共平面的碳原子数一定相同
C.均能与溴水反应且反应类型不同
D.可用NaOH溶液、银氨溶液、酸性KMnO4溶液区分
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】做完海带提碘实验后,实验室得到了含碘废液(含水、CCl4、可能含I2、I—、IO3—的一种或几种),为测定废液中碘的存在形式,并回收废液中的碘和CCl4,设计了如下实验方案。完成下列填空:
Ⅰ.判断废液中碘的存在形式(已知:5SO32—+ 2IO3—+2H+→I2+5SO42—+H2O)
实验中可供选择的试剂是:稀盐酸、淀粉溶液、氯化铁溶液、亚硫酸钠溶液
(1)观察废液,废液分为上下两次,有机层在____层(填“上”或“下”),呈____色。
(2)从废液中取少量水层溶液(pH≈8),滴加淀粉溶液,变为蓝色,该废水中含I2;另从废液中取适量水层溶液用CCl4多次萃取、分液,直到水层用淀粉溶液检验不出有I2存在;取________ ,该废水中含有I—;取______,该废水中不含IO3—。
Ⅱ.回收该废液中的碘和CCl4
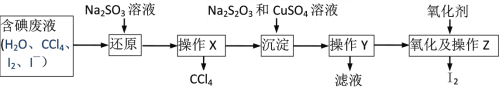
(3)向含碘废液中加入稍过量的Na2SO3溶液,将I2还原为I—,该操作的目的是_______;操作X名称是________。
(4)Na2S2O3、CuSO4溶液和I—反应生成CuI沉淀和Na2S4O6溶液,已知该含碘废液中碘元素的含量为10.33g/L,若回收500mL该含碘废液中的碘,则至少需要2mol/L的硫酸铜溶液_______mL。
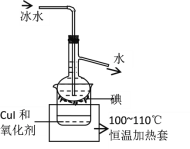
(5)将CuI转移入烧杯中,加入氧化剂在如图所示的装置中反应,一段时间后在蒸馏烧瓶底得到____色的固体碘。H2O2是一种性能优良的绿色氧化剂可将CuI氧化为I2,本实验不选用H2O2,可能的原因是_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com