
【题目】化石燃料是有机物的重要来源,从煤和石油获取的有机物苯和乙烯等简单有机物还是合成其他有机物的原料。如图的转化关系中,已知C能使碳酸钠溶液释放出CO2,反应①②反应机理类似且原子利用率均为 100%,请回答下列问题:
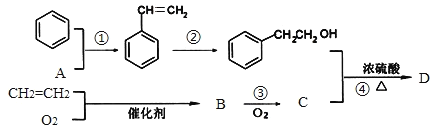
(1)有机物B中含有的官能团名称是_________________。
(2)反应①的反应类型为_________________。
(3)写出反应④的化学方程式__________________________。
(4)下列说法正确的是_________________。
A.乙烯与氧气在催化剂作用下反应也可以生成 C
B.纯C在 16.6℃ 以下呈冰状固体
C.在制备D时,D中常混有一些挥发出来的反应物,可以通过加入NaOH溶液振荡再分液的方法提纯
D.石油裂解气通过净化和分离也能得到丙烯这样的短链烯烃
【答案】醛基 加成反应 ![]() +CH3COOH
+CH3COOH ![]()
![]() +H2O ABD
+H2O ABD
【解析】
苯与乙炔CH≡CH在一定条件下发生加成反应,产生苯乙烯![]() ,苯乙烯与水发生加成反应产生
,苯乙烯与水发生加成反应产生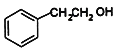 ;CH2=CH2被催化氧化产生的B是CH3CHO,乙醛催化氧化产生乙酸CH3COOH,乙酸与
;CH2=CH2被催化氧化产生的B是CH3CHO,乙醛催化氧化产生乙酸CH3COOH,乙酸与 发生酯化反应产生的D是乙酸苯乙酯
发生酯化反应产生的D是乙酸苯乙酯![]() 和水。
和水。
(1)有机物 B是CH3CHO,在B中含有的官能团名称是醛基;
(2)反应①是苯与乙炔发生加成反应产生苯乙烯,所以①的反应类型为加成反应;
(3)反应④是CH3COOH与苯乙醇发生酯化反应,产生乙酸苯乙酯和水,反应的化学方程式为:![]() +CH3COOH
+CH3COOH ![]()
![]() +H2O;
+H2O;
(4) A.乙烯与氧气在催化剂作用下反应,可以先氧化产生乙醛,然后进一步氧化产生乙酸,也可以直接氧化生成 C,A正确;
B.纯净的乙酸熔点是16.6℃,所以温度在16.6℃以下时,乙酸呈冰状固体,俗称冰醋酸,B正确;
C.在制备乙酸苯乙酯 ![]() 时,在D物质中常混有一些挥发出来乙酸,若向其中加入NaOH溶液振荡,乙酸与NaOH发生中和反应,而酯在NaOH溶液中也会发生水解反应,因此不能用这种方法分离提纯,C错误;
时,在D物质中常混有一些挥发出来乙酸,若向其中加入NaOH溶液振荡,乙酸与NaOH发生中和反应,而酯在NaOH溶液中也会发生水解反应,因此不能用这种方法分离提纯,C错误;
D.石油裂解气含有乙烯、丙烯等多种短链气态不饱和烃,可利用它们的性质的不同,通过净化和分离得到丙烯这样的短链烯烃,D正确;
故合理选项是ABD。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】NA代表阿伏加德罗常数的值。下列说法正确的是
A.将0.1mol CO2溶于适量的水,溶液中CO32-、HCO3-、H2CO3离子总数为0.1NA
B.在7.8gNa2O2与Na2S的混合物中,离子总数为0.3NA
C.使0.5mol乙烯被溴的四氯化碳溶液完全吸收,断裂的共价键总数为0.5NA
D.标准状况下,2.24L Cl2与CH4反应完全,生成物中气体分子数目小于0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列属于非氧化还原反应的是
A. 2Mg+CO2![]() 2MgO+CB. Cu(OH)2+2HCl=CuCl2+2H2O
2MgO+CB. Cu(OH)2+2HCl=CuCl2+2H2O
C. SO2+H2O2=H2SO4D. Br2+2NaI=2NaBr+I2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2是一种高效、广谱、安全的杀菌、消毒剂,易溶于水。制备方法如下:
(1)步骤Ⅰ:电解食盐水制备氯酸钠。用于电解的食盐水需先除去其中的 Ca2+、Mg2+、SO42-等杂质。在除杂操作时,往粗盐水中先加入过量的________(填化学式),至沉淀不再产生后,再加入过量的________和NaOH,充分反应后将沉淀一并滤去。
(2)步骤Ⅱ:将步骤Ⅰ得到的食盐水在特定条件下电解得到氯酸钠(NaClO3),再将它与盐酸反应生成ClO2与Cl2,ClO2与Cl2的物质的量比是____________。
(3)学生拟用左下图所示装置模拟工业制取并收集ClO2,用NaClO3和草酸(H2C2O4)恒温在60℃ 时反应制得。

反应过程中需要对A容器进行加热,加热的方式为____________;加热需要的玻璃仪器除酒精灯外,还有_________________;
(4)反应后在装置C中可得亚氯酸钠(NaClO2)溶液。已知NaClO2饱和溶液在温度低于38℃时,析出的晶体是NaClO2·3H2O,在温度高于38℃时析出的是NaClO2。根据右上图所示NaClO2的溶解度曲线,请完成从NaClO2溶液中制得NaClO2·3H2O的操作步骤:
①_____________;②_______________;③洗涤;④干燥。
(5)目前我国已成功研制出利用NaClO2制取二氧化氯的新方法,将Cl2通入到NaClO2溶液中。现制取270kg二氧化氯,需要亚氯酸钠的质量是________。
(6)ClO2和Cl2均能将电镀废水中的剧毒CN-氧化为无毒物质,自身被还原为Cl-。处理含CN-相同量的电镀废水,所需Cl2的物质的量是ClO2的_______倍。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知 4NH3+5O2 = 4NO+6H2O(g),若反应速率分别用 v(NH3)、v(O2)、v(NO)、v(H2O)表示,则正确的关系是( )
A.v(O2)=![]() v(NH3)B.v(H2O)=
v(NH3)B.v(H2O)= ![]() v(O2)C.v(H2O)=
v(O2)C.v(H2O)=![]() v(NH3)D.v(NO)=
v(NH3)D.v(NO)= ![]() v(O2)
v(O2)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用电解法无害化处理水体中的NO3-,最终生成N2逸出。其装置及转化如图所示。列说法正确的是

A.N电极为电源的负极
B.电解池工作时Na+移向电极Ⅱ
C.电极Ⅰ的电极反应:NO3-+8e+10H+=NH4++3H2O
D.电解池工作时电极Ⅰ产生的NH4+被电极Ⅱ产生的HClO氧化为N2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用绿矾(FeSO4·7H2O)制备补血剂甘氨酸亚铁[(H2NCH2COO)2Fe],有关物质性质如下:
甘氨酸(H2NCH2COOH) | 柠檬酸 | 甘氨酸亚铁 |
易溶于水,微溶于乙醇,两性化合物 | 易溶于水和乙醇,有酸性和还原性 | 易溶于水,难溶于乙醇 |
实验过程:
I.配制含 0.10molFeSO4 的绿矾溶液。
II.制备 FeCO3: 向配制好的绿矾溶液中,缓慢加入 200mL1.1mol/LNH4HCO3 溶液,边加边搅拌,反应结束后过滤并洗涤沉淀。
III.制备(H2NCH2COO)2Fe: 实验装置如下图(夹持和加热仪器已省略),将实验 II 得到的沉淀和含 0.20mol 甘氨酸的水溶液混合后加入 C 中,然后利用 A 中反应产生的气体将 C 中空气排净,接着滴入柠檬酸溶液并加热。反应结束后过滤,滤液经蒸发结晶、过滤、洗涤、干燥得到产品。

回答下列问题:
(1)实验 I 中:配制绿矾溶液时,为防止 FeSO4 被氧化变质,应加入试剂为_________ (写化学式)。
(2)实验 II 中:生成沉淀的离子方程式为_______________________________________。
(3)实验 III 中:
①装置 A中所盛放的药品是_______ (填序号)。
a.Na2CO3 和稀 H2SO4 b.CaCO3 和稀 H2SO4 c.CaCO3 和稀盐酸
②确认 C 中空气排尽的实验现象是___________________________________________。
③加入柠檬酸溶液一方面可调节溶液的 pH 促进 FeCO3 溶解,另一个作用是________。
④洗涤实验 III 中得到的沉淀,所选用的最佳洗涤试剂是__________ (填序号)。
a.热水 b.乙醇溶液 c.柠檬酸溶液
⑤若产品的质量为 17.34g,则产率为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列说法正确的是
A. 电解精炼铜,当外电路通过NA个电子时;阳极质量减少32 g
B. 反应3H2(g)+N2(g) ![]() 2NH3(g) △H=-92kJ·mol-1,当放出热量 9.2 kJ时,转移电子0.6 NA
2NH3(g) △H=-92kJ·mol-1,当放出热量 9.2 kJ时,转移电子0.6 NA
C. lmol·L-1的氯化铜溶液中,若Cl-的数目为2Na,则Cu2+的数目为Na
D. 标准状况下,NO和O2各11. 2L混合充分反应,所得气体的分子总数为0.75 Na
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物环丙叉环丙烷,由于其特殊的电导结构一直受到理论化学家的注意,其结构如图所示。有关它的说法中错误的是( )
![]()
A. 其二氯代物有4种 B. 它所有的原子均在同一平面上
C. 其分子式为C6H8 D. 它不可能是环丙烷的同系物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com