
����Ŀ����֪��Fe(s)+CO2(g)![]() FeO(s)+CO(g) K1 ��
FeO(s)+CO(g) K1 ��
Fe(s)+H2O(g)![]() FeO(s)+H2(g) K2 ��
FeO(s)+H2(g) K2 ��
H2(g)+CO2(g)![]() H2O(g)+CO(g) K3 ��
H2O(g)+CO(g) K3 ��
��֪��ͬ�¶��£�K1��K2ֵ���£�
�¶�/�� | K1 | K2 |
500 | 1.00 | 3.15 |
700 | 1.47 | 2.26 |
900 | 2.40 | 1.60 |
��1����500��ʱ���з�Ӧ����CO2��ʼŨ��Ϊ2 mol��L1��2 min����ƽ�⣬��CO2ת����Ϊ_________����CO��ʾ����ѧ��Ӧ����Ϊ____________��
��2��900��ʱ���з�Ӧ������ƽ�ⳣ��K3Ϊ___________����������ֵ�����ʱ䦤H_____0������������=������������������֪�÷�Ӧ���ڸ���ʱ����Ӧ�Է���������S_____0������������=��������������
��3������ͼ����Ϸ�Ӧ������____________�������������ͼ��v�����ʣ���Ϊ�������H2������ٷֺ�������

���𰸡���1��50% 0.5 mol��L1��min1
��2��1.50 �� �� ��3��BC
����������1����500��ʱ���з�Ӧ��������������ʽ�����ɵ�
Fe(s)+CO2(g) ![]() FeO(s)+CO(g)
FeO(s)+CO(g)
��ʼŨ����mol��L1�� 2 0
�仯Ũ����mol��L1�� x x
ƽ��Ũ�ȣ�mol��L1�� 2x x
K=![]() =1�����x=1��ת����=
=1�����x=1��ת����=![]() ��100%=50%����CO��ʾ����Ӧ����Ϊ
��100%=50%����CO��ʾ����Ӧ����Ϊ![]() = 0.5 mol��L1��min1��
= 0.5 mol��L1��min1��
��2��������ã�����=����900�����з�Ӧ������ƽ�ⳣ��K3Ϊ![]() =1.5����500����
=1.5����500����![]() ��ʱ��ȣ�ƽ�ⳣ�������ʱ䦤H��0������֪�÷�Ӧ���ڸ���ʱ����Ӧ�Է����������������ܹ�ʽ��G=��HT��S��0����S��0��
��ʱ��ȣ�ƽ�ⳣ�������ʱ䦤H��0������֪�÷�Ӧ���ڸ���ʱ����Ӧ�Է����������������ܹ�ʽ��G=��HT��S��0����S��0��
��3��������K2��ֵ�仯��֪�������¶�K2��С��ƽ�������ƶ�������ӦΪ���ȷ�Ӧ���������¶ȣ�ƽ�����淴Ӧ�����ƶ���A������ͼ��֪����ߵ㵽��ƽ�⣬�¶����ߣ��������H2������ٷֺ�����С����ƽ�����淴Ӧ������У�B��ȷ����ͼ��֪���¶�T2�ȵ���ƽ�⣬��T1��T2�������¶�ƽ�������ƶ���H2������ٷֺ�����С��C��ȷ������Ӧ����Ӧ���¶����߶�������D������


 ��ѧ����ͬ����ϰϵ�д�
��ѧ����ͬ����ϰϵ�д� ��ǰ�κ�ͬ����ϰϵ�д�
��ǰ�κ�ͬ����ϰϵ�д� ����С��ҵϵ�д�
����С��ҵϵ�д� �Ƹ�С״Ԫ����������ϰ��ϵ�д�
�Ƹ�С״Ԫ����������ϰ��ϵ�д� �ɹ�ѵ���ƻ�ϵ�д�
�ɹ�ѵ���ƻ�ϵ�д� ����ѵ����ֱͨ�п�����ϵ�д�
����ѵ����ֱͨ�п�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ�������йص������Һ��˵����ȷ����( )
A. ��Na2CO3��Һ��ˮϡ�ͺ�pH���Kw����
B. ����AgCl����ı�����Һ�м�����ˮ��c(Ag+)��Ksp(AgCl)������
C. pH=4.75Ũ�Ⱦ�Ϊ0.1mol/L��CH3COOH��CH3COONa�Ļ����Һ�У�c(CH3COO��)+c(OH��)
<c(H+)+c(CH3COOH)
D. �ֱ���pH=2��pH=3 �� CH3COOH��Һ�к͵����ʵ�����NaOH������CH3COOH��Һ������ֱ�ΪVa��Vb����10Va=Vb
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����KNO3������Ʒ�к���������KCl��BaCl2���ʣ�Ϊ���ᴿKNO3������õ�BaCl2����������ʵ�������

��1���������K2CO3��������Ӧ�����ӷ���ʽΪ_________________________________��
��2�������ͼ�����ʵ��ܽ�����߿�֪�����۵�������_________________��

��3��������Ϊ������֮ǰ��������������b��Ҳ�ܵõ������Ĺ���1������Ϊ�ù۵��Ƿ���ȷ������������______________________________________��
��4�����Ƶõ� KNO3�������� 200 mL0.2mol/L KNO3 ��Һ��
�ٱ�ʵ���õ�����������ƽ��ҩ�ס����������ձ�����ͷ�ιܡ���Ͳ������_______________��
�����������ʹ�����Ƶ�KNO3 ��Һ��Ũ��ƫ�ߵ���______________������ĸ����
A��û��ϴ���ձ��Ͳ����� B������ƿ�����������������ˮ
C������ʱ���ӿ̶��� D������ʱ���ӿ̶���
E�����ݺ�����ƿ������ҡ�ȣ����ú�Һ����ڿ̶��ߣ��ټ�ˮ���̶���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ӦA(g)+3B(g)![]() 2C(g)+2D(g)�ڲ�ͬ����µķ�Ӧ���ʣ����еķ�Ӧ����������
2C(g)+2D(g)�ڲ�ͬ����µķ�Ӧ���ʣ����еķ�Ӧ����������
A. v(A)=0.20 mol/(L��s) B. v(B)=0.30 mol/(L��s)
C. v(C)=0.50 mol/(L��s) D. v(D)=0.60 mol/(L��s)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ��һ·��ó��ʹ�������ɫ��Ʒ�߽������ճ�������������Ʒ����Ҫ�ɷֲ�������Ȼ�߷��ӵ��ǣ� ��
A. ���������������� B. �¹����������Ʒ
C. ̩���������е����� D. �������������̺
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪����ԭ��HSO3����I����������IO3����I2���ں�3mol NaHSO3����Һ����μ���KIO3��Һ������KIO3������I2�����ʵ����Ĺ�ϵ������ͼ��ʾ��
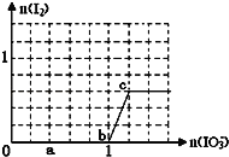
��1��a��ʱ����NaHSO3�����ʵ���Ϊ_____mol�����跴Ӧ����SO2�ݳ���
��2����b�㿪ʼ���㣬������0.3mol I2ʱ��ת�Ƶ�����Ϊ_______����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ҹ��Ŵ�����Ů洲������Ĵ�˵����������Ҳ�����������������⣬���в�ȡ�Ĵ�ʩ�������˵�����������ص���(����)
A���о����ʹ�������������β������Ⱦ
B����ֹʹ�ú��������
C������ʹ������ϴ�·�
D���ϸ�������᳧��β������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��DΪ���ֿ����Ե��Σ����ǵ������ӷֱ������Ba2+��Ag+��Na+��Cu2+�е�ijһ�֣������ӷֱ������NO3-��SO42��Cl-��CO32-���е�һ�֣��������������в����ظ����֣�
�����������ηֱ�����ʢ������ˮ����֧�Թ��У�ֻ��C�ε���Һ����ɫ��
������ٵ���֧�Թ��зֱ�������ᣬB�ε���Һ�г������ɣ�D�ε���Һ����ɫ��ζ�������ݳ���
���ݢ٢�ʵ����ʵ���ƶ����ǵĻ�ѧʽΪ��
��1��A_______________��
��2����D����Һ�еμ�������������ӷ���ʽ��______��D��ˮ��Һ�ʼ��Ե�ԭ���ǣ������ӷ���ʽ��ʾ����________________��
��3��д��C��Ba(OH)2��Һ��Ӧ�����ӷ���ʽ:___________________��
��4���ö��Ե缫���������B��Һ�����缫����4.32g��������������ڱ���µ����Ϊ_________�����Ļ�ѧ����ʽΪ______��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com