
【题目】电化学气敏传感器可用于监测环境中NH3的含量,其工作原理示意图如下。下列说法不正确的是( )

A. 溶液中OH﹣向电极b移动
B. O2在电极b上发生还原反应
C. a极的电极反应式为:2NH3﹣6e﹣+ 6OH﹣= N2 + 6H2O
D. 反应消耗的NH3与O2的物质的量之比为4:3
 优生乐园系列答案
优生乐园系列答案科目:高中化学 来源: 题型:
【题目】在一支25 mL的酸式滴定管中盛入0.lmol·L-1HCl溶液,其液面恰好在5 mL的刻度处,若把滴定管中的溶液全部放入烧杯中,然后以0.lmol·L-1 NaOH 溶液进行中和.则所需 NaOH 溶液的体积
A. 大于20 mL B. 小于20 mL C. 等于20 mL D. 等于5 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用天然气及化工废气中的硫化氢,不仅可制取氢气并回收单质硫,还可减少对环境的污染。
回答下列问题:
(1)在一定的条件下,天然气脱硫工艺中会发生以下反应:
2H2S(g)+3O2(g)=2SO2(g)+2H2O(g) ΔH1
4H2S(g)+SO2(g)=3S2(g)+4H2O(g) ΔH2
2H2S(g)+O2(g)=2S(g)+2H2O(g) ΔH3
则相同条件下反应2S(g)=S2(g)的△H=_______(用含△H1、△H2和△H3的代数式表示)。
(2)硫化氢分解反应2H2S(g)![]() 2H2(g)+S2(g),在101 kPa时各气体的体积分数与温度的关系如下图所示:
2H2(g)+S2(g),在101 kPa时各气体的体积分数与温度的关系如下图所示:

①该反应的△H______0(填“>”、“<”)。
②为提高H2S的平衡分解率,除改变温度外,还可采取的措施是______________________________。
③图中A点时反应的平衡常数Kp=______(用平衡分压代替浓度,平衡分压=总压×物质的量分数)。
(3)我国学者发明的一种分解硫化氢制氢并回收硫的装置如下图所示:

①该装置中能量转化的方式为____________________________________________________。
②若Y极液中的电对(A/B)选用I3-/I-,装置工作时Y极上的电极反应式为__________________________,Y极溶液中发生的离子反应为________________________________;再列举一种可作为Y极循环液常见的电对:_______________。
③该分解H2S制氢的方法主要优点是_____________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】开展中学化学实验研究很有意义。通过研究,可以发现一些实验装置的不足,从而可在此基础上改进实现。
(1)图甲为某版本教材中铜与浓硝酸反应的实验装置。

①铜与浓硝酸反应的化学方程式:________________________。
②装置中氢氧化钠溶液的作用是___________________________。
(2)小明对该实验进行如图乙的改进。装置乙和甲相比,实验过程中具有的优点是___________。
(3)用图乙所示装置进行实验时,小明发现上下抽动铜丝时,容易将试管塞抽出而有气体从软木塞逸出。于是又作图丙的改进。
①利用如图装置收集一试管NO2,请在方框内画出相应的装置图________。
②利用如图装置进行实验,实验中也具有乙的优点。要实现这一优点,实验过程中应进行的操作是____________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】LED产品的使用为城市增添色彩。下图是氢氧燃料电池驱动LED发光的一种装置示意图。下列有关叙述正确的是

A. a处通入氧气, b处通氢气
B. 通入H2的电极发生反应:H2-2e- = 2H+
C. 通入O2的电极发生反应:O2 + 4e- + 2H2O = 4OH-
D. 该装置将化学能最终转化为电能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属钒被誉为“合金的维生素”,常用于催化剂和新型电池。钒(V)在溶液中主要以VO43-(黄色)、VO2+(浅黄色)、VO2+ (蓝色)、V3+(绿色)、V2+(紫色)等形式存在。回答下列问题:
(1)已知:4Al(s)+3O2(g)=2Al2O3(s) △H1 4V(s)+5O2(g)=2V2O5(s) △H2
写出V2O5与Al 反应制备金属钒的热化学方程式__________________。(反应热用△H1、△H2表示)
(2) V2O5具有强氧化性,溶于浓盐酸可以得到蓝色溶液(含有VO2+),试写出V2O5与浓盐酸
反应的化学反应方程式:_________________________________。
(3)VO43-和V2O74-在pH≥13的溶液中可相互转化。室温下,1.0mol·L-1的Na3VO4溶液中c(VO43-)随c(H+)的变化如图所示。溶液中c(H+)增大,VO43-的平衡转化率_________(填“增大”“减小”或“不变”)。根据A点数据,计算该转化反应的平衡常数的数值为________。
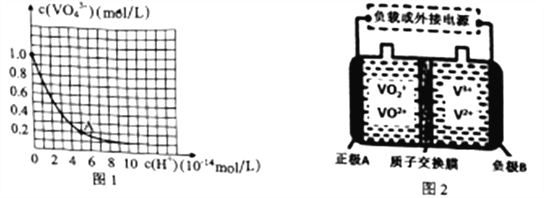
(4)全钒液流电池是一种优良的新型蓄电储能设备,其工作原理如图2所示:
①放电过程中,A电极的反应式为___________________。
②充电过程中,B电极附近溶液颜色变化为___________________。
③若该电池放电时的电流强度I=2.0A,电池工作10分钟,电解精炼铜得到铜mg,则电流利用率为______________(写出表达式,不必计算出结果。已知:电量Q=It,t为时间/秒;电解时Q=znF,z为每摩尔物质得失电子摩尔数,n为物质的量,法拉弟常数F=96500C/mol,电流利用效率=![]() ×100%)
×100%)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用电解法可用于治理亚硝酸盐对水体的污染,模拟工艺如图所示,下列说法不正确的是
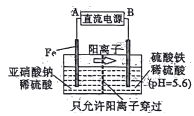
A. A、B分别为直流电源的正极和负极
B. 研究表明,当右侧区域pH较小时,会有气体逸出,该现象说明H+的氧化性强弱与其c(H+)有关
C. 电解过程中,左侧区域将依次发生反应为:Fe-2e-=Fe2+ 2NO2-+8H++6Fe2+=N2↑+6Fe3++4H2O
D. 当电解过程转移0.6mol电子时,左侧区域质量减少1.4g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下图中四个图象的说法正确的是( ) 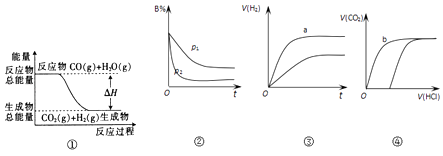
A.①表示反应CO(g)+H2O(g)CO2(g)+H2(g)中的△H大于0
B.②表示其它条件不变时,反应 4A(g)+3B(g)2C(g)+6D(?)在不同压强下B% 随时间的变化,则D一定是气体
C.③表示体积和pH均相同的HCl和CH3COOH两种溶液中,分别加入足量的锌,产生H2的体积随时间的变化,则a表示CH3COOH溶液
D.④表示10 mL 0.1mol/L Na2CO3和NaHCO3两种溶液中,分别滴加0.1mol/L HCl,产生CO2的体积随盐酸体积的变化,则b表示NaHCO3溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com