
【题目】LED产品的使用为城市增添色彩。下图是氢氧燃料电池驱动LED发光的一种装置示意图。下列有关叙述正确的是

A. a处通入氧气, b处通氢气
B. 通入H2的电极发生反应:H2-2e- = 2H+
C. 通入O2的电极发生反应:O2 + 4e- + 2H2O = 4OH-
D. 该装置将化学能最终转化为电能
科目:高中化学 来源: 题型:
【题目】(1)下列物质中,由极性键形成的非极性分子是____。
A.CO2 B.H2O C.CO D.CCl4
(2)近年来,我国北方地区雾霾频发。引起雾霾的PM2.5微细粒子包含(NH4)2SO4、NH4NO3、有机颗粒物及扬尘等。通过测定雾霾中锌等重金属的含量,可知交通污染是目前造成雾霾天气的主要原因之一。回答下列问题:
(1)基态O原子核外电子的运动状态有______种,其电子云形状有____种。
(2)基态Zn原子的核外电子排布式为____。
(3)(NH4)2SO4中存在的化学键类型有_______。
(4)N和F能形成化合物N2F2,N2F2中氮原子的杂化轨道类型为________,写出N2F2的一种结构式:____,1mol N2F2分子中所含σ键的数目是_________。
(5)下列说法正确的是________(填字母)。
a.N2O为直线形分子
b.C、N、O的第一电离能依次增大
c.O3与SO2、NO2-互为等电子体
d.相同压强下,HCOOH的沸点比CH3OCH3的高,说明前者是极性分子,后者是非极性分子
(6)测定大气中PM2.5浓度的方法之一是β-射线吸收法,其放射源可用85Kr。已知85 Kr晶体的晶胞结构如图所示。设晶胞中所含85Kr原子数为m,与每个85 Kr原子相紧邻的85 Kr原子数为n,则![]() _______(填数值)。该晶胞的边长为a nm,则85Kr晶体的密度为______g/cm3.(设NA为阿伏加德罗常数的值)
_______(填数值)。该晶胞的边长为a nm,则85Kr晶体的密度为______g/cm3.(设NA为阿伏加德罗常数的值)

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2016年9月,天宫二号发射成功,若在天宫二号空间实验室(失重条件下)进行以下实验,其中最难以完成的是( )
A. 将金粉和铜粉混合 B. 将牛奶加入水中混合
C. 蒸发食盐水制取食盐晶体 D. 用漏斗、滤纸过滤除去水中的泥沙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙醇可以发生下列反应,在反应里乙醇分子断裂H—O键的是( )
①乙醇与浓氢溴酸加热发生取代反应 ②乙醇与乙酸的酯化反应
③乙醇在浓硫酸存在下发生消去反应 ④乙醇与金属钠的反应
A. ①②B. ③④C. ①③D. ②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水分子间存在一种叫“氢键”的作用(介于范德华力与化学键之间)彼此结合而形成(H2O)n。在冰中每个水分子被4个水分子包围形成变形的正四面体,通过“氢键”相互连接成庞大的分子晶体,其结构示意图如图所示。

(1)1 mol H2O形成的冰中有________mol“氢键”。
(2)水分子可电离生成两种含有相同电子数的微粒,其电离方程式为________。
(3)在冰晶体中除氢键外,还存在范德华力(11 kJ·mol-1)。已知冰的升华热是51 kJ·mol-1,则冰晶体中氢键的能量是________ kJ·mol-1。
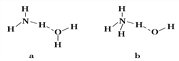
(4)氨气极易溶于水的原因之一也是与氢键有关。请判断NH3溶于水后,形成的NH3·H2O的合理结构是________(填序号)。
(5)NH3与PH3相比,热稳定性更强的是__________
(6)NH3、PH3在常温、常压下都是气体,但NH3比PH3易液化,其主要原因是____
A.键的极性N—H比P—H强
B.分子的极性NH3比PH3强
C.相对分子质量PH3比NH3大
D.NH3分子之间存在特殊的分子间作用力
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在生物体内含量极少,但对于维持生物体的正常生命活动必不可少的元素有( )
A. Fe、Mn、Zn、Cu B. Zn、Cu、Mg、Ca
C. Zn、Mg、B、Mn D. Mg、Mn、Cu、Mo
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各物质混合后,不能生成NaOH的是( )
A. Na和H2O B. Na2O2和H2O
C. Na2CO3和Ca(OH)2 D. NaCl和Ca(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(2015·上海)离子方程式2Ca2+ + 3HCO3– + 3OH– → 2CaCO3↓ + CO32– + 3H2O可以表示( )
A.Ca(HCO3)2与NaOH溶液反应
B.NaHCO3与澄清石灰水反应
C.Ca(HCO3)2与澄清石灰水反应
D.NH4HCO3与澄清石灰水反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能源是国民经济发展的重要基础,我国目前使用的能源主要是化石燃料。
(1)在25℃、101kPa时,16gCH4完全燃烧生成液态水时放出的热量是890.3kJ,则CH4燃烧的热化学方程式为_____________________。
(2)已知:C(s)+O2(g)=CO2(g);H=﹣437.3 kJ·mol﹣1
H2(g)+![]() O2(g)═H2O(g);H=﹣285.8 kJ·mol﹣1
O2(g)═H2O(g);H=﹣285.8 kJ·mol﹣1
CO(g)+![]() O2(g)═CO2(g);H=﹣283.0 kJ·mol﹣1
O2(g)═CO2(g);H=﹣283.0 kJ·mol﹣1
则煤气化反应C(s)+H2O(g)=CO(g)+H2(g) 的焓变H=_______kJ·mol﹣1。
(3)如图所示组成闭合回路,其中甲装置中CH4为负极,O2为正极,稀土金属材料为电极,以KOH溶液为电解质;乙装置中a、b为石墨,b极上有红色物质析出,CuSO4溶液的体积为400mL。

①装置中气体A为_____(填“CH4”或“O2和CO2”),d极上的电极反应式为________。
②乙装置中a极上的电极反应式为_____________。若在a极产生224mL(标准状况)气体,则甲装置中消耗CH4____mL(标准状况),乙装置中所得溶液的pH=___。(忽略电解前后溶液体秋变化)
③如果乙中电极不变,将溶液换成饱和Na2SO4溶液,当阴极上有a mol气体生成时,同时有w g Na2SO4·10H2O晶体析出,若温度不变,剩余溶液中溶质的质量分数应为_____(用含w、a的表达式表示,不必化简)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com