
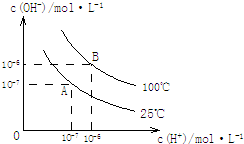
 在水的电离平衡中,c(H+)和c(OH-)的关系如图所示:
在水的电离平衡中,c(H+)和c(OH-)的关系如图所示:| Kw |
| c(H+) |
| Kw |
| c(OH-) |
| 10-12 |
| 0.01 |
| 10-12 |
| 10-7 |
| 10-4x-10-5y |
| x+y |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)海水中锂元素储量非常丰富,从海水中提取锂的研究极具潜力.锂是制造化学电源的重要原料.如LiFePO4电池中某电极的工作原理如图:
(1)海水中锂元素储量非常丰富,从海水中提取锂的研究极具潜力.锂是制造化学电源的重要原料.如LiFePO4电池中某电极的工作原理如图:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙烯与溴化氢加成 |
| B、CH3CH2CH2Br与NaOH水溶液共热 |
| C、丙烯与氯气加成 |
| D、CH3CHBrCH2CH3与NaOH醇溶液共热 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 镍锌电池具有绿色环保、大电流、性能好等优点,是电动玩具和数码产品的理想电源,如图是其工作原理示意图.下列说法正确的是( )
镍锌电池具有绿色环保、大电流、性能好等优点,是电动玩具和数码产品的理想电源,如图是其工作原理示意图.下列说法正确的是( )| A、a为电池负极,电池放电时发生还原反应 |
| B、电池放电时,负极附近区域pH升高 |
| C、电池充电时,阳极反应为2Ni(OH)2-2e-+2OH-═2NiOOH+2H2O |
| D、电池充电时,总反应为Zn+2NiOOH+H2O═ZnO+2Ni(OH)2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com