
 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案科目:高中化学 来源: 题型:阅读理解



| ||
| ||

| ||
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
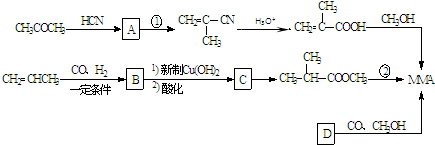
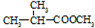 互为同分异构体,则其物质结构简式为:
互为同分异构体,则其物质结构简式为: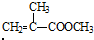 +CH3CH2CH2OH→
+CH3CH2CH2OH→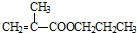 +CH3OH
+CH3OH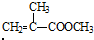 +CH3CH2CH2OH→
+CH3CH2CH2OH→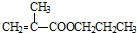 +CH3OH
+CH3OH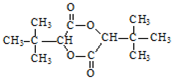 的合成路线流程图(无机试剂任选).合成路线流程图示例如图:
的合成路线流程图(无机试剂任选).合成路线流程图示例如图: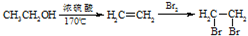
查看答案和解析>>
科目:高中化学 来源:必修一导学指导化学苏教版 苏教版 题型:013
|
有一种物质,既是工业上制玻璃和光导纤维的重要原料,又是重要的建筑材料,它的化学成分是 | |
| [ ] | |
A. |
Al2O3 |
B. |
MgO |
C. |
CaCO3 |
D. |
SiO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


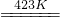 4KSbF6+2MnF3+F2
4KSbF6+2MnF3+F2查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com