
 完成下列空白.
完成下列空白.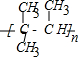 ;
; +3HNO3$→_{△}^{浓硫酸}$
+3HNO3$→_{△}^{浓硫酸}$ +3H2O.
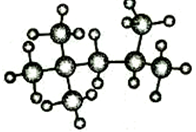
+3H2O. 分析 (1)由异辛烷的球棍模型可知其结构简式图: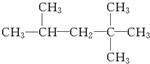 ,主链有5个碳原子,从左端编号,2号碳上有2个甲基,4号碳上有1个甲基,据此写出其名称;
,主链有5个碳原子,从左端编号,2号碳上有2个甲基,4号碳上有1个甲基,据此写出其名称;
(2)①碳碳双键断裂发生加成反应生成对应的烷烃,据此写出反应的化学方程式;
②2-甲基-2-丁烯,双键断裂,彼此首尾相连形成聚合物,据此写出反应方程式:
③甲苯与浓硝酸在浓硫酸做催化剂,吸水剂条件下加热生成2,4,6-三硝基甲苯和水.
解答 解:(1)由异辛烷的球棍模型可知其结构简式图: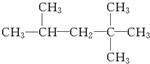 ,主链有5个碳原子,从左端编号,2号碳上有2个甲基,4号碳上有1个甲基,该烷烃的系统命名为:2,2,4-三甲基戊烷;
,主链有5个碳原子,从左端编号,2号碳上有2个甲基,4号碳上有1个甲基,该烷烃的系统命名为:2,2,4-三甲基戊烷;
故答案为:2,2,4-三甲基戊烷;
(2)①2,5-二甲基-2,4-己二烯的结构简式为(CH3)2C=CHCH=C(CH3)2,与氢气按照物质的量之比1:2发生加成反应生成相应的烷烃,反应的化学方程式为:(CH3)2C=CHCH=C(CH3)2+2H2$\stackrel{催化剂}{→}$ (CH3)2CHCH2CH2CH(CH3)2,
故答案为:(CH3)2C=CHCH=C(CH3)2+2H2$\stackrel{催化剂}{→}$ (CH3)2CHCH2CH2CH(CH3)2;
②2-甲基-2-丁烯的结构简式为:C(CH3)2=CHCH3,2-甲基-2-丁烯加聚反应的化学方程式为:C(CH3)2=CHCH3$\stackrel{引发剂}{→}$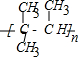 ,
,
故答案为:C(CH3)2=CHCH3$\stackrel{引发剂}{→}$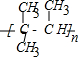 ;
;
③甲苯与浓硝酸在浓硫酸做催化剂,吸水剂条件下加热生成2,4,6-三硝基甲苯和水,化学方程式为 +3HNO3$→_{△}^{浓硫酸}$
+3HNO3$→_{△}^{浓硫酸}$ +3H2O,
+3H2O,
故答案为: +3HNO3$→_{△}^{浓硫酸}$
+3HNO3$→_{△}^{浓硫酸}$ +3H2O.
+3H2O.
点评 本题考查了有机物的系统命名,有机方程式书写,明确烷烃系统命名方法及有机物结构特别是所含官能团是解题关键,注意反应条件的书写,题目难度中等.


 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案 品学双优卷系列答案
品学双优卷系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
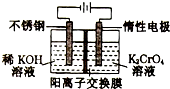 以铬酸钾(右室起始加入0.4molK2CrO4)为原料,电化学法制备重铬酸钾的实验装置示意图如下,下列说法不正确的是( )
以铬酸钾(右室起始加入0.4molK2CrO4)为原料,电化学法制备重铬酸钾的实验装置示意图如下,下列说法不正确的是( )| A. | 在阳极室,通电后溶液逐渐由黄色变为橙色 | |
| B. | 在阴极室,发生的电极反应为:2H2O+2e-═2OH-+H2↑ | |
| C. | 若测得右室中K与Cr的物质的量之比($\frac{nk}{ncr}$)为3:2,则此过程电路中共转移电子数为0.1NA | |
| D. | 若测定阳极液中K与Cr的物质的量之比($\frac{nk}{ncr}$)为d,则此时铬酸钾的转化率为2-d |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
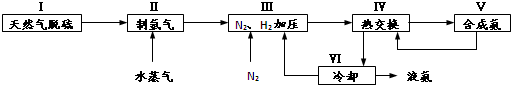
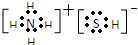 ,写出再生反应的化学方程式:2NH4HS+O2=2S↓+2NH3•H2O.NH3的沸点高于H2S,是因为NH3分子之间存在着一种比分子间作用力更强的作用力.
,写出再生反应的化学方程式:2NH4HS+O2=2S↓+2NH3•H2O.NH3的沸点高于H2S,是因为NH3分子之间存在着一种比分子间作用力更强的作用力.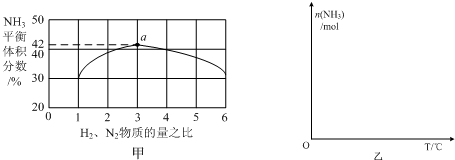
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 某种激光染料,应用于可调谐染料激光器,它由C、H、O三种元素组成,分子球棍模型如图所示,下列有关叙述正确的是( )
某种激光染料,应用于可调谐染料激光器,它由C、H、O三种元素组成,分子球棍模型如图所示,下列有关叙述正确的是( )| A. | ③④ | B. | ①④ | C. | ②③④ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在某反应中,当反应物具有的总能量大于生成物具有的总能量时,该反应吸热 | |
| B. | 同温同压下,4Al(s)+3O2(g)═2Al2O3(s)在常温和点燃条件下的△H不同 | |
| C. | 稀溶液中:H+(aq)+OH-(aq)═H2O(l);△H=-53.7KJ/mol,若将含0.5molH2SO4的浓溶液与含1molNaOH的溶液混合,放出的热量大于53.7kJ | |
| D. | 需要加热的化学反应一定是吸热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 甲、乙、丙、丁、戊是中学常见的无机物,其中甲、乙均为单质,它们的转化关系如图所示(某些条件和部分产物已略去).下列说法不正确的是( )
甲、乙、丙、丁、戊是中学常见的无机物,其中甲、乙均为单质,它们的转化关系如图所示(某些条件和部分产物已略去).下列说法不正确的是( )| A. | 若甲为短周期中原子半径最大的主族元素的单质,且戊为碱,则丙只能为Na2O2 | |
| B. | 若甲既能与盐酸反应又能与NaOH溶液反应,则丙可能属于两性氧化物 | |
| C. | 若丙、丁混合产生白烟,且丙为18电子分子,丁为10电子分子,则乙的水溶液可能具有漂白作用 | |
| D. | 若甲、丙、戊含有同一种元素,则三种物质中,该元素的化合价由低到高的顺序可能为:甲<丙<戊 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
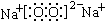 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com