
【题目】下列实验操作过程中不需要使用两开门圆底烧瓶的是
A.过滤 B.蒸馏 C.溶解 D.分液
科目:高中化学 来源: 题型:
【题目】常温下,在20.00 mL 0.1000 mol·L-1 NH3·H2O溶液中逐滴滴加0.1000 mol·L-1 HCl溶液,溶液pH随滴入HCl溶液体积的变化曲线如图所示。下列说法正确的是

A. ①溶液:c(Cl-)>c(NH)>c(OH-)>c(H+)
B. ②溶液:c(NH)=c(Cl-)>c(OH-)=c(H+)
C. ①、②、③三点所示的溶液中水的电离程度②>③>①
D. 滴定过程中不可能出现:c(NH3·H2O)>c(NH)>c(OH-)>c(Cl-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某一元弱酸(用HA表示)在水中的电离方程式是:HA![]() H++A﹣,回答下列问题:
H++A﹣,回答下列问题:
(1)向溶液中加入适量NaA固体,以上平衡将向______(填“正”、“逆”)反应方向移动。
(2)若向溶液中加水稀释,以上平衡将向_______(填“正”、“逆”)反应方向移动,溶液中c(A﹣)将____(填“增大”、“减小”或“不变”),溶液中c(OH﹣)将____(填“增大”、“减小”或“不变”)。
(3)已知室温时,0.1mol·L﹣1的某一元酸HA在水中有 0.1% 发生电离,回答下列各问题:
①该溶液的pH=_______。
②HA的电离平衡常数K=________。
③NaA溶液显碱性的原因:_____________________________(用离子方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下发生反应:2A(g)+2B(g)xC(g)+2D(g),在2L密闭容器中,把4molA和2molB混合,2min后达到平衡时生成1.6molC,又测得反应速率VD=0.2mol/(Lmin),下列说法正确的是( )
A.A和B的转化率均是20%
B.x=4
C.平衡时A的物质的量为2.8mol
D.平衡时气体压强比原来减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下向10 mL pH=3的醋酸溶液中加水稀释后,下列说法正确的是( )
A. 溶液中导电粒子的数目减少
B. 溶液中![]() 不变
不变
C. 醋酸的电离程度增大,c(H+)亦增大
D. 再加入10 mL pH=11的NaOH溶液,混合液pH=7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外小组运用电化学原理合成氨,其装置结构如图所示。下列有关说法不正确的是

A. 放电时,b极表面H2和CO均被氧化
B. 该电池工作时,H+由b极区迁移至a极区
C. a极的电极反应为N2+6H++6e-=2NH3
D. b极区发生反应CO+H2O=CO2+H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭容器中加入A,B两种气体,保持一定温度,在t1、t2、t3、t4时刻测得各物质的浓度如下:据此下列结论中正确的是( )
测定时刻/s | t1 | t2 | t3 | t4 |
C(A)/molL﹣1 | 6 | 3 | 2 | 2 |
C(B)/molL﹣1 | 5 | 3.5 | 3 | 3 |
C(C)/molL﹣1 | 1 | 2.5 | 3 | 3 |
A.在容器中发生的反应为2A(g)+B(g)2C(g)
B.该温度下,此反应的平衡常数为0.25
C.A的转化率比B转化率的低
D.在t3时刻反应已经停止
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质的分离或提纯,应选用下述方法的哪一种(填序号)
A.分液 B.过滤 C.萃取 D.蒸馏 E.蒸发结晶 F.加热分解
(1)除去CaCl2溶液中的CaCO3 ________。(2)从碘水中提取碘________。
(3)用自来水制取蒸馏水 _________。(4)分离植物油和水______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有阳离子交换膜、阴离子交换膜、石墨电极和如图所示的电解槽。用氯碱工业中的离子交换膜技术原理,可电解Na2SO4溶液生产NaOH溶液和H2SO4溶液。下列说法中正确的是
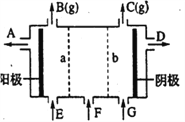
A. b是阴离子交换膜,允许Na+通过
B. 从A口出来的是H2SO4溶液
C. 阴极反应式为 4OH--4e-=2H2O+O2↑
D. Na2SO4溶液从G口加入
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com