
�����Ȼ�ѧ����ʽ��ȷ���ǣ�ע��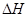 �ľ���ֵ����ȷ��( )
�ľ���ֵ����ȷ��( )
| A��C2H5OH(l)+3O2(g)=2CO2(g) +3H2O(g)����H=" ��1367.0" kJ/mol��ȼ���ȣ� |
| B��NaOH(aq) + HCl(aq)="NaCl(aq)" + H2O(l)����H= ��57.3kJ/mol���к��ȣ� |
| C��S(s) + O2(g) = SO2(g)����H= ��269.8kJ/mol����Ӧ�ȣ� |
| D��2HCl(g)=Cl2(g) + H2(g)����H=" ��" 184.6kJ/mol����Ӧ�ȣ� |
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��֪��Ӧ��H2(g) �� 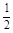 O2(g) �� H2O(g) ��H1
O2(g) �� H2O(g) ��H1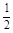 N2(g) �� O2(g) �� NO2 (g) ��H2
N2(g) �� O2(g) �� NO2 (g) ��H2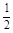 N2(g) ��
N2(g) �� 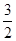 H2(g) �� NH3 (g) ��H3
H2(g) �� NH3 (g) ��H3
��Ӧ2NH3 (g) ��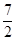 O2(g) ��2NO2 (g) ��3H2O(g) �ġ�H��
O2(g) ��2NO2 (g) ��3H2O(g) �ġ�H��
| A��2��H1��2��H2��2��H3 | B����H1����H2����H3 |
| C��3��H1��2��H2��2��H3 | D��3��H1��2��H2��2��H3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
����Zn(s)��H2SO4(aq)=ZnSO4(aq)��H2(g)����H=���Ļ�ѧ��Ӧ��������������ȷ����
| A����Ӧ������������ϵ����ͼ��ʾ����÷�ӦΪ���ȷ�Ӧ |
| B�����������Ϊԭ��أ�����32.5 gп�ܽ�ʱ�������ų�����һ��Ϊ11.2 L |
| C����ѧ��Ӧ���ʱ��뷴Ӧ����ʽ�ļ���ϵ���й� |
| D�������÷�Ӧ��Ƴ�ԭ��أ�пΪ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
������ͼ��ʾͼ��д����Ӧ���Ȼ�ѧ����ʽ���ش��������⣺

��1����Ӧ���̢ٵ��Ȼ�ѧ����ʽΪ��____________________________________________��
��2����Ӧ���̢ڵ��Ȼ�ѧ����ʽΪ��____________________________________________��
��3��Q2��Q1�Ĺ�ϵ��Q2________Q1(����ڡ���С�ڡ����ڡ�)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��������ѡ���У�ȫ��������ͼ��Ӱ���ֵ���Դ������ �� ��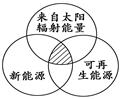
| A��ú̿��ʯ�͡����� | B��ˮ�ܡ������ܡ���Ȼ�� |
| C��̫���ܡ����ܡ���ϫ�� | D�������ܡ������ܡ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
ǿ����ǿ���ϡ��Һ�����кͷ�Ӧ����ЧӦ��H+(aq)+OH-(aq)=H2O��1�� ��H=��57��3kJ��mol����1L0��5mol��L��NaOH��Һ�м����������ʣ���ϡ���� ��Ũ���� ��ϡ���ᣬǡ����ȫ��Ӧʱ����ЧӦ��H1����H2����H3�Ĺ�ϵ��ȷ����
| A����H1>��H2>��H3 | B����H1<��H3<��H2 |
| C����H1<��H2<��H3 | D����H1>��H3>��H2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
���ڣ�2C4H10(g)+13O2(g)=8CO2(g)+10H2O(l)����H =��5800kJ/mol�������������
| A���÷�Ӧ�ķ�Ӧ��Ϊ��H=��5800kJ/mol���Ƿ��ȷ�Ӧ |
| B���÷�Ӧ�ġ�H������ʵ�״̬�йأ��뻯ѧ������Ҳ�й� |
| C����ʽ�ĺ���Ϊ��25�桢101kPa�£�2mol C4H10������ȫȼ������CO2��Һ̬ˮʱ�ų�����5800kJ |
| D���÷�ӦΪ����ȼ�յ��Ȼ�ѧ����ʽ���ɴ˿�֪�����ȼ����Ϊ5800kJ/mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
����˵����ȷ������ǣ� ��
(1)���ȷ�Ӧ����Ҫ���Ⱦ��ܷ�Ӧ�����ȷ�Ӧ�����ȾͲ��ܷ�Ӧ
(2)���ʷ�����ѧ�仯�����������ı仯
(3)���������仯�����ʱ仯���ǻ�ѧ�仯
(4)���ȷ�Ӧ�ͷ��ȷ�Ӧ���п����Է�����
(5)Naת��ΪNa��ʱ�����յ��������Ǹù��̵ķ�Ӧ��
(6)ˮ������ΪҺ̬ˮʱ�ų����������Ǹñ仯�ķ�Ӧ��
| A��(1)(2) | B��(3)(5) | C��(2)(6) | D��(2)(4) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
���ǵ����Ϻ����ḻ��һ��Ԫ�أ������仯�����ڹ�ũҵ������������������Ҫ���á���ش��������⣺
(1)��ͼ��N2��H2��Ӧ����2 mol NH3�����������仯ʾ��ͼ��д������NH3���Ȼ�ѧ����ʽ��________________________________________________________________________��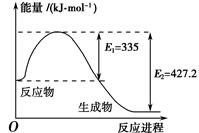
(2)����̬��̬ԭ���γ�1 mol��ѧ���ͷŵ���������м��ܡ��ӻ�ѧ���ĽǶȷ�������
ѧ��Ӧ�Ĺ��̾��Ƿ�Ӧ��Ļ�ѧ�����ƻ���������Ļ�ѧ�����γɹ��̡��ڻ�ѧ��Ӧ��
���У���ѧ����Ҫ�����������γɻ�ѧ���ֻ��ͷ�������
��֪��ӦN2(g)��3H2(g) 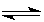 2NH3(g) ��H��a kJ��mol��1��
2NH3(g) ��H��a kJ��mol��1��
�Ը��ݱ������м������ݹ���a����ֵ��________��
| ��ѧ�� | H��H | N��H | N��N |
| ����kJ��mol��1 | 436 | 391 | 945 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com