
| 2.8L |
| 22.4L/mol |
| 3.36L |
| 22.4L/mol |
| 2.7g |
| 18g/mol |
| 2.8L |
| 22.4L/mol |
| 3.36L |
| 22.4L/mol |
| 2.7g |
| 18g/mol |
| 3.40g-0.3mol×1g/mol-0.125mol×12g/mol |
| 16g/mol |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| 实验 编号 | HA物质的量 | NaOH物质的量 | 混合溶液 |
| 浓度(mol?L-1) | 浓度(mol?L-1) | 的pH | |
| ① | 0.1 | 0.1 | pH=9 |
| ② | c | 0.2 | pH=7 |
| ③ | 0.2 | 0.1 | pH<7 |
查看答案和解析>>
科目:高中化学 来源: 题型:
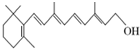 (1)如图的键线式表示维生素A的分子结构.
(1)如图的键线式表示维生素A的分子结构.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 实 验 事 实 | 理 论 解 释 |
| A. | SO2溶于水形成的溶液能导电 | SO2是电解质 |
| B. | 白磷为正四面体分子 | 白磷分子中P-P间的键角是109°28′ |
| C. | 1体积水可以溶解700体积氨气 | 氨是极性分子且由于有氢键的影响 |
| D. | HF的沸点高于HCl | H-F的键长比H-Cl的键长短 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com