
【题目】某柔性屏手机的柔性电池以碳纳米管做电极材料,以吸收ZnSO4溶液的有机高聚物做固态电解质,其电池总反应为MnO2+![]() Zn+(1+
Zn+(1+![]() )H2O+
)H2O+![]() ZnSO4
ZnSO4![]() MnOOH+
MnOOH+![]() ZnSO4[Zn(OH)2]3·xH2O。其电池结构如图甲所示,图乙是有机高聚物的结构片段。
ZnSO4[Zn(OH)2]3·xH2O。其电池结构如图甲所示,图乙是有机高聚物的结构片段。
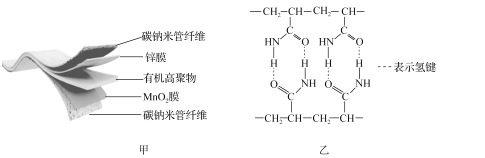
(1)Mn2+的核外电子排布式为_____;有机高聚物中C的杂化方式为_____。
(2)已知CN-与N2互为等电子体,推算拟卤(CN)2分子中σ键与π键数目之比为_____。
(3)NO2-的空间构型为_____。
(4)MnO是离子晶体,其晶格能可通过如图的Born-Haber循环计算得到。
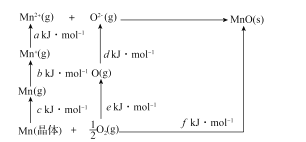
Mn的第一电离能是_____,O2的键能是_____,MnO的晶格能是_____。
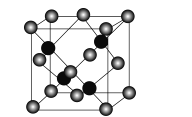
(5)R(晶胞结构如图)由Zn、S组成,其化学式为_____(用元素符号表示)。已知其晶胞边长为acm,则该晶胞的密度为_____g·cm3(阿伏加德罗常数用NA表示)。
【答案】1s22s22p63s23p63d5 sp2、sp3 3:4 V型 bkJmol﹣1 2ekJmol﹣1 (f-a-b-c-d-e)kJmol﹣1 ZnS ![]()
【解析】
(1) Mn元素的原子核外有25个电子,其基态原子电子排布式为1s22s22p63s23p63d54s2;根据价层电子对互斥理论判断C原子杂化方式;
(2) CN-和氮气分子互为等电子体,二者结构相同,根据氮气分子判断(CN)2分子中存在的σ键与π键的个数;
(3) NO2-中N原子的价层电子对数=2+![]() (5+1-2×2)=3,杂化类型是sp2,含有1个孤电子对,NO2-的空间构型是V型;
(5+1-2×2)=3,杂化类型是sp2,含有1个孤电子对,NO2-的空间构型是V型;
(4) Mn的第一电离能为气态Mn原子失去第一个电子时需要吸收的能量;由1molO2分子变成O原子的过程中,需要吸收的能量为2ekJ;晶格能是气态离子形成1mol离子晶体释放的能量;
(5) ZnS晶胞结构如图所示,利用均摊法找出晶胞中有4个Zn,有4个S,然后进行相关计算,求出晶胞密度。
(1) Mn元素的原子核外有25个电子,其基态原子电子排布式为1s22s22p63s23p63d54s2,则基态Mn2+的核外电子排布式为1s22s22p63s23p63d5;这些C原子中有些C原子价层电子对个数是3、有些是4,根据价层电子对互斥理论判断C原子杂化方式分别为sp2、sp3;故答案为:1s22s22p63s23p63d5;sp2、sp3;
(2)CN-与N2结构相似,C原子与N原子之间形成三键,则拟卤(CN)2分子结构式为![]() ,三键中含有1个σ键、2个π键,单键属于σ键,故(CN)2分子中σ键与π键数目之比为3:4,故答案为:3:4;
,三键中含有1个σ键、2个π键,单键属于σ键,故(CN)2分子中σ键与π键数目之比为3:4,故答案为:3:4;
(3) NO2-中N原子的价层电子对数=2+![]() (5+1-2×2)=3,杂化类型是sp2,含有1个孤电子对,NO2-的空间构型是V型,故答案为V型;
(5+1-2×2)=3,杂化类型是sp2,含有1个孤电子对,NO2-的空间构型是V型,故答案为V型;
(4)由图中Mn (晶体)![]() Mn (g)
Mn (g)![]() Mn+(g)过程,电离能为1mol的气态原子变为+1价阳离子的能量,故其第一电离能为bkJmol﹣1;由图中
Mn+(g)过程,电离能为1mol的气态原子变为+1价阳离子的能量,故其第一电离能为bkJmol﹣1;由图中![]() O2(g)
O2(g)![]() 2O(g)为
2O(g)为![]() molO=O的键能,故O=O键键能为ekJmol﹣1×2=2ekJmol﹣1;Mn晶格能为从气态离子形成1mol晶体放出的能量,根据盖斯定律,故晶格能=(f-a-b-c-d-e)kJmol﹣1,故答案为:bkJmol﹣1;2ekJmol﹣1;(f-a-b-c-d-e)kJmol﹣1;
molO=O的键能,故O=O键键能为ekJmol﹣1×2=2ekJmol﹣1;Mn晶格能为从气态离子形成1mol晶体放出的能量,根据盖斯定律,故晶格能=(f-a-b-c-d-e)kJmol﹣1,故答案为:bkJmol﹣1;2ekJmol﹣1;(f-a-b-c-d-e)kJmol﹣1;
(5)由晶胞的结构可知,Zn全部在晶胞的内部,所以1个晶胞中含有4个Zn2+,S分别位于晶胞的顶点和面心,根据晶胞中原子的“均摊法”可计算1个晶胞中S2-的个数为: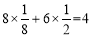 ,由Zn,S组成化学式为ZnS;1mol晶体的质量为97g,1mol晶胞的体积为NA a3cm3,因此该晶体的密度为
,由Zn,S组成化学式为ZnS;1mol晶体的质量为97g,1mol晶胞的体积为NA a3cm3,因此该晶体的密度为![]() ,故答案为:ZnS;
,故答案为:ZnS;![]() 。
。


 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案科目:高中化学 来源: 题型:
【题目】明矾石的主要成分是K2SO4·Al2(SO4)3·2Al2O3·6H2O,含有少量氧化铁,利用明矾石制备K2SO4的工艺流程如图所示:
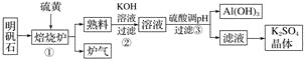
据此流程图回答下列问题:
(1)①焙烧炉中Al2(SO4)3与S反应的产物是两种氧化物,该反应的化学方程式为______;写出炉气的一种用途________。
(2)②中Al2O3参与反应的离子方程式为__________。
(3)③中调节pH不能用CO2的理由是____________________。
(4)工业冶炼金属铝需要定期更换补充阳极碳块的原因是__________________。
(5)纯净氢氧化铝经历两次__________________(填反应类型)可制得铝。以Al和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,放电时NiO(OH)转化为Ni(OH)2,该电池负极的电极反应式是__________________。
(6)现有明矾石1 625 t,按上述流程制得780 t Al(OH)3,忽略铝元素的损失,请计算明矾石中钾元素的质量分数为____________%。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计如图所示实验,探究反应中的能量变化。
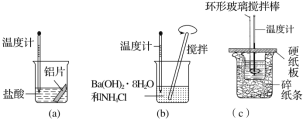
下列判断正确的是( )
A.由实验可知,(a)、(b)、(c)所涉及的反应都是放热反应
B.将实验(a)中的铝片更换为等质量的铝粉后释放出的热量有所增加
C.实验(c)中将环形玻璃搅拌棒改为铁质搅拌棒对实验结果没有影响
D.若用NaOH固体测定中和热,则测定中和热的数值偏高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Cl2是一种重要的化工原料,也是一种剧毒气体。某化学兴趣小组制备Cl2并探究Cl2相关性质的过程如下。回答下列问题:
(1)氯气的制备
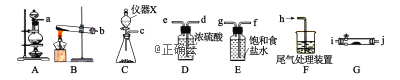
①上图中仪器X的名称是_________________,若用KMnO4和浓HCl反应制备Cl2则发生反应的化学方程式为_______________________________________________________;
②欲用二氧化锰和浓盐酸制备纯净干燥的Cl2,仪器接口的连接顺序为_______________;(根据气流方向,按照小写字母顺序填写)。
(2)制备的氯气与Fe粉在硬质玻璃管G中的反应,需采取________反应条件,将反应后的硬质玻璃管中固体溶于稀盐酸,取少量溶解后的溶液,检测其中金属阳离子种类:
实验编号 | 实验操作 | 实验现象 | 实验结论 |
① | 取少量待测液,滴加______溶液 | ____________ | 含有Fe2+ |
② | 取少量待测液,滴加______溶液 | ____________ | 含有Fe3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】第20届中国国际工业博览会上,华东师范大学带来的一种“锌十碘”新型安全动力电池亮相工博会高校展区。该新型安全动力电池无污染、高安全、长寿命且具有合适的充电时间,可以应用于日常生活、交通出行等各个领域。已知该电池的工作原理如图所示。下列有关说法正确的是( )
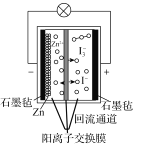
A.正极反应式为I3--2e-=3I-
B.6.5gZn溶解时,电解质溶液中有0.2mol电子移动
C.转移1mol电子时,有1molZn2+从左池移向右池
D.“回流通道”可以减缓电池两室的压差,避免电池受损
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含有酚类物质的废水来源广泛,危害较大。含酚废水不经处理排入水体,会危害水生生物的繁殖和生存;饮用水含酚,会影响人体健康。某科研结构研究出一种高效光催化剂BMO(Bi2MoO6),可用于光催化降解丁基酚,原理如图所示。下列说法错误的是( )
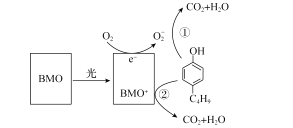
A.光催化剂BMO可降低丁基酚氧化反应的ΔH
B.在丁基酚氧化过程中BMO表现出强还原性
C.苯环上连有一OH和一C4H9的同分异构体共有12种(不考虑立体异构)
D.反应中BMO参与反应过程且可以循环利用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述错误的是

A. 图甲表示分别用NaOH溶液滴定等浓度等体积的盐酸和醋酸溶液反应变化曲线,指示剂都可用酚酞
B. 图乙表示分别用等浓度AgNO3溶液滴定等浓度等体积的NaCl、NaBr及NaI溶液反应变化曲线(X-表示Cl-、Br-、I-),则c为I–(溶度积常数:Ksp(AgI)<Ksp(AgBr)<Ksp(AgCl))
C. 图丙表示一定温度下,水溶液中H+和OH-的浓度变化曲线,b→a可能是加CuCl2溶液导致的
D. 图丁表示其他条件不变时,可逆反应A(g)+3B(g) ![]() 2C(g) ΔH<0 , C的物质的量分数与温度的关系
2C(g) ΔH<0 , C的物质的量分数与温度的关系
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】曲美替尼是一种抑制黑色素瘤的新型抗癌药物,下面是合成曲美替尼中间体G的反应路线:
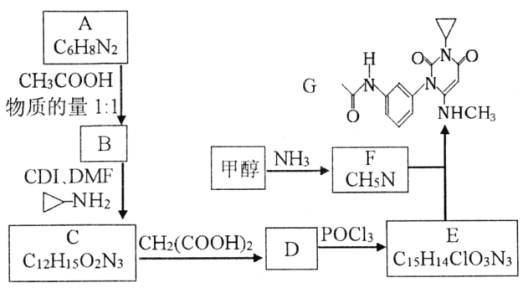
已知:①D分子中有2个6元环;
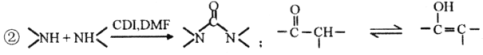
请回答:
(1)化合物A的结构简式___________。A生成B的反应类型___________。
(2)下列说法不正确的是___________。
A.B既能表现碱性又能表现酸性
B.1moC在碱溶液中完全水解最多可以消耗4 molOH-
C.D与POCl3的反应还会生成E的一种同分异构体
D.G的分子式为C16H18O3N4
(3)写出C→D的化学方程式____________________________________________。
(4)X是比A多2个碳原子的A的同系物,写出符合下列条件的X可能的结构简式:_______________________________________________________。
①1H-NMR谱显示分子中有3种氢原子,②IR谱显示分子中有苯环与-NH2相连结构
(5)流程中使用的DMF即N,N-二甲基甲酰胺结构简式为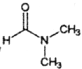 ,是常用的有机溶剂。设计以甲醇和氨为主要原料制取DMF的合成路线(用流程图表示,其他无机试剂任选)。_____________
,是常用的有机溶剂。设计以甲醇和氨为主要原料制取DMF的合成路线(用流程图表示,其他无机试剂任选)。_____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮及其化合物的转化过程如下图所示,其中如图为反应①过程中能量变化的曲线图。
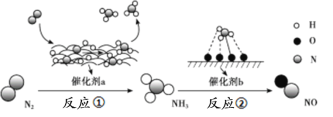

下列分析合理的是
A.如图中c曲线是加入催化剂a时的能量变化曲线
B.反应①的热化学方程式为:N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92 kJ/mol
2NH3(g) ΔH=-92 kJ/mol
C.在反应②中,若有1.25 mol电子发生转移,则参加反应的NH3的体积为5.6 L
D.催化剂a、b能提高化学反应①、②的化学反应速率和平衡转化率
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com