
【题目】下列变化中,不需要破坏化学键的是( )
A.氯化氢溶于水B.加热氯酸钾使其分解
C.干冰气化D.氯化钠熔化
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】(1)理论上讲,任何自发的氧化还原反应都可以设计成原电池,请利用反应“Cu +2Ag+![]() 2Ag + Cu2+”设计一个化学电池(正极材料用碳棒),回答下列问题:
2Ag + Cu2+”设计一个化学电池(正极材料用碳棒),回答下列问题:
①该电池的负极材料是 ;
②若导线上转移电子2.5mol,则正极生成银 克。
(2)现有A、B、C、D四种金属片,①把A、B用导线连接后同时浸入稀硫酸溶液中,A 上有气泡产生;②把C、D用导线连接后同时侵入稀硫酸溶液中,D发生还原反应;③把 A、C用导线连接后同时浸入稀硫酸溶液中,电子流动方向为A→导线→C。根据上述情况,回答下列向题
①在①中,金属片 发生氧化反应
②在②中,金属片 作负极,
③如果把B、D用导线连接后同时侵入稀硫酸溶液,则金属片 上有气泡产生。
④上述四种金属的活动顺序是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】写出下列反应的化学方程式:
(1)1-丁烯与溴水的反应 ______________________;
(2)乙醇与乙酸的反应____________________;
(3)用苯制溴苯的反应_________________________;
(4)乙醇的催化氧化_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上硝酸的制备和自然界中硝酸的生成既有相同的地方,又有区别。下图路线中的①-③、Ⅰ-Ⅲ分别是工业生产硝酸和雷电高能固氮过程中硝酸的生成途径。回答下列问题: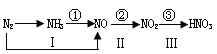
(1)雷电高能固氮生产硝酸的三个反应中,是否均为氧化还原反应?_______。
(2)图中途径I、①和②对应的三个反应中,常温下就能进行的是途径________。
(3)途径③对应的反应为NO2+H2O—HNO3+NO(未配平),该反应过程中氧化产物和还原产物的物质的量之比为__________________。
(4)硝酸必须保存于棕色瓶里并置于阴凉处的原因是____________________;可用铝质或铁质容器盛放冷的浓硝酸的原因是_____________________。
(5)硝酸的用途之一是与氨气反应制硝酸铵,其化学方程式为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲叉琥珀酸是化工生产的重要原料,广泛应用于化学合成行业。可通过以下路径合成:
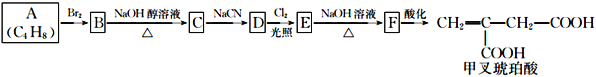
已知:
①B分子中只含两种不同化学环境的氢原子;
②R-Br+NaCN→R-CN+NaBr,R-CN![]() R-COONa+NH3↑,R-CCl3
R-COONa+NH3↑,R-CCl3![]() R-COONa+ NaCl。
R-COONa+ NaCl。
请回答下列问题:
(1)甲叉琥珀酸的分子式是_______________。
(2)A的结构简式为____________,B的化学名称是__________________。
(3)C分子中官能团的名称是_____________,C→D的反应类型是_______________。
(4)写出E→F的化学反应方程式:___________________________________________。
(5)M是甲叉琥珀酸的同分异构体,M分子中所含官能团与甲叉琥珀酸完全相同,M可能的结构共有___________种(不包括甲叉琥珀酸),其中核磁共振氢谱中只有三组吸收峰的同分异构体的结构简式为__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】组成人体细胞的主要元素含量占细胞鲜重的百分比前6位依次为( )
A. C、H、O、N、P、S B. C、O、N、H、P、S
C. O、C、H、N、P、S D. C、O、N、H、S、P
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.石油和天然气属于一次能源
B.绿色植物进行光合作用时,太阳能转化为化学能
C.燃料燃烧时,化学能全部转化为热能
D.石墨转化为金刚石是吸热反应,故石墨能量比金刚石能量低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)固体可分为晶体、非晶体和准晶体三大类,可通过________________方法区分晶体、非晶体和准晶体,以色列科学家丹尼尔·谢赫特曼因发现锰的化合物准晶体而独享了2011年诺贝尔化学奖。基态Mn原子的电子排布式为_______________。
(2)PCl3的立体构型为______________,中心原子的杂化轨道类型_______________。
(3)硼的卤化物在工业中有重要作用,硼的四种卤化物的沸点如下表所示。
BF3 | BCl3 | BBr3 | BI3 | |
沸点/K | 172 | 285 | 364 | 483 |
①四种卤化物沸点依次升高的原因是___________________。
②B、C、N、O三种元素第一电离能由小到大的顺序为___________。
③用BF3分子结构解释反应BF3(g)+NH4F(s)=NH4BF4(s)能够发生的原因:____________。
(4)碳元素的单质有多种形式,下图依次是C60、石墨和金刚石的结构图:
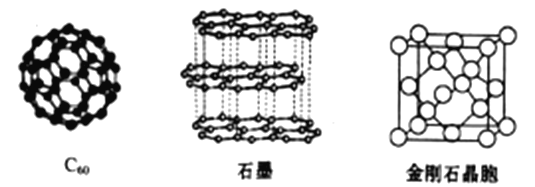
回答下列问题
①石墨晶体中,层内C-C键的键长为142pm,而金刚石中C-C键的键长为154pm,其原因是金刚石中只存在C-C间的________共价键,而石墨层内的C-C间存在_________键。
②金刚石晶胞含有___________个碳原子。若碳原子半径为r,金刚石晶胞的边长为a,列式表示碳原子在晶胞中的空间占有率__________(不要求计算结果)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是100mg CaC2O4H2O受热分解时,所得固体产物的质量随温度变化的曲线.试利用图中信息结合所学的知识,回答下列各问题: 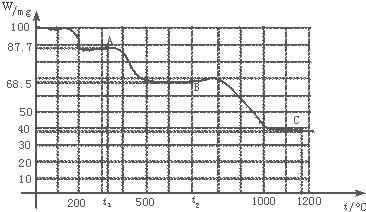
(1)温度分别为t1和t2时,固体产物的化学式A是 , B是 .
(2)由CaC2O4H2O得到A的化学方程式为 .
(3)由A得到B的化学方程式为 .
(4)由图计算产物C的相对分子质量,并推断C的合理的化学式.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com