
����Ŀ���Ӻ�ˮ�п�����ȡ�ܶ����õ����ʣ�����Ӻ�ˮ�������õ���±ˮ�п�����ȡ�⡣����̿�������ǹ�ҵ���ķ���֮һ�����������£�

������ʾ����pH=2ʱ��NaNO2��Һֻ�ܽ�I-����ΪI2,ͬʱ����NO��
��I2+5Cl2+6H2O=2HIO3+10HCl��
��5SO32-+2IO3-+2H+=I2+5SO42-+H2O��
����I2�ڼ�����Һ�з�Ӧ����I-��IO3-��
(1)��Ӧ�������ӷ���ʽ_____________��
(2)�������У�����I2�����ԣ��������X��������________________��
(3)��֪����Ӧ����ÿ����3molI2ת��5mol���ӣ������ӷ���ʽ��_______________��
(4)Cl2������KMnO4�ȶ��dz��õ�ǿ�����������ù���������±ˮ�е�I-ȴѡ���˼۸�ϸߵ�NaNO2,ԭ����_______________��
(5)�������У���֪��Ӧ�����˺���Һ���Դ���������I2��I-��IO3-����ֱ������Һ�е�I-��IO3-����ʵ�鷽������������ʵ���пɹ�ѡ����Լ���ϡH2SO4��������Һ��Fe2(SO4)3��Һ��Na2SO3��Һ
A����Һ��CCl4�����ȡ����Һ��ֱ��ˮ���õ�����Һ���鲻���ⵥ�ʴ��ڡ�
B��_______________________��
���𰸡� 2NO2-+2I-+4H+ =I2+2NO��+2H2O ����������ȣ��������ᾧ���������ᾧ���۷֣� 3I2+3CO32-=5I-+IO3-+3CO2������3I2+6CO32-+3H2O=5I-+IO3-+6HCO3-�� ���������Ը�����صȶ��dz��õ�ǿ�����������������I2(���������ƽ��ܰѵ����������ɵⵥ�ʣ���˼�Լ���) ��ˮ��ȡ������Һ���Թ��У����뼸�ε�����Һ���μ�Fe2(SO4)3��Һ������Һ������˵����Һ�к���I��������ˮ����ȡ������Һ���Թ��У����뼸�ε�����Һ���������ữ���μ�Na2SO3��Һ������Һ������˵����Һ�к���IO3��
����������Ӧ���ǵ����ӱ����������������ɵ��ʵ⣬Ȼ�����û���̿�������ʵ⡣�����������õ����������롣������������Ũ̼������Һ���յ��ʵ⣬ת��Ϊ������͵����ӣ���������Һ�ж����ַ���������ԭ��Ӧ���ɵ��ʵ⣬�ݴ˽��
��1����Ӧ��ΪpH=2��Һ�����ԣ�NaNO2��Һ��I������ΪI2��ͬʱ����NO�����䷴Ӧ�����ӷ���ʽΪ��2NO2��+2I��+4H+��I2+2NO��+2H2O��
��2������I2�����������ԣ��������X�ķ�������������ȡ������ᾧ��
��3��������֪��������Ӧ����ÿ����3molI2ת��5mol���ӣ������������ԭ��Ӧ�е�ʧ������Ϊ5����0������Ϊ+5�ۺʹ�0�۽���Ϊ-1�ۣ���������ӷ�Ӧ����ʽ�ǣ�3I2+3CO32��=5I��+IO3��+3CO2����3I2+6CO32��+3H2O=5I��+IO3��+6HCO3����
��4��Cl2������KMnO4�ȶ��dz��õ�ǿ�����������ù���������±ˮ�е�I��ȴѡ���˼۸�ϸߵ�NaNO2��ԭ�������������Ը�����صȶ��dz��õ�ǿ�����������������I2���Ӷ��ò���I2��
��5��������Һ�е�I������ѡ���������������������ĵⵥ�������۱�����������Һ�е�IO3�������û�ԭ�����仹ԭ�����ⵥ�������۱��������ʵ�鷽��Ϊ����ˮ��ȡ������Һ���Թ��У����뼸�ε�����Һ���μ�Fe2(SO4)3��Һ������Һ������˵����Һ�к���I��������ˮ����ȡ������Һ���Թ��У����뼸�ε�����Һ���������ữ���μ�Na2SO3��Һ������Һ������˵����Һ�к���IO3����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˹��ѧ�������û������������е�ʵ���У��ú�20�����ӵĸ�Ԫ�ص�ͬλ�ط��������95�����ӵ���Ԫ�أ�����ɹ��Ƶ�4����115��Ԫ�ص�ԭ�ӡ�����NԪ��ͬ���壮��4��ԭ�������������˥��ɵ�113��Ԫ�أ�ǰ�ߵ�һ�ֺ���Ϊ![]() �������й�������ȷ���ǣ� ��
�������й�������ȷ���ǣ� ��
A. 115��Ԫ��˥���113��Ԫ���ǻ�ѧ�仯
B. 115��Ԫ��X�Ľ������ԭ������Ϊ288
C. 113��Ԫ�ص�ԭ���������3������
D. ��115��Ԫ����NԪ��ͬ���壬�����Ƿǽ���Ԫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��MnCO3�������Ʊ����Ե缫����MnO2�������̿�MnCO3��SiO2��FeCO3������Al2O3�ȣ�Ϊԭ���Ʊ�̼���̴ֲ�Ʒ���������£�
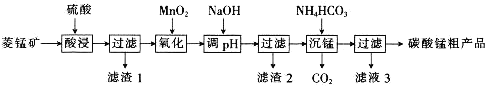
��֪���ٳ����£�Ksp[Fe(OH)3]=8.0��10��38��Ksp[Al(OH)3]=4.0��10��34��
���������������������Al3+��Fe3+��ȫ������pH�ֱ�Ϊ4.6��3.4��Mn2+��ʼ������pHΪ8.1��
��1��������������в�����Ũ����������ᣬԭ����_________________________________��
��2�������ӷ���ʽ��ʾ�������������м�MnO2��Ŀ�ģ�______________________________��
��3������pH��ʱ���������������������Ļ����Һ�еμ�����������Һ�����ֳ������棬��c(Fe3+)=1.0��10��5mol��L��1ʱ��c(Al3+)=______________mol��L��1��
��4���١����̡������У���Ӧ�����ӷ���ʽΪ__________________________________��
�ڡ����̡������г����������¶ȵĹ�ϵ��ͼ��ʾ��
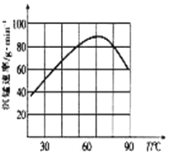
���¶ȸ���60��ʱ���������������¶����߶�������ԭ�������___________________��
��5������Һ3�пɷ����һ�ֲ���̼Ԫ�صĵ��ʣ����Ļ�ѧʽΪ___________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��19����ϩ�Ʒӣ��ṹ��ʽ����ͼ��ʾ������һ�ּ�����ҩ�������������ȷ����( )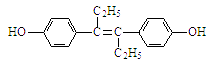
A.��ϩ�Ʒӵķ���ʽΪC18H20O2
B.��ϩ�Ʒ���NaOH��Һ��NaHCO3��Һ���ܷ�Ӧ
C.1 mol��ϩ�Ʒ��������2mol Na������Ӧ
D.��ϩ�Ʒ��뱥����ˮ���Է����ӳɷ�Ӧ��ȡ����Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��1,3-����ϩ������������ 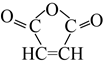 ������Ҫ�Ļ���ԭ�ϣ������ںϳɿɽ����PBS���Ϻ��¿��ᡣ
������Ҫ�Ļ���ԭ�ϣ������ںϳɿɽ����PBS���Ϻ��¿��ᡣ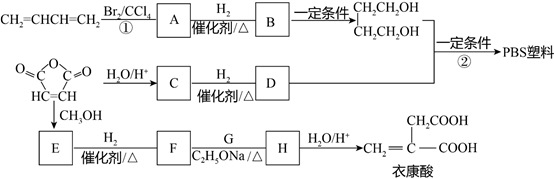
��֪�� 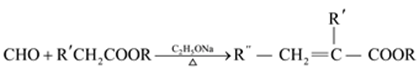
��1����Ӧ�ٵķ�Ӧ��������
��2��C�ķ���ʽ��C4H4O4 �� ��һ�ֶ�Ԫ���ᡣCΪ˳ʽ�ṹ���ṹ��ʽ����
��3����Ӧ�ڵĻ�ѧ����ʽ����
��4��E�ķ���ʽC6H8O4��
i��G����������
ii��H�Ľṹ��ʽ����
��5�����¿��������ͬ�������Ŀ�Ĺ����ŵ�ͬ���칹�����Ŀ����������˳���칹����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�����ڱ������ڵ�һ����,A��B��C����Ԫ�ص�ԭ�Ӻ��������֮�͵���B��������,BԪ�ص�ԭ�Ӻ�������������������������������ȷ���� (����)
![]()
A. A��B��C���Ӱ뾶��С:A>C>B
B. CԪ�ص�������������ǿ�ķǽ�������
C. A��C����̬�⻯�ﱥ��ˮ��Һ��pH:A<C
D. ����������Ӧˮ���������:C>B
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������������˷ܼ�����ϳ�·������ͼ��ʾ��
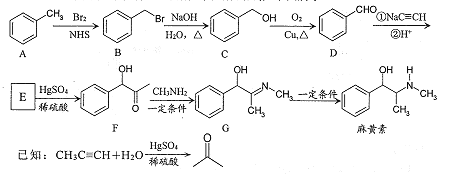
��1��F�еĺ�������������Ϊ ____��_____��
��2��E�Ľṹ��ʽΪ ____��
��3��д��B��C�Ļ�ѧ��Ӧ����ʽ��_______��
��4�� F��G����������Ӧ����Ӧ��������Ϊ_____�� ______��
��5����д��ͬʱ��������������F��һ��ͬ���칹��Ľṹ��ʽ_____��
���ܷ���������Ӧ����ˮ���������FeCl3��ɫ���ۺ˴Ź���������ʾ������塣
��6����д�����Ҵ�Ϊԭ���Ʊ�ǿ��ˮ����֬![]() �ĺϳ�·������ͼ����ѡ�����������Լ������Լ���ѡ���ϳ�·������ͼʾ����������ɣ�___________________��
�ĺϳ�·������ͼ����ѡ�����������Լ������Լ���ѡ���ϳ�·������ͼʾ����������ɣ�___________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ȼ���(CdCl2)��һ�ֳ����ڱ�Ĥ̫���ܵ���ϵ����ʣ��������ж�����ѧ��ѡ������һ��������������������������(����)
A. Cl2 B. HCl C. MgCl2 D. Mg(OH)2
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com