
【题目】结合下表回答下列问题(均为常温下的数据):
酸 | 电离常数(Ka) |
CH3COOH | 1.8×10-5 |
HClO | 3×10-8 |
H2CO3 | K1=4.4×10-7 K2=4.7×10-11 |
H2C2O4 | K1=5.4×10-2 K2=5.4×10-5 |
H2S | K1=1.3×10-7 K2=7.1×10-15 |
请回答下列问题:
(1)同浓度的CH3COO-、HCO3-、CO32-、HC2O4-、ClO-、S2-中结合H+的能力最弱的是____。
(2)常温下0.1 mol/L的CH3COOH溶液在加水稀释过程中,下列表达式的数据一定变小的是________(填字母)。
A.c(H+) B.![]() C.
C.![]() D.c(OH-)
D.c(OH-)
(3)0.1 mol/L的H2C2O4溶液与0.1mol/L的KOH的溶液等体积混合后所得溶液中各离子浓度由大到小的顺序为__________________。
(4)pH相同的NaClO和CH3COOK溶液,其溶液的物质的量浓度的大小关系是CH3COOK________NaClO (填“>”、“<”或“=”)。
(5)向0.1mol/LCH3COOH 溶液中滴加NaOH 溶液至c(CH3COOH)∶c(CH3COO-)=5∶9,此时溶液pH=______________。
(6)向NaClO溶液中通入少量的CO2,所发生的离子方程式为___________。
【答案】HC2O4- AC c(K+)>c(HC2O4-)>c(H+)>c(C2O42-)>c(OH-) > 5 ClO-+H2O+CO2![]() HClO+HCO3-
HClO+HCO3-
【解析】
(1) 酸根离子对应酸的酸的电离平衡常数越大,则其结合氢离子能力越弱;
(2) CH3COOH溶液加水稀释过程,促进电离,c(H+)减小,c(OH-)增大,Kw不变,升温促进电离平衡正向进行,电离程度增大,Kw增大;
(3)反应后溶质为KHC2O4,所得溶液呈酸性,说明HC2O4的电离程度大于其水解程度,又氢离子来自水的电离和草酸氢根离子的电离,则:c(H+)>c(C2O42-)>c(OH-);
(4)酸越弱,酸根离子水解程度就越大;
(5)根据醋酸的电离度表达式![]() ==1.8×10-5,c(CH3COOH):c(CH3COO-)=5:9,求出溶液中氢离子的浓度;
==1.8×10-5,c(CH3COOH):c(CH3COO-)=5:9,求出溶液中氢离子的浓度;
(6)利用弱酸的电离平衡常数书写离子方程式。
(1)平衡常数越大,则其结合氢离子能力越弱,由于电离平衡常数H2C2O4>HC2O4->CH3COOH>H2CO3>H2S>HClO>HCO3->HS-,则同浓度的CH3COO-、HCO3-、CO32-、HC2O4-、ClO-、S2-结合H+的能力由弱到强的顺序为:HC2O4-、CH3COO-、HCO3-、ClO-、CO32-、S2-,结合H+的能力最弱的HC2O4-;
(2) A.CH3COOH溶液加水稀释过程,促进醋酸的电离,c(H+)减小,A正确;
B.![]() ,稀释过程促进醋酸的电离,氢离子的物质的量增大,醋酸的物质的量减小,所以比值变大,B错误;
,稀释过程促进醋酸的电离,氢离子的物质的量增大,醋酸的物质的量减小,所以比值变大,B错误;
C.稀释过程,促进电离,c(H+)减小,c(OH-)增大,c(H+) c(OH-)=Kw,Kw不变,C错误;
D.稀释过程,促进电离,c(H+)减小,c(OH-)增大,D错误;
(3) 0.1mo1/L的H2C2O4溶液与0.1mo1/L的KOH的溶液等体积混合,反应后溶质为KHC2O4,所得溶液呈酸性,说明HC2O4的电离程度大于其水解程度,再结合氢离子来自水的电离和草酸氢根离子的电离,则c(H+)>c(C2O42-)>c(OH-),溶液中离子浓度大小为:c(K+)>c(HC2O4-)>c(H+)>c(C2O42-)>c(OH-);
(4)弱酸的酸性越弱,相应的酸根离子水解程度就越大。由于酸性CH3COOH>HClO,所以当盐的浓度相等时,溶液的碱性NaClO>CH3COOK,即pH:NaClO>CH3COOK;若溶液的pH相同,则盐的浓度CH3COOK >NaClO;
(5) 根据醋酸的电离度表达式![]() =1.8×10-5,c(CH3COOH):c(CH3COO-)=5:9,则溶液中c(H+)=1.8×10-5×
=1.8×10-5,c(CH3COOH):c(CH3COO-)=5:9,则溶液中c(H+)=1.8×10-5×![]() =1.8×10-5×
=1.8×10-5×![]() =1×10-5mol/L,所以溶液的pH=5;
=1×10-5mol/L,所以溶液的pH=5;
(6)由于酸性:H2CO3> HClO>HCO3-,所以向NaClO溶液中通入少量的CO2,所发生的离子方程式为 ClO-+H2O+CO2![]() HClO+HCO3-。
HClO+HCO3-。


科目:高中化学 来源: 题型:
【题目】在2L的密闭容器中放入4molN2O5,发生如下反应:2N2O5(g)![]() 4NO2(g)+ O2(g)。反应5min后,测得N2O5转化了20%,求:
4NO2(g)+ O2(g)。反应5min后,测得N2O5转化了20%,求:
(1)υ(NO2)、υ(O2)分别为多少?
(2)5min时,N2O5占混合气体总体积的百分比是多少?
(要求写出计算过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用密度为1.84g·mLˉ1、质量分数为98%的浓硫酸配制100mL3mol·Lˉ1稀硫酸。下列各步骤中操作正确的是( )
A.计算、量取:用10mL量筒量取16.3mL浓硫酸
B.溶解、稀释:将浓硫酸倒入烧杯,再倒入30mL左右的蒸馏水,搅拌,静置
C.转移、洗涤:待溶液冷却后,将溶液转移到容量瓶中,用蒸馏水洗涤烧杯和玻璃棒,洗涤液转入容量瓶,重复2~3次
D.定容、摇匀:加水至凹液面最低处与刻度线相切,摇匀,在容量瓶上贴上标签,注明溶液成分及浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从某化工厂提供的硒酸泥(主要含S、Se、Fe2O3及SiO2)中提取粗硒的工艺流程如下图所示:

备注:氧化浸出液中Se的含量为43.45g/L
根据以上信息回答下列问题:
(1)把煤油加热后再进行浸泡的目的是:__________________________。
(2)将含硫的滤液进行“冷却、结晶、过滤”操作可以除去煤油中的硫,由这一操作可推测硫的物理性质是:__________________________。
(3)“氧化浸硒”过程中:
①需要控制H2SO4的浓度至少为3mol/L,理由是:__________________________。
②硒转化为H2SeO3并生成一种黄绿色的气体,此过程的化学方程式为_______________。
(4)要将1L氧化浸出液中的硒元素全部还原,需要至少加入Na2SO3_____mol;
(5)滤渣A的主要成分有___________;滤液B的金属阳离子有___________;
(6)处理硒酸泥的另一种方法是往硒酸泥中加入等体积的浓硫酸进行焙烧,本工艺流程与此方法相比主要的优点是(写两点):__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,向某VL的密闭容器中充入3molH2(g)和3molI2(g),发生反应:H2(g)+I2(g)![]() 2HI(g) △H=-26.5kJmol-1,测得各物质的物质的量浓度与时间变化的关系如图所示。请回答下列问题:
2HI(g) △H=-26.5kJmol-1,测得各物质的物质的量浓度与时间变化的关系如图所示。请回答下列问题:

(1)0-5秒内平均反应速率v(HI)=___mol/(Ls)。
(2)该反应达到平衡状态时,放出的热量为___kJ。
(3)判断该反应达到平衡的依据是___(填序号)。
①H2消耗的速率和I2消耗的速率相等
②H2、I2、HI的浓度比为1:1:2
③H2、I2、HI的浓度都不再发生变化
④该条件下正、逆反应速率都为零
⑤混合气体的平均分子量不再发生变化
⑥气体的颜色不再发生变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是
A. 已知HI(g) ![]() 1/2H2(g)+1/2I2(s) ΔH=-26.5 kJ·mol-1,由此可知1 mol HI气体在密闭容器中充分分解后可以放出26.5 kJ的热量
1/2H2(g)+1/2I2(s) ΔH=-26.5 kJ·mol-1,由此可知1 mol HI气体在密闭容器中充分分解后可以放出26.5 kJ的热量
B. 已知2H2(g)+O2(g)===2H2O(g) ΔH=-571.6 kJ·mol-1,则氢气的燃烧热为ΔH=-285.8 kJ·mol-1
C. 已知2C(s)+2O2(g)=2CO2(g) ΔH1, 2C(s)+O2(g)=2CO(g) ΔH2,则ΔH1<ΔH2
D. 含20.0 g NaOH的稀溶液与稀盐酸完全中和,放出28.7 kJ的热量,则稀醋酸和稀NaOH溶液反应的热化学方程式为:NaOH(aq)+CH3COOH(aq)===CH3COONa(aq)+H2O(l) ΔH=-57.4 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学在学习元素化合物知识的过程中,发现含有相同元素的物质间在一定条件下存在转化规律,绘制出如下转化关系图(部分反应物或产物略去),并用于研究物质A、B、C、D的性质及其变化。
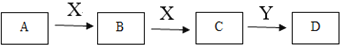
(1)若A是黄绿色气体,X是生活中应用最大量的金属,D是白色固体。
① 组成A的元素在周期表中的位置是______。
② 下列说法正确的是______(填字母)。
a.B的水溶液中加入KSCN溶液,变为红色
b.C只具有还原性
c.若Y是碱,D放置在空气中会迅速变为灰绿色,最终变为红褐色
(2)若A、B、C、D的焰色反应均为黄色,X的固体俗称干冰。
① B转化为C的离子方程式是______。
② A用于呼吸面具或潜水艇中氧气的来源,则A和X反应生成1 mol B时,转移电子数为______。
③ C与Y反应生成X的离子方程式_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱性锌锰电池的工作原理:Zn+2MnO2+2H2O![]() 2MnO(OH)+Zn(OH)2,其中的电解质溶液是KOH溶液。某课题组用废旧铁壳无汞碱性锌锰电池为原料,制备一种新型材料——MnxZn(1x)Fe2O4,其工艺流程如图所示:
2MnO(OH)+Zn(OH)2,其中的电解质溶液是KOH溶液。某课题组用废旧铁壳无汞碱性锌锰电池为原料,制备一种新型材料——MnxZn(1x)Fe2O4,其工艺流程如图所示:

(1)已知MnxZn(1x)Fe2O4中锰元素的化合价与实验室用二氧化锰制取氯气时还原产物中的锰相同,则铁元素的化合价为___________。
(2)“溶渣”工序中稀硫酸与铁反应生成的硫酸亚铁可将+3价锰的化合物全部还原成Mn2+,写出该反应的离子方程式:_________________________________。
(3)“调铁”工序的目的是调整滤液中铁离子的总浓度,使其中金属元素的物质的量之比与产品的化学式MnxZn(1x)Fe2O4相符合。
①写出“调铁”工序中发生反应的离子方程式:______________________、_______。
②若测得滤液的成分为c(Mn2+)+c(Zn2+)=a mol·L1,c(Fe2+)+c(Fe3+)=b mol·L1,滤液体积为1 m3,“调铁”工序中,需加入的铁粉质量为___________kg(忽略溶液体积变化,用含a、b的代数式表示)。
(4)在“氧化”工序中,加入双氧水的目的是把 Fe 2+ 氧化为 Fe 3+;生产过程中发现实际消耗双氧水的量大于理论值,其可能原因除温度外,主要是______________________。
(5)用氨水“调pH”后,经“结晶”、“过滤”可得到产品和滤液C,从滤液C中还可分离出一种氮肥,该氮肥的溶液中离子浓度由大到小的排序为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是研究二氧化硫性质的微型实验装置.现用60%硫酸溶液和亚硫酸钠晶体反应制取SO2气体,实验现象很明显,且不易污染空气.下列说法中错误的是( )

A. 紫色石蕊溶液先变红后褪色B. 品红溶液褪色
C. 溴水橙色褪去D. 含酚酞的NaOH溶液红色变浅
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com