
【题目】镁是一种银白色的碱土金属,镁元素在地壳中的含量约为2.00%,位居第八位,镁及其化合物在研究和生产中具有广泛用途。请回答下列问题:
(1)在室温下,纯净的氮化镁(Mg3N2)为黄绿色的粉末,能与水反应,常用作触媒,实验室用如图1所示装置和药品制备少量氮化镁。
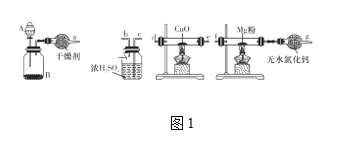
①A中盛装的是____,B中可盛装碱石灰,二者混合可制取氨气。
②按照气流的方向从左至右连接装置:a接____、____接____、_b__接____。
③气体通过CuO这一装置的目的是什么?用化学方程式回答:______。
④无水氯化钙装置可防止外界空气中的水进入,以防_____________(化学方程式表示)的发生。
(2)碳酸镁可用作耐火材料、锅炉和管道的保温材料,以及食品、药品、化妆品、橡胶、墨水等的添加剂。
Ⅰ.合成碳酸镁晶体的步骤如下:
步骤1:配制0.5 mol·L-1MgSO4溶液和0.5 mol·L-1NH4HCO3溶液。
步骤2:用量筒量取500 mL NH4HCO3溶液于1 000 mL四口烧瓶中,开启搅拌器,温度控制在50 ℃。
步骤3:将250 mL MgSO4溶液逐滴加入NH4HCO3溶液中,1 min内滴加完毕,然后用氨水调节溶液pH到9.5。
步骤4:放置1 h后,过滤,洗涤。
步骤5:在40 ℃的真空干燥箱中干燥10 h,得到产品碳酸镁晶体(MgCO3·nH2O,n=1~5)。
①配制0.5 mol·L-1MgSO4溶液500 mL,需要的仪器有托盘天平、药匙、烧杯、玻璃棒、量筒、胶头滴管、____。
②步骤3中加氨水后发生反应的离子方程式为________________
Ⅱ.测定合成的MgCO3·nH2O中的n值。
称量1.000 g碳酸镁晶体,放入图2所示的广口瓶中,加入适量水,滴入稀硫酸与晶体反应,生成的CO2被NaOH溶液吸收,在室温下反应4~5 h,后期将温度升到30 ℃,最后烧杯中的溶液用已知浓度的盐酸滴定,测得生成CO2的总量;重复上述操作2次。

③上述反应后期要升温到30 ℃,主要目的是_____________________
④若实验测得1.000 g碳酸镁晶体产生CO2的平均物质的量为a mol,则n为__________(用含a的表达式表示)。
⑤若称取100 g上述晶体进行热重分析,得到的热重曲线如图3所示,则合成的晶体中n=____(取整数)。
【答案】浓氨水 d e c b f 2NH3+3CuO![]() N2+3H2O+3Cu Mg3N2+6H2O===3Mg(OH)2+2NH3↑ 500mL容量瓶 Mg2++HCO3-+NH3·H2O+(n-1)H2O
N2+3H2O+3Cu Mg3N2+6H2O===3Mg(OH)2+2NH3↑ 500mL容量瓶 Mg2++HCO3-+NH3·H2O+(n-1)H2O![]() MgCO3·nH2O↓+NH4+。 升高温度,气体的溶解度减小,使溶解在水中的CO2逸出,便于吸收完全 1-84a/18a 1
MgCO3·nH2O↓+NH4+。 升高温度,气体的溶解度减小,使溶解在水中的CO2逸出,便于吸收完全 1-84a/18a 1
【解析】
根据题意可知,本题考查了物质含量的实验探究过程分析、实验装置的连接,运用各物质的化学性质和装置连接步骤分析。
(1)①A、B二者混合可制取氨气,而浓氨水和生石灰或氢氧化钠固体混合放热,可使一水合氨分解生成氨气。因此A中盛装的是浓氨水;
故答案为:浓氨水;
②根据实验目的及题给装置可知,按照气流的方向从左向右连接装置的顺序为:a接d,e接c,b接f;
故答案为:d; e ; c ;b ;f;
③气体通过CuO这一装置的目的是氨气有还原性,能还原氧化铜,生成氮气,则气体通过CuO这一装置的目的用化学方程式表示为:2NH3+3CuO![]() N2+3H2O+3Cu;
N2+3H2O+3Cu;
故答案为:2NH3+3CuO![]() N2+3H2O+3Cu;
N2+3H2O+3Cu;
④无水氯化钙装置可防止外界空气中的水进入,以防氮化镁和水发生反应生成氢氧化镁和氨气,化学方程式为:Mg3N2+6H2O![]() 3Mg(OH)2+2NH3↑;
3Mg(OH)2+2NH3↑;
故答案为:Mg3N2+6H2O![]() 3Mg(OH)2+2NH3↑;
3Mg(OH)2+2NH3↑;
(2)①配制0.5 mol·L-1MgSO4溶液500 mL,除提供的仪器外,还需要的仪器为500 mL容量瓶;
故答案为:500 mL容量瓶;
②步骤3中加氨水后反应生成碳酸镁结晶水合物,反应的离子方程式为Mg2++HCO3-+NH3·H2O+(n-1)H2O![]() MgCO3·nH2O↓+NH4+;
MgCO3·nH2O↓+NH4+;
故答案为:Mg2++HCO3-+NH3·H2O+(n-1)H2O![]() MgCO3·nH2O↓+NH4+;
MgCO3·nH2O↓+NH4+;
③题述反应后期将温度升到30 ℃,是为了使生成的二氧化碳全部逸出,便于其被氢氧化钠溶液完全吸收,从而减小测定产生的误差;
故答案为:升高温度,气体的溶解度减小,使溶解在水中的CO2逸出,便于吸收完全;
④若实验测得1.000 g碳酸镁晶须产生的CO2的平均物质的量为amol,依据碳元素守恒可知,晶须中碳酸镁的物质的量为amol,根据MgCO3·nH2O中碳酸镁和结晶水的物质的量之比为1∶n,得到![]() ,得到
,得到![]() ;
;
故答案为:![]()
⑤由题图3知400 ℃时剩余质量为82.3 g,这是该晶须失去结晶水后的质量,则有![]() ,解得n=1;
,解得n=1;
故答案为:1。


科目:高中化学 来源: 题型:
【题目】![]() 是一种有机烯醚 ,可以烃用 A 通过下列路线制得:
是一种有机烯醚 ,可以烃用 A 通过下列路线制得:
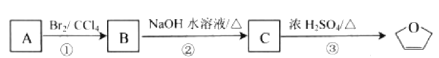
则下列说法正确的是
A.![]() 分子式为C4H4O
分子式为C4H4O
B.A的结构简式是CH2=CHCH2CH3
C.![]() 分子中所有原子可能共面
分子中所有原子可能共面
D.①②③的反应类型分别为加成、水解、取代
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA表示阿伏加德罗常数的值。下列说法中正确的有几项:
①lmolCl2做氧化剂时得到的电子效为2NA
②25℃时,1LpH=12的碳酸钠溶液中含有Na+的数目为0.02NA
③过氧化钠与水反应时,生成0.5molO2转移的电子数为2NA
④50mL18.4mol/L的浓硫酸与足量的铜微热后反应,生成SO2分子数小于0.46NA
⑤利用氰尿酸与次氯酸在一定pH下反应可制备三氯异氰尿酸(结构如图)。若原料完全反应,得到1mol产物同时生成3NA个H2O

A. 0 B. 1 C. 2 D. 3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B是中学化学常见的化合物,它们各由两种元素组成;乙为元素R组成的单质,它们之间存在如图所示关系.根据要求回答问题:

![]() 如图三个反应中,属于氧化还原反应的有______个.
如图三个反应中,属于氧化还原反应的有______个.
![]() 若元素R与氧同主族,下列事实能说明R与氧的非金属性相对强弱的有______.
若元素R与氧同主族,下列事实能说明R与氧的非金属性相对强弱的有______.
A.还原性:![]() B.酸性:
B.酸性:![]()
C.稳定性:![]() C.沸点:
C.沸点:![]()
![]() 若化合物B常温下为气体,其水溶液呈碱性
若化合物B常温下为气体,其水溶液呈碱性![]() 答题必须用具体物质表示
答题必须用具体物质表示![]() .
.
![]() 化合物B的电子式为______;其水溶液呈碱性的原因是______
化合物B的电子式为______;其水溶液呈碱性的原因是______![]() 用离子方程式表示
用离子方程式表示![]() .
.
![]() 化合物B可与
化合物B可与![]() 组成燃料电池
组成燃料电池![]() 氢氧化钾溶液为电解质溶液
氢氧化钾溶液为电解质溶液![]() ,其反应产物与反应Ⅲ相同.写出该电池负极的电极反应式______.
,其反应产物与反应Ⅲ相同.写出该电池负极的电极反应式______.
![]() 当1mol的化合物B分别参与反应Ⅱ、Ⅲ时,热效应为
当1mol的化合物B分别参与反应Ⅱ、Ⅲ时,热效应为![]() 和
和![]() ,则反应Ⅰ的热化学方程式为______
,则反应Ⅰ的热化学方程式为______![]() 注:反应条件相同、所有物质均为气体
注:反应条件相同、所有物质均为气体![]() .
.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电镀行业产生的酸性含铬废水对环境有污染,其中所含的Cr(Ⅵ)是主要污染物,可采用多种处理方法将其除去。查阅资料可知:
①在酸性环境下,Cr(Ⅵ)通常以Cr2O72-的形式存在;
②Cr2O72-的氧化能力强于CrO42-;
③常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下表所示:
阳离子 | Fe3+ | Fe2+ | Cr3+ |
开始沉淀的pH | 1.9 | 7.0 | 4.3 |
沉淀完全的pH | 3.2 | 9.0 | 5.6 |
Ⅰ.腐蚀电池法
(1)向酸性含铬废水中投放废铁屑和焦炭,利用原电池原理还原Cr(Ⅵ)。下列关于焦炭的说法正确的是_______(填字母代号)。
a.作原电池的正极 b.在反应中作还原剂 c.表面可能有气泡产生
Ⅱ.电解还原法
向酸性含铬废水中加入适量NaCl固体,以Fe为电极电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成排出,从而使废水中铬含量低于排放标准。电解装置如图1所示。
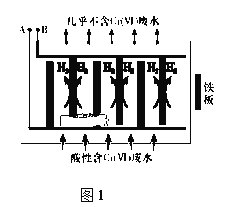
(2)A极连接电源的______________极,A极上发生的电极反应式为_______________
(3)电解开始时,B极上除了发生产生H2的反应外,还有少量Cr2O72-在B极上直接放电,该反应的电极反应式为_________________
(4)电解过程中,溶液的pH不同时,通电时间(t)与溶液中铬元素去除率的关系如图2所示。
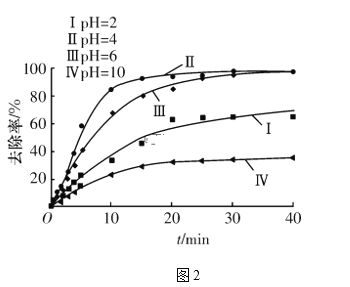
①由图可知,电解还原法应采取的最佳pH范围为____(填字母代号)。
a.2~4 b.4~6 c.6~10
②解释曲线Ⅰ和曲线Ⅳ去除率低的原因:________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用如图所示装置测定中和热的实验步骤如下:
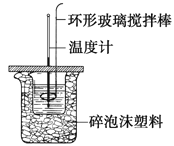
步骤一:用量筒量取50ml 0.50 molL-1盐酸倒入小烧杯中,测出盐酸温度t1;
步骤二:用另一量筒量取50ml 0.55 molL-1NaOH溶液,并用另一温度计测出其温度t2;
步骤三:将NaOH溶液倒入小烧杯中,设法使之混合均匀,测得混合液最高温度t3。
回答下列问题:
(1)步骤三中倒入NaOH溶液的正确操作是__________。
A.沿玻璃棒缓慢倒入 B.分三次少量倒入 C.一次迅速倒入
(2)使盐酸与NaOH溶液混合均匀的正确操作是________(填序号)。
A.轻轻地振荡烧杯 B.揭开硬纸片用玻璃棒搅拌
C.用温度计小心搅拌 D.用套在温度计上的环形玻璃搅拌棒轻轻地搅动
(3)___________(填“能”或“不能”)用Ba(OH)2溶液和硫酸代替NaOH溶液和盐酸测中和热,理由是________________________________________。
(4)在反应中若因为有放热现象,而造成少量HCl在反应中挥发,则测得的中和热_______(填“偏大”、“偏小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两种常见的非金属元素A与B,与常见的三种金属元素C、D、E,A的一种单质是自然界硬度最大的物质,B与C的单质在加热条件下反应生成淡黄色化合物X,D的单质既能与盐酸,也能与NaOH溶液反应生成![]() ,E的单质在B的单质中燃烧火星四溅,生成一种黑色固体Y。请回答下列问题:
,E的单质在B的单质中燃烧火星四溅,生成一种黑色固体Y。请回答下列问题:
![]() 物质X的名称______。
物质X的名称______。
![]() 将D的单质用砂纸打磨,然后灼烧,液态的D并不滴落的原因______。
将D的单质用砂纸打磨,然后灼烧,液态的D并不滴落的原因______。
![]() 写出E的单质与水蒸气反应的化学方程式______。
写出E的单质与水蒸气反应的化学方程式______。
![]() gC的单质投入足量
gC的单质投入足量![]() 溶液中,下列实验现象正确的有______。
溶液中,下列实验现象正确的有______。
A.钠沉在溶液底部
B.熔化成银色光亮的小球
C.小球四处游动发出”嘶嘶”的声音
D.生成红色固体物质
![]() 第
第![]() 中可能的离子方程式为______。将所得沉淀过滤、洗涤、干燥,可得到______g固体。
中可能的离子方程式为______。将所得沉淀过滤、洗涤、干燥,可得到______g固体。
![]() 在少量
在少量![]() 中燃烧,所得混合气体在标况下的平均摩尔质量为
中燃烧,所得混合气体在标况下的平均摩尔质量为![]() ,则A与
,则A与![]() 的物质的量之比为______。
的物质的量之比为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镍及其化合物用途广泛。某矿渣的主要成分是NiFe2O4(铁酸镍)、NiO、FeO、CaO、SiO2等,如下图是从该矿渣中回收NiSO4的工艺路线:
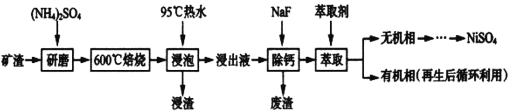
已知:(NH4)2SO4在350℃以上会分解生成NH3和H2SO4,NiFe2O4在焙烧过程中生成NiSO4、Fe2(SO4)3。锡(Sn)位于第五周期第IVA族。
(1)焙烧前将矿渣与(NH4)2SO4混合研磨,混合研磨的目的是_______________。
(2)“浸泡”过程中Fe2(SO4)3生成FeO(OH)的离子方程式为_________________________,“浸渣”的成分除Fe2O3、FeO(OH)外还含有___________________(填化学式)。
(3)为保证产品纯度,要检测“浸出液”的总铁量:取一定体积的浸出液,用盐酸酸化后,加入SnCl2将:Fe3+还原为Fe2+,所需SnC12的物质的量不少于Fe3+物质的量的_____倍:除去过量的SnCl2后,再用酸性K2Cr2O7标准溶液滴定溶液中的Fe2+,还原产物为Cr3+,滴定时反应的离子方程式为_________________________________________。
(4)“浸出液”中c(Ca2+)=1.0×10-3mol·L-1,当除钙率达到99%时,溶液中c(F-)=___mol· L-1。[已知KSP(CaF2)=4.0×10-11]
(5)已知正十二烷可用作该工艺的萃取剂。用电化学制备正十二烷的方法为:向烧杯中加入50mL甲醇,不断搅拌加入少量金属钠,再加入11mL正庚酸搅拌均匀,装好铂电极,接通电源反应,当电流明显减小时切断电源,然后提纯正十二烷。已知电解总反应为:2C6H13COONa+2CH3OH![]() C12H26+2CO2↑+H2↑+2CH3ONa,则阳极的电极反应式为______________________________________
C12H26+2CO2↑+H2↑+2CH3ONa,则阳极的电极反应式为______________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将28.8g铜与150mL一定浓度的硝酸反应,铜完全溶解,产生的NO和NO2混合气体在标准状况下的体积为11.2L。请回答:
(1)NO的体积为___L,NO2的体积为___L;
(2)待产生的气体全部释放,向溶液中加入200mL5mol·L-1的NaOH溶液,恰好使溶液中的Cu2+全部转化成沉淀,则原硝酸溶液的浓度为___mol·L-1。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com