
下列数据是对应物质的熔点据此做出的下列判断中错误的是
Na2O | NaCl | AlF3 | AlCl3 |
920 | 801 | 1291 | 190 |
BCl3 | Al2O3 | CO2 | SiO2 |
-107 | 2073 | -57 | 1723 |
A.铝的化合物的晶体中有的是离子晶体
B.表中只有BCl3和干冰是分子晶体
C.同族元素的氧化物可形成不同类型的晶体
D.不同族元素的氧化物可形成相同类型的晶体
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2013-2014福建省南平市毕业班质量检查理综化学试卷(解析版) 题型:推断题
(15分)实验室利用硫酸厂烧渣(主要成分为铁的氧化物及少量FeS、SiO2等)制备聚铁(碱式硫酸铁的聚合物)和绿矾(FeSO4·7H2O),过程如下:
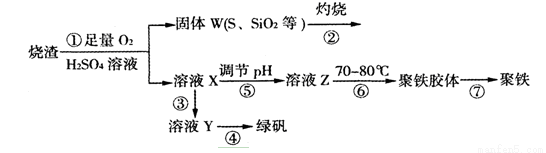
(1)将过程②中的产生的气体通入下列溶液中,溶液会褪色的是 ;
A.品红溶液 B.紫色石蕊溶液 C.酸性KMnO4溶液 D.溴水
(2)过程①中,FeS和O2、H2SO4反应的离子方程式为: ;
(3)过程③中,需加入的物质是 ;
(4)过程④中,蒸发结晶需要使用酒精灯、三角架、泥三角,还需要的仪器有 ;
(5)过程⑤调节pH可选用下列试剂中的 (填选项序号);
A.稀硫酸 B.CaCO3 C.NaOH溶液
(6)过程⑥中,将溶液Z加热到70一80℃,目的是 ;
(7)实验室为测量所得到的聚铁样品中铁元素的质量分数,进行下列实验。①用分析天平称取2.700g样品;②将样品溶于足量的盐酸后,加入过量的氯化钡溶液;③过滤、洗涤、干燥,称量,得固体质量为3.495g。若该聚铁主要成分为[(Fe(OH)(SO4)]n,则该聚铁样品中铁元素的质量分数为 。(假设杂质中不含铁元素和硫元素)。
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省高一下学期期末考试化学试卷(解析版) 题型:选择题
下列说法不正确的是( )
A.粘有油脂的试管可以用热的纯碱溶液洗涤
B.石油的分馏、裂化、裂解都是化学变化
C.食醋中含有乙酸,乙酸可由乙醇氧化得到
D.煤可与水蒸气反应制成水煤气,水煤气的主要成分为CO和H2
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省高一下学期期末考试化学试卷(解析版) 题型:选择题
下列判断错误的是( )
A.熔点:SiO2>NaCl>SiCl4 B.稳定性:AsH3 >PH3> NH3
C.酸性:HClO4>H2SO4>H3PO4 D.碱性:NaOH>Mg(OH)2>Al(OH)3
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省三明市三校高三下学期联考理综化学试卷(解析版) 题型:简答题
(12分)D、A、B、C为四种原子序数依次增大的短周期元素,A、B、C同周期,A的原子半径是同周期中最大的;B、D同主族。已知D元素的一种单质是日常生活中饮水机常用的消毒剂,C元素的单质可以从A、B两元素组成的化合物的水溶液中置换出B元素的单质。
(1)C元素在周期表中的位置 周期 族。
(2)A、B元素形成的常见化合物水溶液显 性,原因是(用离子方程式表示) 用石墨做电极电解该化合物的水溶液,则阴极反应式为 ,
(3)A、D元素可以形成化合物A2D2,写出A2D2与CO2反应的化学方程式 (用元素符号表示)。该反应中还原剂是 。
(4)B元素的单质在不同的条件下可以与O2发生一系列反应:① B(s)+O2(g)=BO2(g);△H=-296.8kJ/mol②2BO2(g)+O2(g)  2BO3(g);△H=-196.6kJ/mol
2BO3(g);△H=-196.6kJ/mol
则1 mol BO3(g)若完全分解成B(s),反应过程中的热效应为 。
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省“四地六校”下学期第三次联考高二化学试卷(解析版) 题型:填空题
(13分)C和Si分别是构成生命体和岩石的重要元素。
(1)CH4和SiH4沸点较高的是 。原因是 。稳定性较高的是 。
(2)SiC的晶体结构与晶体硅相似,其中C原子的杂化方式为 。微粒间存在的作用力是 。
(3)CO2形成的干冰晶体与SiO2晶体相比,下列说法不正确的有 。
A中心原子的杂化方式不同 B构成晶体的微粒种类不同 C晶体内微粒间作用力不同
D晶体导电性不同 E.常温时,晶体挥发性不同
(4)已知键能数据如下,化学反应的ΔH等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。写出Si(s)在O2中燃烧生成SiO2(s)的热化学方程式 。
化学键 | Si—O | O=O | Si—Si |
键能(kJ·mol-1) | 460 | 498 | 226 |
(5)氨基酸是构成蛋白质的物质基础,甘氨酸H2N-CH2-COOH中,各元素的电负性从大到小为 。
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省“四地六校”下学期第三次联考高二化学试卷(解析版) 题型:选择题
已知:X、Y、Z、W为短周期元素,原子半径X:99pm Y:154pm Z:125pm W:117pm ,X、Y、W位置如图所示(副族省略),X、Y、Z的最高价氧化物对应的水化物相互能反应,
下列说法正确的是( )
|
|
|
| X |
Y |
|
| W |
|
A.元素Z处于周期表的阴影位置
B.X与W形成的化合物熔点很高,为离子化合物
C.X、W的最高价氧化物对应水化物的酸性: X>W
D.Y、W的最高价氧化物的晶体类型相同
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省“四地六校”下学期第三次联考高一化学试卷(解析版) 题型:选择题
某原电池总反应为2Fe3++Fe=3Fe2+,不能实现该反应的原电池是( )
A.正极为Cu,负极为Fe,电解质溶液为FeCl3
B.正极为C,负极为Fe,电解质溶液为Fe(NO)3
C.正极为Fe,负极为Zn,电解质溶液为Fe2(SO4)3
D.正极为Ag,负极为Fe,电解质溶液为Fe2(SO4)3
查看答案和解析>>
科目:高中化学 来源:2013-2014甘肃省高二下学期期末考试化学试卷(解析版) 题型:填空题
卤代烃是一类重要的有机合成中间体,是许多有机合成的原料。根据卤代烃的相关性质,回答下列问题
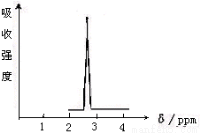
(1)化合物A和B的分子式都是C2H4Br2,A的核磁共振氢谱图如图所示,则A的结构简式为 ,请预测B的核磁共振氢谱上应该有 个峰(信号)。
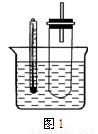
(2)某同学用如图1装置(铁架台、酒精灯等略)验证取代反应和消去反应的产物。
实验操作Ⅰ:在试管中加入5 mL 1 mol/L NaOH溶液和0.5 mL溴乙烷振荡。
实验操作Ⅱ:将试管如图1固定后,水浴加热。
①据图1:用水浴加热而不直接用酒精灯加热的原因是 。
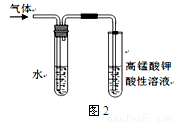
②图2是为证明溴乙烷在NaOH乙醇溶液中发生的是消去
反应,实验中需要检验的产物是 ,
水的作用是 ,
实验现象是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com