
(12分)D、A、B、C为四种原子序数依次增大的短周期元素,A、B、C同周期,A的原子半径是同周期中最大的;B、D同主族。已知D元素的一种单质是日常生活中饮水机常用的消毒剂,C元素的单质可以从A、B两元素组成的化合物的水溶液中置换出B元素的单质。
(1)C元素在周期表中的位置 周期 族。
(2)A、B元素形成的常见化合物水溶液显 性,原因是(用离子方程式表示) 用石墨做电极电解该化合物的水溶液,则阴极反应式为 ,
(3)A、D元素可以形成化合物A2D2,写出A2D2与CO2反应的化学方程式 (用元素符号表示)。该反应中还原剂是 。
(4)B元素的单质在不同的条件下可以与O2发生一系列反应:① B(s)+O2(g)=BO2(g);△H=-296.8kJ/mol②2BO2(g)+O2(g)  2BO3(g);△H=-196.6kJ/mol
2BO3(g);△H=-196.6kJ/mol
则1 mol BO3(g)若完全分解成B(s),反应过程中的热效应为 。
(1)第三周期第ⅦA族; (2)碱性;S2-+H2O HS-+OH-;2H++2e-=H2↑;
HS-+OH-;2H++2e-=H2↑;
(3) 2Na2O2+2CO2 =Na2CO3+ O2 ; Na2O2; (4)吸收395.1KJ的热量(或+395.1KJ)
【解析】
试题分析:根据题意可知这几种元素分别是:A是Na;B是S;C是Cl;D是O。(1)Cl元素在周期表中的位置是位于第三周期第ⅦA族;(2)A、B元素形成的常见化合物Na2S是强碱弱酸盐,弱酸根离子水解使水溶液显碱性。水解的两种方程式为:S2-+H2O HS-+OH-;用石墨做电极电解该化合物的水溶液,由于放电能力H+>Na+,所以在阴极是H+得到电子。该电极的反应式为2H++2e-=H2↑; (3)Na2O2与CO2反应的化学方程式是2Na2O2+2CO2 =Na2CO3+ O2 ;在该反应中氧化剂、还原剂都是Na2O2。①×2+②足量可得BO3(g)=3/2 O2(g)+ B(s) ΔH=+395.1KJ/mol.
HS-+OH-;用石墨做电极电解该化合物的水溶液,由于放电能力H+>Na+,所以在阴极是H+得到电子。该电极的反应式为2H++2e-=H2↑; (3)Na2O2与CO2反应的化学方程式是2Na2O2+2CO2 =Na2CO3+ O2 ;在该反应中氧化剂、还原剂都是Na2O2。①×2+②足量可得BO3(g)=3/2 O2(g)+ B(s) ΔH=+395.1KJ/mol.
考点:考查元素的推断、盐的水解、电解原理的应用、还原剂的判断、热化学方程式的书写的知识。


科目:高中化学 来源:2013-2014福建省高三热身考试化学试卷(解析版) 题型:选择题
化学与生产和生活密切相关,下列说法正确的是
A.金属钠可以保存在煤油或酒精中,防止在空气中变质
B.石油的裂化和煤的干馏,都属于化学变化
C.等物质的量的乙烯和乙醇完全燃烧时所需氧气的质量相等
D.聚氯乙烯制品易造成白色污染,可采用焚烧法处理
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省高一下学期期末考试化学试卷(解析版) 题型:推断题
A是一种重要的化工原料,A的产量可以用来衡量一个国家的石油化工水平,D是具有果香气味的烃的衍生物。A、B、C、D在一定条件下存在如下转化关系(部分反应条件、产物被省略)。
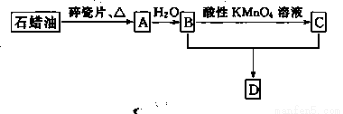
(1)工业上,由石油获得石蜡油的方法是_____ _,由石蜡油获得A是___ __变化(“物理”或“化学”)。
(2)写出反应B+C→ D的化学方程式: _____________________________ __。
(3)丁烷是由石蜡油获得A的过程中的中间产物之一,写出它的两种同分异构体的结构简式:
。
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省高一下学期期末考试化学试卷(解析版) 题型:选择题
下图是部分短周期元素化合价与原子序数的关系图,下列说法正确的是( )
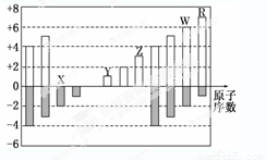
A.原子半径:Z>Y>X
B.气态氢化物的稳定性:W>R
C.WX3和水反应形成的化合物是离子化合物[来*源#^@:中国教育出版~网]
D.Y和Z两者最高价氧化物对应的水化物能相互反应
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省高一下学期期末考试化学试卷(解析版) 题型:选择题
下列叙述错误的是( )
A.13C和14C属于同一种元素,它们互为同位素
B.1H和2H是不同的核素,它们的质子数相等
C.14C和14N的质量数相等,它们的中子数不等
D.6Li和7Li的电子数相等,中子数也相等
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省三明市三校高三下学期联考理综化学试卷(解析版) 题型:选择题
下列数据是对应物质的熔点据此做出的下列判断中错误的是
Na2O | NaCl | AlF3 | AlCl3 |
920 | 801 | 1291 | 190 |
BCl3 | Al2O3 | CO2 | SiO2 |
-107 | 2073 | -57 | 1723 |
A.铝的化合物的晶体中有的是离子晶体
B.表中只有BCl3和干冰是分子晶体
C.同族元素的氧化物可形成不同类型的晶体
D.不同族元素的氧化物可形成相同类型的晶体
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省“四地六校”下学期第三次联考高二化学试卷(解析版) 题型:选择题
常温下,向20.00 mL 0.100 mol·L-1CH3COONa溶液中逐滴加入0.100 mol·L-1盐酸,溶液的pH与所加入盐酸体积的关系如图所示(不考虑挥发)。下列说法正确的是
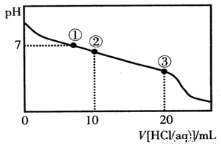
A.点①所示溶液中:c(Na+)=c(Cl-)>c(H+)=c(OH-)
B.点②所示溶液中:c(Na+)>c(Cl-)>c(CH3COO-)>c(CH3COOH)
C.点③所示溶液中:c(Na+)>c(CH3COOH)>c(H+)>c(CH3COO-)
D.整个过程中可能出现:c(H+)+c(Na+)=c(CH3COO-)+c(CH3COOH)
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省“四地六校”下学期第三次联考高一化学试卷(解析版) 题型:推断题
A、B、C、D均是短周期元素,A和B同周期, B和C同族,A元素族序数是周期数的三倍,B原子最外层电子数是内层电子数的二倍,B与A能生成化合物BA2,C与A生成化合物CA2, A的阴离子与D的阳离子电子层结构相同,都与氖原子的电子层结构相同,D 的单质与A 的单质在不同条件下反应,可生成D2A或D2A2。请回答
(1)写出元素符号A: ,B: ,C: 。
(2)D2A的电子式 ,BA2的结构式 。
(3)D2A2的化学式 ,灼烧这化合物火焰呈 色。
(4)C在元素周期表中的位置是 ,其原子结构示意图为 。
(5)比较A、B气态氢化物的沸点 ;原因 。
查看答案和解析>>
科目:高中化学 来源:2013-2014福建安溪一中、惠安一中、养正中学下学期期中高二化学(解析版) 题型:选择题
下列叙述中,可以说明金属甲的活动性比金属乙的活动性强的是( )
A.在氧化还原反应中,甲原子失去的电子比乙原子失去的电子多
B.同价态的阳离子,甲比乙的氧化性强
C.甲能跟稀盐酸反应放出氢气而乙不能
D.将甲、乙作电极组成原电池时,甲是正极
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com