
【题目】某课外活动小组用如图装置进行实验,试回答下列问题。

(1)若开始时开关K与a连接,则B极的电极反应式为_____________。
(2)若开始时开关K与b连接,总反应的离子方程式为_______。有关上述(2)实验,下列说法正确的是(填序号)____________。
①溶液中Na+向A极移动
②若标准状况下B极产生2.24 L气体,则溶液中转移0.2 mol 电子
③反应一段时间后加适量盐酸可恢复到电解前电解质的浓度
④从A极处逸出的气体能使湿润的KI淀粉试纸变蓝
(3)该小组同学认为,如果模拟工业上离子交换膜法制烧碱的方法,那么可以设想用如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。

①该电解槽的阳极反应式为:_________________。
②制得的氢氧化钾溶液从出口(填写“A”、“B”、“C”、“D”)______导出。
【答案】![]()
![]() ④
④ ![]() D
D
【解析】
(1)若开始时开关K与a连接,则形成原电池反应,为铁的吸氧腐蚀;
(2)若开始时开关K与b连接,形成电解池装置,石墨为阳极,发生氧化反应生成氯气,铁为阴极,发生还原反应生成氢气和氢氧化钠;
(3)①电解时,溶液中的氢氧根离子的放电能力大于硫酸根离子的放电能力,阳极上失电子发生氧化反应;②钾离子通过阳离子交换膜进入阴极生成氢氧化钾,阳极氢氧根放电生成氧气,硫酸根通过阴离子膜进入阴极区得到硫酸。
(1)开始时开关K与a连接,是原电池,铁为负极,发生氧化反应,失去电子生成亚铁离子,电极方程式为![]() ;
;
(2)开关K与b连接,装置为电解池,铁为阴极,发生还原反应为:![]() ,石墨为阳极发生氧化反应:
,石墨为阳极发生氧化反应:![]() ,总方程式为
,总方程式为![]() 。
。
①电解过程中阳离子向阴极移动,B为阴极,溶液中Na+向,B极移动,故①错误;
②电子只能通过导线,不能通过溶液,故②错误;
③反应一段时间后通入适量HCl气体,可恢复到电解前电解质的浓度,不是加入盐酸,故③错误;
④A生成氯气,能使湿润KI淀粉试纸变蓝,故④正确。
故答案为④;
(3)①电解时,阳极上失电子发生氧化反应,溶液中的氢氧根离子的放电能力大于硫酸根离子的放电能力,所以阳极上氢氧根离子失电子生成水和氧气![]() 。
。
②阴极氢离子放电,氢氧根离子浓度增大,钾离子向阴极移动,所以氢氧化钾在阴极生成,这说明制得的氢氧化钾溶液从出口D导出。


科目:高中化学 来源: 题型:
【题目】NaOH溶液滴定邻苯二甲酸氢钾(邻苯二甲酸氢钾H2A的Ka1=1.1×103 ,Ka2=3.9×106)溶液,混合溶液的相对导电能力变化曲线如图所示,其中b点为反应终点。下列叙述错误的是

A. 混合溶液的导电能力与离子浓度和种类有关
B. Na+与A2的导电能力之和大于HA的
C. b点的混合溶液pH=7
D. c点的混合溶液中,c(Na+)>c(K+)>c(OH)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋资源的开发与利用具有广阔的前景。海水的pH一般在7.5~8.6之间。某地海水中主要离子的含量如下表:
成分 | Na+ | K+ | Ca2+ | Mg2+ | Cl- | SO42- | HCO3- |
含量/mgL-1 | 9360 | 83 | 160 | 1100 | 16000 | 1200 | 118 |
(1)海水显弱碱性的原因是(用离子方程式表示):____________,该海水中Ca2+的物质的量浓度为__________mol/L 。
(2)电渗析法是近年发展起来的一种较好的海水淡化技术,其原理如下图所示。其中阴(阳)离子交换膜只允许阴(阳)离子通过,电极均为惰性电极。

① 开始时阳极的电极反应式为________________。
② 电解一段时间,____极(填“阴”或“阳”)会产生水垢,其成份为_____(填化学式)。
③ 淡水的出口为a、b、c中的__________出口。
(3)海水中锂元素储量非常丰富,从海水中提取锂的研究极具潜力。锂是制造化学电源的重要原料,如LiFePO4电池某电极的工作原理如图所示:

该电池电解质为能传导 Li+的固体材料。
上面左图中的小黑点表示_____(填粒子符号),充电时该电极反应式为_______。
(4)利用海洋资源可获得MnO2 。MnO2可用来制备高锰酸钾:将MnO2与KOH混合后在空气中加热熔融,得到绿色的锰酸钾(K2MnO4),再利用氯气将锰酸钾氧化成高锰酸钾。该制备过程中消耗相同条件下氯气和空气的体积比为_________(空气中氧气的体积分数按20%计)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钴、镍与铁是同族元素,它们的单质及化合物的性质有很多相似之处。
(1)为了比较Fe、Co、Cu三种金属的活动性,某实验小组设计如下甲、乙、丙三个实验装置。丙装置中X、Y均为石墨电极。反应一段时间后,可观察到甲装置中Co电极附近产生气泡,丙装置中X极附近溶液变红。
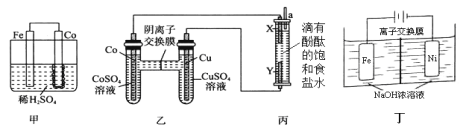
①甲池Fe电极反应式为_________。由现象可知三种金属的活动性由强到弱的顺序是__________(填元素符号)。
②写出丙装置中反应的离子方程式____________________。
(2)Na2FeO4具有广泛用途,可通过电解法制取得到,工作原理图丁所示。通电后,铁电极附近生成紫红色的FeO42,镍电极有气泡产生。已知: Na2FeO4只在强碱性条件下稳定,易被H2还原。
①Fe电极反应式为________。
②电解过程中,须将阴极产生的气体及时排出,其原因是_______________。
③当阴极产生112mL(标准状况)的气体时,通过阴离子交换膜的离子有_______mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向物质的量各有1mol的NH4Al(SO4)2和H2SO4混合稀溶液中逐滴加入一定量Ba(OH)2溶液,产生沉淀的量随着Ba(OH)2 加入量的变化如图所示。下列离子方程式书写正确的是

A. O→A:H++SO42-+Ba2++OH-=BaSO4↓+H2O
B. A→B:2Al3++3SO42-+3Ba2+ +6OH-=3BaSO4↓+2Al(OH)3↓
C. B→C:NH4++SO42-+Ba2+ +OH-=BaSO4↓+NH3·H2O
D. D→E:NH4++ OH-=NH3·H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向VmL0.1mol/L氨水中滴加等物质的量浓度的稀H2SO4,测得混合溶液的温度和pOH[pOH=-lgc(OH-)]随着加入稀硫酸的体积的变化如图所示(实线为温度变化,虚线为pOH变化),下列说法不正确的是( )
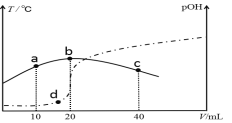
A. a、b、c三点由水电离的c(H+)依次减小
B. V=40
C. b点时溶液的pOH>pH
D. a、b、d三点对应NH3·H2O的电离常数:K(b)>K(d)>K(a)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通过传感器可以监测空气中甲醛的含量。一种燃料电池型甲醛气体传感器的原理如图所示,下列说法错误的是

A. a为电池的正极,发生还原反应
B. b极的电极反应为HCHO+H2O-4e-==CO2+4H+
C. 传感器工作过程中,电解质溶液中硫酸的浓度减小
D. 当电路中转移2×10-4 mol电子时,传感器内参加反应的HCHO为3.0 mg
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在给定条件下,下列选项所示的物质间转化均能实现的是( )
A.NaCl(aq)![]() Cl2(g)
Cl2(g)![]() FeCl2(s)
FeCl2(s)
B.S(s)![]() SO3(g)
SO3(g)![]() H2SO4(aq)
H2SO4(aq)
C.Al(s)![]() AlCl3(aq)
AlCl3(aq)![]() Al(OH)3(s)
Al(OH)3(s)
D.N2(g)![]() NH3(g)
NH3(g)![]() Na2CO3(s)
Na2CO3(s)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温恒容容器中发生N2O4(g)2NO2(g),若反应物的浓度由0.1molL﹣1降到0.06molL﹣1需20s,那么由0.06molL﹣1降到0.036molL﹣1,所需反应时间为( )
A. 10 sB. 12 sC. 大于12 sD. 小于12 s
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com