
【题目】氧化还原反应广泛地存在于生产和生活之中.
(1)铜丝浸入AgNO3溶液后,表面会附有银白色物质,则还原性:银(填“大于”、“小于”或“等于”,下同)铜.
(2)为防治碘缺乏病,通常在食盐中添加少量的碘酸钾(KIO3).碘酸钾和碘化钾在溶液中能发生下列反应:KIO3+5KI+3H2SO4═3I2+3K2SO4+3H2O
①该反应中,氧化产物与还原产物的质量之比为
②当有1mol I2生成时,有mol还原剂被氧化.
(3)某一反应体系中有反应物和生成物共5种物质:H2S、HNO3、NO、H2O、X.
①已知H2S在反应中失去电子,则该反应的氧化剂是 .
②已知0.5mol H2S在反应中失去1mol电子生成X,则X的化学式为 .
【答案】
(1)小于
(2)5:1;![]()
(3)HNO3;S
【解析】解:(1)铜丝浸入AgNO3溶液后,表面会附有银白色物质,说明铜置换出银,则说明银的还原性小于铜,故答案为:小于;(2)5KI+KIO3+3H2SO4═3I2+3K2SO4+3H2O中,KI中I元素的化合价由﹣1价升高为0,KIO3中I元素的化合价由+5价降低为0,则①该反应中,氧化产物与还原产物的质量之比为5:1,故答案为:5:1;②该反应中生成3molI2 , 有5molKI被氧化,则有1mol I2生成时,有 ![]() mol还原剂被氧化,故答案为:
mol还原剂被氧化,故答案为: ![]() ;(3)①H2S在反应中失去电子,则被氧化,反应中为还原剂,则具有氧化性的只有HNO3 , 在反应中得电子被还原生成NO,氧化剂为HNO3 , 故答案为:HNO3;②已知0.5mol H2S在反应中失去1mol电子生成,则设反应后S元素化合价为x,则0.5(x+2)=1,x=0,应生成S单质,
;(3)①H2S在反应中失去电子,则被氧化,反应中为还原剂,则具有氧化性的只有HNO3 , 在反应中得电子被还原生成NO,氧化剂为HNO3 , 故答案为:HNO3;②已知0.5mol H2S在反应中失去1mol电子生成,则设反应后S元素化合价为x,则0.5(x+2)=1,x=0,应生成S单质,
故答案为:S.
(1)铜丝浸入AgNO3溶液后,表面会附有银白色物质,说明铜置换出银,根据还原剂还原性大于还原产物判断;(2)5KI+KIO3+3H2SO4═3I2+3K2SO4+3H2O中,KI中I元素的化合价由﹣1价升高为0,KIO3中I元素的化合价由+5价降低为0,结合氧化还原反应中基本概念来解答;(3)H2S在反应中失去电子,则被氧化,反应中为还原剂,则具有氧化性的只有HNO3 , 在反应中得电子被还原生成NO,结合质量守恒定律判断X.


 一线名师权威作业本系列答案
一线名师权威作业本系列答案科目:高中化学 来源: 题型:
【题目】据报道,最近摩托罗拉(MOTOROLA)公司研发了一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,电量是现用镍氢电池和锂电池的10倍,可连续使用1个月充电一次。假定放电过程中,甲醇完全氧化产生的CO2被充分吸收生成CO32-
(1)该电池反应的总离子方程式为____________________________________________。
(2)甲醇在______极发生反应(填正或负),电池在放电过程中溶液的pH将______(填降低或上升、不变);若有16克甲醇蒸气被完全氧化,产生的电能电解足量的CuSO4溶液,(假设整个过程中能量利用率为80%),则将产生标准状况下的O2________升。
(3)最近,又有科学家制造出一种固体电解质的燃料电池,其效率更高。一个电极通入空气,另一电极通入汽油蒸气。其中固体电解质是掺杂了Y2O3(Y:钇)的ZrO2(Zr:锆)固体,它在高温下能传导O2-离子(其中氧化反应发生完全)。以丁烷(C4H10)代表汽油。
①电池的负极反应式为____________________________________________。
②放电时固体电解质里的O2-离子的移动方向是向____________极移动(填正或负)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依据图中氮元素及其化合物的转化关系,判断下列说法不正确的是( )

A. X是N2O5
B. 可用排水法收集NO、NO2气体
C. 工业上以NH3、空气、水为原料生产硝酸
D. 由NH3→N2,从原理上看,NH3可与NO2反应实现
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某一元弱酸(用HA表示)在水中的电离方程式是:HA![]() H++A﹣,回答下列问题:
H++A﹣,回答下列问题:
(1)向溶液中加入适量NaA固体,以上平衡将向______(填“正”、“逆”)反应方向移动。
(2)若向溶液中加水稀释,以上平衡将向_______(填“正”、“逆”)反应方向移动,溶液中c(A﹣)将____(填“增大”、“减小”或“不变”),溶液中c(OH﹣)将____(填“增大”、“减小”或“不变”)。
(3)已知室温时,0.1mol·L﹣1的某一元酸HA在水中有 0.1% 发生电离,回答下列各问题:
①该溶液的pH=_______。
②HA的电离平衡常数K=________。
③NaA溶液显碱性的原因:_____________________________(用离子方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2A(g)+B(g)3C(g)+4D(g)的反应,在不同条件下的反应的速率最快的是( )
A.v(A)=0.7 mol/(L.min)
B.v(B)=0.3mol/(L.min)
C.v(C)=0.9 mol/(L.min)
D.v(D)=1.1mol/(L.min)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下发生反应:2A(g)+2B(g)xC(g)+2D(g),在2L密闭容器中,把4molA和2molB混合,2min后达到平衡时生成1.6molC,又测得反应速率VD=0.2mol/(Lmin),下列说法正确的是( )
A.A和B的转化率均是20%
B.x=4
C.平衡时A的物质的量为2.8mol
D.平衡时气体压强比原来减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外小组运用电化学原理合成氨,其装置结构如图所示。下列有关说法不正确的是

A. 放电时,b极表面H2和CO均被氧化
B. 该电池工作时,H+由b极区迁移至a极区
C. a极的电极反应为N2+6H++6e-=2NH3
D. b极区发生反应CO+H2O=CO2+H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NH3催化还原NxOy可以消除氮氧化物的污染.
已知:反应Ⅰ:4NH3(g)+6NO(g)5N2(g)+6H2O(l)△H1
反应Ⅱ:2NO(g)+O2(g)2NO2(g)△H2 (且|△H1|=2|△H2|)
反应Ⅲ:4NH3(g)+6NO2(g)5N2(g)+3O2(g)+6H2O(l)△H3
反应I和反应II在不同温度时的平衡常数及其大小关系如表
温度/K | 反应I | 反应II | 已知: |
298 | K1 | K2 | |
398 | K1′ | K2′ |
(1)推测反应Ⅲ是反应(填“吸热”或“放热”)
(2)相同条件下,反应I在2L密闭容器内,选用不同的催化剂,反应产生N2的量随时间变化如图所示.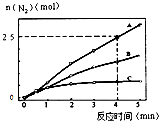
①计算0~4分钟在A催化剂作用下,反应速率v(NO)=
②下列说法正确的是 .
A.该反应的活化能大小顺序是:Ea(A)>Ea(B)>Ea(C)
B.增大压强能使反应速率加快,是因为增加了活化分子百分数
C.单位时间内H﹣O键与N﹣H键断裂的数目相等时,说明反应已经达到平衡
D.若在恒容绝热的密闭容器中发生反应,当K值不变时,说明反应已经达到平衡
(3)一定条件下,反应II达到平衡时体系中n(NO):n(O2):n(NO2)=2:1:2.在其它条件不变时,再充入NO2气体,分析NO2体积分数﹣﹣φ(NO2)的变化情况:(填“变大”、“变小”或“不变”)恒温恒压容器,φ(NO2);恒温恒容容器,φ(NO2) .
(4)一定温度下,反应III在容积可变的密闭容器中达到平衡,此时容积为3L,c(N2)与反应时间t变化曲线X如图所示,若在t1时刻改变一个条件,曲线X变为曲线Y或曲线Z.则: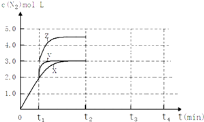
①变为曲线Y改变的条件是 . 变为曲线Z改变的条件是
②若t2降低温度,t3达到平衡,请在图中画出曲线X在t2﹣t4内 c(N2)的变化曲线.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com