
【题目】在有机物分子中,若某个碳原子连接着四个不同的原子或原子团,则这个碳原子被称为“手性碳原子”,新型纤维酸类降脂药克利贝特可由物质X在一定条件下反应制得:
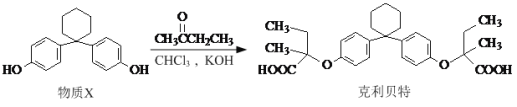
下列有关叙述正确的是
A. 克利贝特的分子式为C28H34O6
B. B.物质X分子中所有碳原子可能位于同一平面内
C. 用NaOH溶液可以鉴别物质X和克利贝特
D. 物质X中无手性碳原子,克利贝特中有两个手性碳原子
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】前中国科学院院长卢嘉锡与法裔加拿大科学家Gignere巧妙地利用尿素(H2NCONH2)和H2O2形成化合物H2NCONH2·H2O2,不但使H2O2稳定下来,而且其结构也没有发生改变,得到了可供衍射实验的单晶体。下列说法中不正确的是
A. H2NCONH2与H2O2是通过氢键结合的B. H2O2分子中只含σ键,不含π键
C. H2NCONH2中σ键与π键的数目之比为7:1D. H2NCONH2·H2O2属于离子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,HNO2的电离平衡常数为K=4.6×10-4(已知![]() 2.14),向20mL0.01molL-1HNO2溶液中逐滴加入相同浓度的NaOH溶液,测得混合液的 pH随NaOH溶液体积的变化如图所示,下列判断正确的是( )
2.14),向20mL0.01molL-1HNO2溶液中逐滴加入相同浓度的NaOH溶液,测得混合液的 pH随NaOH溶液体积的变化如图所示,下列判断正确的是( )
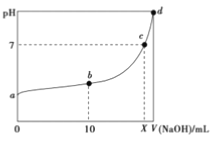
A. X=20
B. a点溶液中c(H+)=2.14×10-3molL-1
C. b点溶液中微粒浓度的大小关系为c(HNO2)>c(Na+)>c(NO2-)
D. 水的电离程度b>d
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】航天飞机用的铝粉与高氯酸铵(NH4ClO4)的混合物为固体燃料,点燃时铝粉氧化放热引发高氯酸铵反应,其方程式可表示为:2NH4ClO4 ![]() N2↑+ 4H2O+Cl2↑+2O2↑,放出热量为Q,下列对此反应叙述中错误的是( )
N2↑+ 4H2O+Cl2↑+2O2↑,放出热量为Q,下列对此反应叙述中错误的是( )
A. 上述反应瞬间产生大量高温气体推动航天飞机飞行
B. 反应属于分解反应
C. 反应从能量变化上说,主要是化学能转变为热能和动能
D. 在反应中高氯酸铵只起氧化剂作用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知元素镓和砷的单质及其化合物在工业生产上有重要的用途。回答下列问题:
(1)砷元素基态原子的电子排布式为_______________________。
(2)砷与氢元素可形成化合物砷化氢,该化合物的空间构型为_____________,其中砷原子的杂化方式为__________。
(3)根据等电子原理,写出由短周期元素组成且与砷化氢互为等电子体的一种离子的化学式________。
(4)已知由元素砷与镓元素组成的化合物A为第三代半导体。已知化合物A的晶胞结构与金刚石相似,其中砷原子位于立方体内,镓原子位于立方体顶点和面心,请写出化合物A的化学式____________;
(5)已知铝与镓元素位于同一主族,金属铝属立方晶系,其晶胞边长为405 pm,密度是2.70g·cm-3,通过计算确定铝原子在三维空间中堆积方式________________(已知NA=6.02×1023,1pm=10-10cm,4053=6.64×107);晶胞中距离最近的铝原子可看作是接触的,列式计算铝的原子半径r(A1)=______pm.(只列出计算式即可)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年是元素周期表诞生150周年,元素周期表(律)在学习、研究和生产实践中有很重要的作用。下表为元素周期表的一部分,回答下列问题。
族 周期 | IA | 0 | ||||||
1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
2 | ② | ③ | ||||||
3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
4 | ||||||||
(1)元素①~⑧中,金属性最强的是________(填元素符号)。
(2)中国青年化学家姜雪峰被国际组织推选为“元素⑦代言人”,元素⑦的原子结构示意图是________,其氢化物的电子式是_________。
(3)元素①和②可以形成多种化合物。下图模型表示的分子中,不可能由①和②形成的是_______(填序号)。
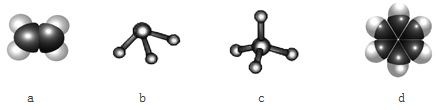
(4)比较元素②、③的最高价氧化物对应水化物的酸性:______>______(填化学式)。说明你判断的理由:_________。
(5)主族元素砷(As)的部分信息如图所示。
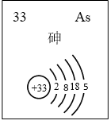
i.砷(As)在周期表中的位置是______。
ii.下列说法正确的是_______(填序号)。
a. 砷元素的最高化合价为+4
b. 推测砷有多种氧化物
c. ③的气态氢化物的还原性大于砷的气态氢化物的还原性
(6)某小组同学设计实验比较VIIA元素的非金属性:Cl>Br>I。
已知:常温下浓盐酸与高锰酸钾反应生成氯气。
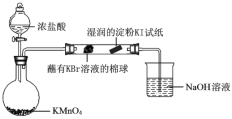
打开分液漏斗的活塞,烧瓶中产生黄绿色气体,蘸有KBr溶液的棉球变为橙红色,湿润的淀粉KI试纸变蓝,据此现象能否说明非金属性:Br > I,并说明理由_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个不传热的固定容积的容器中,对于反应 A(g)+2B(g)![]() 3C(g)(正反应为吸热反应),下列叙述为平衡状态标志的是
3C(g)(正反应为吸热反应),下列叙述为平衡状态标志的是
①体系的温度不再变化 ②外界条件不变时,A、B、C浓度保持不变 ③气体平均分子量不再变化 ④体系的压强不再变化 ⑤气体密度不再变化 ⑥3 v正(B)=2 v逆(C) ⑦单位时间内消耗1 mol A(g)的同时生成3 mol C(g)
A.①②⑥B.①②③⑤C.②③④⑤D.①②④⑤⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求回答下列问题
Ⅰ.下列物质组别中:A.冰与水 B.H2、D2、T2 C.O2与 O3 D. ![]() 与
与![]() E.CH3—CH2—CH2—CH3与
E.CH3—CH2—CH2—CH3与![]() F.
F. 与
与 G.甲烷和庚烷。
G.甲烷和庚烷。
①互为同位素的是_________(填组别选项,下同);
②互为同素异形体的是_________;
③互为同分异构体的是_________;
④属于同一物质的是_________;
⑤属于同系物的是_________。
Ⅱ.(1)乙烯使溴水褪色的反应类型和使酸性高锰酸钾溶液褪色的反应类型_______(填“相同”或“不相同”)。
(2)用苯制备溴苯的化学方程式是_____________________,该反应的类型_________。
(3)已知 2CH3CHO+O2![]() 2CH3COOH。若以乙烯为主要原料合成乙酸,其合成路线如图所示。则反应②的化学方程式为______________,该反应的类型为__________。
2CH3COOH。若以乙烯为主要原料合成乙酸,其合成路线如图所示。则反应②的化学方程式为______________,该反应的类型为__________。
![]()
Ⅲ.在光照条件下,CH4与Cl2能发生取代反应。若将1 mol CH4与一定量Cl2反应,待反应完全测得四种有机取代产物的物质的量之比为 n(CH3Cl)∶n(CH2Cl2)∶n(CHCl3)∶n(CCl4)=1∶1∶1∶1,则消耗的Cl2物质的量为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值。下列说法正确的是
A.15g14CO与15N2的混合气体所含质子数为7.5NA
B.11.2LCl2与NaOH溶液反应转移电子数为0.5NA
C.2molSO2与1mol02反应生成SO3的分子数为2NA
D.48gO2和O3的混合气体中含有3NA个氧原子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com