
【题目】甲酸为一元弱酸,在15mL0.1mol/L KOH溶液中逐滴加入0.2mol/L甲酸溶液,溶液的pH变化和所加入的甲酸的体积关系描绘成如图所示曲线。下面有关微粒浓度的大小关系正确的是
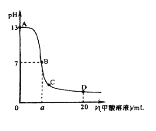
A. 在A、B间的任意一点上都存在:c(K+)>c(HCOO-)>c(OH-)>c(H+)
B. 在B点:c(K+)= c(HCOO-)>c(OH-)=c(H+),且a=7.5
C. 在C点:c(HCOO-)>c(K+)>c(H+)>c(OH-)
D. 在D点: c(HCOO-)+ c(HCOOH)=2 c(K+)
【答案】C
【解析】
A. 刚滴加甲酸时,氢氧化钾过量,c(OH-)>c(HCOO-)。
B. 滴加甲酸7.5mL时,氢氧化钾和甲酸恰好完全反应,生成物为强碱弱酸盐,,HCOO-会发生水解溶液呈碱性。
C. C点甲酸过量溶液呈酸性,c(H+)>c(OH-),根据电荷守恒可知c(HCOO-)>c(K+)。
D. D点甲酸过量,加入甲酸物质的量为0.02L×0.2mol/L=0.004mol,KOH物质的量为0.015L×0.1mol/L=0.0015mol,根据物料守恒进行分析。
A.刚滴加甲酸时,氢氧化钾过量,c(OH-)>c(HCOO-),A错误。
B.滴加甲酸7.5mL时,氢氧化钾和甲酸恰好完全反应,生成物为强碱弱酸盐,溶液呈碱性,c(OH-)>c(H+)。B点pH为7,甲酸应该稍过量,a>7.5,B错误。
C. C点甲酸过量溶液呈酸性,c(H+)>c(OH-),根据电荷守恒可知c(HCOO-)>c(K+),在C点:c(HCOO-)>c(K+)>c(H+)>c(OH-),C正确。
D. D点甲酸过量,加入甲酸物质的量为0.02L×0.2mol/L=0.004mol,KOH物质的量为0.015L×0.1mol/L=0.0015mol,根据物料守恒 c(HCOO-)+c(HCOOH)>2 c(K+),D错误。


科目:高中化学 来源: 题型:
【题目】将体积均为V0的三种溶液分别加水稀释至体积为V时,pH与V0/V的关系如下图所示:

下列说法正确的是
A. 酸性:HX>HY
B. HX溶液滴定NaOH溶液时指示剂用甲基橙比用酚酞误差小
C. “HX+NaX-混合溶液中,V0/V=10-1时,c(HX)<c(X-)
D. V0/V在10-1~10-3,“HX+NaX”混合溶液随V0/V的减小,X-的水解与HX的电离程度始终保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列溶液中各组离子一定能大量共存的是
A.使石蕊试液呈红色的溶液中:Na+、Al3+、NO3-、![]()
B.![]() =0.1 mol·L-1的溶液:Na+、K+、CO32-、NO3-
=0.1 mol·L-1的溶液:Na+、K+、CO32-、NO3-
C.含有0.1 mol·L-1 HCO3-的溶液:Na+、Fe3+、NO3-、SCN-
D.由水电离产生的c(H+)=10-12 mol·L-1的溶液:NH4+,SO42-、HCO3-、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】橡皮筋在拉伸和收缩状态时结构如图,在其拉伸过程中有放热现象。25℃、101kPa时,下列过程的焓变、熵变和自发性与橡皮筋从拉伸状态到收缩状态一致的是( )
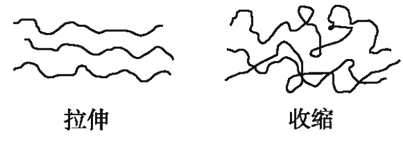
A. CaCO3=CaO+CO2↑
B. NaOH的溶解
C. 2H2+O2=2H2O
D. Ba(OH)28H2O+2NH4Cl=BaCl2+2NH3↑+10H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质能满足如图所示转化关系的是(图中箭头表示进一步转化)

a | b | c | d | |
① | Si | SiO2 | H2SiO3 | Na2SiO3 |
② | Al | AlCl3 | NaAlO2 | Al(OH)3 |
③ | Cu | CuO | Cu(OH)2 | CuSO4 |
④ | Fe2O3 | FeCl3 | FeCl2 | Fe |
A. ①② B. ②③ C. ③④ D. ②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】欲测定含少量氯化钠的小苏打固态样品中NaHCO3的质量分数可采用以下四种方法。
方法一: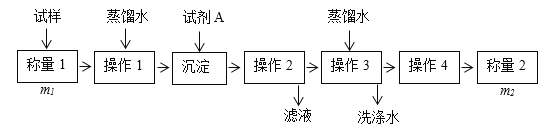
方法二: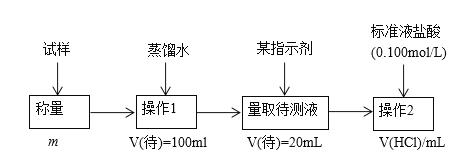
方法三: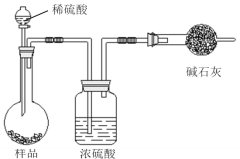
方法四:不使用化学试剂,使用实验室常用仪器
按要求回答下列问题:
(1)方法一:加入足量的试剂A______(填写A的化学式)可将HCO3-离子转化为沉淀并称重。操作1、2、3、4的名称依次是溶解、_______、洗涤和_______;
(2)方法二:在操作1中所用到的玻璃仪器中,除了烧杯、玻璃棒外,还需要的用到的是_____,在操作2中应选择的指示剂是____________;
(3)在方法二中计算该样品中NaHCO3的质量分数为___________[用流程图中的数据m、V(HCl) 填写有关的表达式];
(4)在方法三中:根据所用的实验装置,除了称量试样质量外,还需测定的实验数据是________;
(5)仔细分析方法三中的实验装置,若由此测得的数据来计算实验结果,则有可能偏高也有可能偏低,偏高的原因可能是__________,偏低的原因可能是_______(均文字简述);
(6)方法四的实验原理是:_____________(用化学方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】没食子酸丙酯简称PG,是一种白色粉末,难溶于水,微溶于棉子油等油脂,是常用的食用油抗氧化剂。其结构简式如图所示。
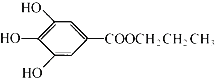
已知:PG经水解可转化为没食子酸,没食子酸能与NaHCO3溶液反应生成CO2
回答下列问题:
(1)从分子结构或性质上看,PG具有抗氧化作用的主要原因是:______(文字简述)
(2)1mol没食子酸最多可以与含________mol碳酸钠的溶液发生反应。
(3)写出PG在NaOH溶液中水解的化学方程式:_______________________。
(4)没食子酸有多种同分异构体,写出其中符合下列要求的同分异构体的结构简式:____。
a.含有苯环,且苯环上的一溴代物只有一种;
b.既能发生银镜反应,又能发生水解反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列热化学方程式:Zn(s) +![]() O2(g) =ZnO(s) ΔH1=-351.1kJ/mol
O2(g) =ZnO(s) ΔH1=-351.1kJ/mol
Hg(l) +![]() O2(g) = HgO(s) ΔH2=-90.7kJ/mol
O2(g) = HgO(s) ΔH2=-90.7kJ/mol
由此可知Zn(s) + HgO(s) = ZnO(s) + Hg(l)的ΔH3,其中ΔH3的值是
A.-260.4 kJ/molB.-254.6 kJ/molC.-438.9 kJ/molD.-441.8 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】测定溶液电导率的变化是定量研究电解质在溶液中反应规律的一种方法,溶液电导率越大其导电能力越强。室温下,用0.100molL-1的NH3H2O滴定10.00mL浓度均为0.100molL-1HCl和CH3COOH的混合溶液,所得电导率曲线如图所示。下列说法正确的是( )
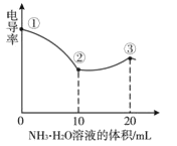
A.①点溶液:pH最大
B.溶液温度:①高于②
C.③点溶液中:c(Cl-)>c(CH3COO-)
D.②点溶液中:c(NH4+)+c(NH3H2O)>c(CH3COOH)+c(CH3COO-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com