
����Ŀ����1��ͼ1��ʾ10mL��Ͳ��Һ���λ�ã�A��B,B��C�̶ȼ����1mL, ����̶�AΪ4��������Һ��������__________mL��
��2��ͼII��ʾ50mL�ζ�����Һ����λ�ã����Һ�洦�Ķ�����a ����ζ�����Һ������������ţ�________��
A. ��amL B.�ǣ�50-a��mL
C. һ������amL D.һ�����ڣ�50-a��mL
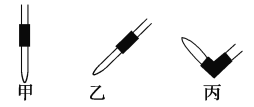
��3����ȥ��ʽ�ζ��������ݵķ���Ӧ������ͼ��ʾ�����е�____________��Ȼ�����ἷѹ������ʹ���첿�ֳ�����Һ��

��4��ʵ���ҳ����ü�ȩ���ⶨ(NH4)2SO4��Ʒ�е��������������䷴Ӧԭ��Ϊ��
4NH4����6HCHO��3H����6H2O��(CH2)6N4H��
�ζ�ʱ��1mol (CH2)6N4H����1mol H���൱��Ȼ����NaOH����Һ�ζ���Ӧ���ɵ��ᡣij��ȤС���ü�ȩ������������ʵ�飺
����I����ȡ��Ʒ1.500g��
�������Ʒ�ܽ����ȫת�Ƶ�250mL����ƿ�У����ݣ����ҡ�ȡ�
�������ȡ25.00mL��Ʒ��Һ��250mL��ƿ�У�����10mL20�������Լ�ȩ��Һ��ҡ�ȡ�����5min����1��2�η�̪��Һ����NaOH����Һ�ζ����յ㡣�����������������ظ�2�Ρ�
��1�����ݲ������գ�
����ʽ�ζ���������ˮϴ�Ӻ�ֱ�Ӽ���NaOH����Һ���еζ���������Ʒ�е����������� ���ƫ�ߡ�����ƫ�͡�����Ӱ�족����
����ƿ������ˮϴ�Ӻ�ˮδ��������ζ�ʱ��ȥNaOH����Һ����� ���ƫ����ƫС������Ӱ�족����
���ζ�ʱ�ߵα�ҡ����ƿ���۾�Ӧ�۲� ��
A �ζ�����Һ��ı仯 B ��ƿ����Һ��ɫ�ı仯
���ζ��ﵽ�յ�ʱ����ָ̪ʾ���� ɫ��� ɫ��
��2���ζ�������±���ʾ��
�ζ����� | ������Һ�� ���/mL | ����Һ����� | |
�ζ�ǰ�̶�/mL | �ζ���̶�/mL | ||
1 | 25.00 | 1.02 | 21.03 |
2 | 25.00 | 2.00 | 21.99 |
3 | 25.00 | 0.20 | 20.20 |
��NaOH����Һ��Ũ��Ϊ0.1010mo1��L��1�������Ʒ�е�����������Ϊ ��
���𰸡���1��3.2��2��D��3������4����1����ƫ�� ����Ӱ�� ��B �������ۺ죨��dz�죩��2��18.85��
��������
�����������1����Ͳ���̶����϶�����С������̶�AΪ4��������Һ��������3.2mL��
��2���ζ������̶����϶�����������������Һ�洦�Ķ�����a ����ζ�����Һ������һ�����ڣ�50-a��mL����ѡD��
��3����ȥ��ʽ�ζ��������ݵķ���Ӧ������ͼ��ʾ�����е���������Ȼ�����ἷѹ������ʹ���첿�ֳ�����Һ��
��4���ټ�ʽ�ζ���������ˮϴ�Ӻ�û����NaOH����Һ��ϴ��ֱ�Ӽ���NaOH����Һ��ʹ�ζ�������������Һ��Ũ��ƫС���������������Ʊ���Һ����жϣ��ò����Ʒ��(CH2)6N4H��ƫ�࣬��˽��������������ƫ�ߣ�
����ƿ������ˮϴ�Ӻ�ˮδ������������Һ�к��еı��̶ȵ����ʵ����ʵ������䣬��ζ�ʱ��ȥNaOH����Һ�����Ҳ���䣬��˲�������κ�Ӱ�죻
�۵ζ�ʱ�ߵα�ҡ����ƿ���۾�Ӧ�۲���ƿ����Һ��ɫ�ı仯����ѡ��B��ȷ��
������ָʾ����̪������Һ�У�����֪Ũ�ȵļ�ζ�δ֪Ũ�ȵ��ᣬ��˿�ʼ��Һ����ɫ�����ζ��ﵽ�յ�ʱ����ָ̪ʾ������ɫ���dz��ɫ��
��5������ʵ���֪��һ��ʵ�鷴Ӧ���ı���Һ�����21.03mL-1.02mL��20.01mL���ڶ���ʵ�鷴Ӧ���ı���Һ�����21.99mL-2.00mL��19.99ml��������ʵ�鷴Ӧ���ı���Һ�����20.20mL-0.20mL��20.00ml����˷�Ӧ���ı���Һ�������V��(20.01mL+19.99ml+20.00ml)��3��20.00mL�������ᡢ����кͷ�Ӧʱ�����ʵ�����ϵ��1:1��֪��c��25.00mL��0.1010 mol��L��1��20.00mL�����c��0.0808mol/L����250mL��Һ�к���(CH2)6N4H����H+�����ʵ�����0.0808mol/L��0.25L��0.0202mol������1.500 g��Ʒ�к�NH4+�����ʵ�����0.0202mol�����к���N��������m(N)��0.0202mol��14g/mol��0.2828g������NԪ�ص����������ǣ�0.2828g��1.500 g����100%��18.85%��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������������У�����֤������������ʵ��ǣ� ��
A. 1mol/L������Һ��c��H+��=10-2mol/L�� B. �������κα���ˮ���ܣ�
C. 10mL1mol/L����ǡ����10mL1mol/LNaOH��Һ��ȫ��Ӧ�� D. ������Һ�ĵ����Ա�������Һ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������Ҫʵ����Ҫ�顣���˻�����˼������Ҫ��̤ʵ�أ�������ҵ�гɣ���ȼ��ȼ��Ҫ�ܿ�һЩ������ȼ�ո���������Ҫ������Ŀ����
A. ���Ϳ�ȼ����Ż�� B. ��������������ĺ���
C. ���߿�ȼ����Ż�� D. �����ȼ���������ĽӴ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������Ǻ���һ�����һ�������ˮƽ����Ҫ��־��������������У���ؼ���һ����ӦΪ2SO2��g��+O2��g��![]() 2SO3��g��
2SO3��g��
��1��һ�������£�SO2��O2��Ӧ10min����SO2��SO3�����ʵ���Ũ�ȷֱ�Ϊ1mol/L��3mol/L����SO2��ʼ���ʵ���Ũ��Ϊ____________________��10min������SO3��ƽ����Ӧ����v��SO3��Ϊ____��
��2�����й��ڸ÷�Ӧ��˵����ȷ����_________����ѡ����ĸ����
A.����O2��Ũ���ܼӿ췴Ӧ����
B.������ϵ�¶��ܼӿ췴Ӧ����
C.ʹ�ô����ܼӿ췴Ӧ����
D.һ�������´ﵽ��Ӧ��ʱSO2ȫ��ת��ΪSO3
��3���ڷ�Ӧ�����У���ijһʱ��SO2��O2��SO3��Ũ�ȷֱ�Ϊ0.2mol/L��0.1 mol/L��0.2mol/L������Ӧ�ﵽƽ��ʱ�����ܴ��ڵ�������___________����ѡ����ĸ����
A.O2Ϊ0.2mol/L B. SO2Ϊ0.25mol/L
C.SO3Ϊ0.4mol/L D. SO2��SO3��Ϊ0.15mol/L
��4��FeS2���ղ�����SO2�����������ᡣ��֪25�桢101KPaʱ��
2 SO2��g��+ O2��g��2SO3��g����H1=-197kJmol-1��
H2O��g���TH2O��l����H2=-44kJmol-1��
2SO2��g��+O2��g��+2H2O��g���T2H2SO4��l����H3=-545kJmol-1
��SO3��g����H2O��l����Ӧ����H2SO4��l�����Ȼ�ѧ����ʽ��____________________��
��5����ҵ�����ᣬ�ù����İ�ˮ��SO2����β���������÷�Ӧ�����ӷ���ʽΪ__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��Һ���ܺ���Cl����SO42����CO32����NH4+��Fe3+��Fe2+��Al3+��Na+��ijͬѧΪ��ȷ����ɷ֣�ȡ������Һ����Ʋ����������ʵ�飺
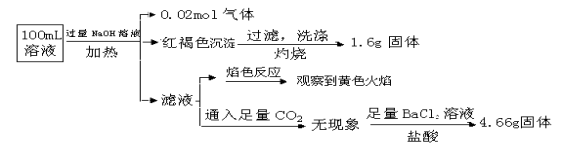
����˵����ȷ���ǣ� ��
A��ԭ��Һ��c��Fe3+��=0.2 mol��L-1
B����Һ��������4�����Ӵ��ڣ�����Cl��һ�����ڣ���c��Cl������0.2 mol��L-1
C��SO42����NH4+ ��Na+һ�����ڣ�CO32��һ��������
D��Ҫȷ��ԭ��Һ���Ƿ���Fe2+,�����Ϊ��ȡ����ԭ��Һ���Թ���,����������ˮ���������ټ�KSCN��Һ����Һ��Ѫ��ɫ������Fe2+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���ǣ� ��
A�������¶ȣ�Al2(SO4)3��Һ��pH����
B�������£�CuSO4��ҺpH��7�������ˮ�м���CuSO4������ˮ�ĵ��롣
C��Na2SiO3��Һ���ȡ����ɡ����պ����ù���ijɷ���SiO2��
D����ͬ�¶��£�AgCl����ͬ���ʵ���Ũ�ȵ�CaCl2��NaCl��Һ�е��ܽ�Ȳ�ͬ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����б仯ԭ����ͬ�������������
A. ��NaͶ��ˮ����Һ�ʼ��� B. Cl2��ʹƷ����ɫ
C. ���������������� D. ����̿����Ϊ��ˮ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʵ�ˮ��Һ��ˮ������Ե��ǣ� ��
A. SO2 B. AlCl3 C. NaHCO3 D. NaHSO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������X�͵���Y��Ӧ����X3+ ��Y2�� �� ����������������1��X����������2��X������������3��X3+�����������4��X���������ԣ���5��Y2���ǻ�ԭ�����6��X3+ ���������ԣ�������ȷ���ǣ� ��
A.��1����4����5����6��
B.��2����3����4����5��
C.��1����3����5����6��
D.��1����2����4����6��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com