
【题目】下列溶液中,跟100mL 0.5mol/L NaCl溶液所含的Cl-物质的量浓度相同的是( )
A. 50mL 0.5mol/L MgCl2溶液 B. 200mL 0.25mol/L AlCl3溶液
C. 100mL 0.5mol/L NaClO3溶液 D. 25mL 0.5mol/L HCl溶液
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】阿伏加德罗常数的值为NA。工业上,利用乙烯水化法制乙醇:CH2=CH2+H2O![]() CH3CH2OH。下列有关说法正确的是
CH3CH2OH。下列有关说法正确的是
A. 1mol乙烯和1mol乙醇分别完全燃烧,消耗O2的分子数均为3NA
B. 1mol H2O和H2F+的混合物中所含质子数为10NA
C. 乙醇催化氧化生成1mol乙醛时转移电子数为NA
D. 46g乙醇中所含共价键的数目为7NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W结构中含有三个六元环,是一种新型香料的主要成分之一.W的合成路线如下(部分产物和部分反应条件略去):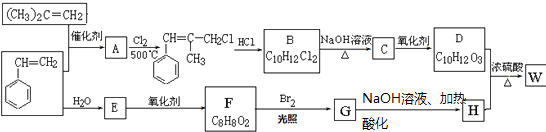 ,
,
已知:①RCH═CH2+CH2═CHR′ ![]() CH2═CH2+RCH═CHR′
CH2═CH2+RCH═CHR′
②B中核磁共振氢谱图显示分子中有6种不同环境的氢原子
③D和H是同系物,D与H发生反应生成W.
请回答下列问题:
(1)G分子中含有的官能团名称是 .
(2)A→B反应过程中涉及的反应类型有、 .
(3)A的结构简式为; F的结构简式为;
(4)B→C的化学方程式为;D+H→W的化学方程式为 .
(5)K为F的同系物,碳数比F多1,其符合下列条件的K的同分异构体共有种.a.能发生银镜反
b.能与FeCl3溶液发生显色反应
c.核磁共振氢谱上有四个峰,其峰面积之比为1:1:2:6
(6)K的所有同分异构体在下列﹣种表征仪器中显示的信号(或数据)完全相同,该仪器是(填标号).a.质谱仪 b.红外光谱仪 c.元素分析仪 d.核磁共振仪.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语表述正确的是__________其中更能反映其真实存在状况的是__________________
A.CO2的比例模型为:![]() B.NH4Cl的电子式为:
B.NH4Cl的电子式为: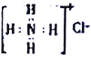
C.S2-结构示意图: D.丙烷分子的比例模型示意图:
D.丙烷分子的比例模型示意图: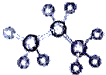
E.HC1O的结构式:H-O-C1 F.H2O2的电子式:![]()
G.2,2-二甲基丙烷的结构简式: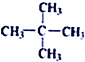 H.乙烯的实验式为CH2=CH2
H.乙烯的实验式为CH2=CH2
I.甲烷比例模型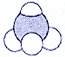 J.聚丙烯的结构简式为:
J.聚丙烯的结构简式为:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能影响水的电离平衡,并使溶液中的c(H+)>c(OH-)的措施是( )
A. 向水中通入SO2 B. 将水加热煮沸
C. 向纯水中投入一小块金属钠 D. 向水中加入NaCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量纯净的氨基甲酸铵置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)![]() 2NH3(g)+CO2(g)。可以判断该分解反应已经达到化学平衡的是
2NH3(g)+CO2(g)。可以判断该分解反应已经达到化学平衡的是
A. 2v(NH3) = v(CO2)
B. 密闭容器中总压强不变
C. 密闭容器中混合气体的平均摩尔质量不变
D. 密闭容器中二氧化碳的体积分数不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在容积为1L的密闭容器内放入2mol N2O4和8molNO2 , 发生如下反应:2NO2(红棕色)N2O4(无色)(△H<0),反应中NO2、N2O4的物质的量随反应时间变化的曲线如图,按下列要求作答:
(1)在该温度下,反应的化学平衡常数表达式为:
(2)若t1=10s,t2=20s,计算从t1至t2时以N2O4表示的反应速率:molL﹣1s﹣1
(3)图中t1、t2、t3哪一个时刻表示反应已经达到平衡?答:
(4)t1时,正反应速率(填“>”、“<”或“=”)逆反应速率
(5)维持容器的温度不变,若缩小容器的体积,则平衡向移动(填“正反应方向”、“逆反应方向”或“不移动”)
(6)维持容器的体积不变,升高温度,达到新平衡时体系的颜色(填“变深”、“变浅”或“不变”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com