
【题目】有机物C常用于食品行业。已知9.0gC在足量O2中充分燃烧,将生成的混合气体依次通过足量的浓硫酸和碱石灰,分别增重5.4g和13.2g,经检验剩余气体为O2。
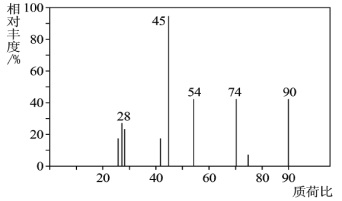
(1)C分子的质谱图如图所示,从图中可知其相对分子质量是__,则C的分子式是__。
(2)C能与NaHCO3溶液发生反应,C一定含有的官能团是__。
(3)C分子的核磁共振氢谱有4个峰,峰面积之比是1:1:1:3,则C的结构简式是__。
(4)0.1molC与1.0mol/L的氢氧化钠溶液反应,需溶液的体积是__mL。
【答案】90 C3H6O3 羧基(-COOH) CH3CH(OH)COOH 100 mL
【解析】
根据质谱仪的最大质荷比得相对分子质量,通过燃烧法确定实验式,最后可以确定结构简式;醇羟基没有酸性不能与氢氧化钠、碳酸钠、碳酸氢钠反应,可以与钠单质反应,羧基具有酸性,可以与钠、氢氧化钠、碳酸钠、碳酸氢钠反应。
(1)由质谱仪的最大质荷比可知C的相对分子质量为90,经过燃烧测定:0.1mol C在足量O2中充分燃烧,水的质量是5.4g,水的物质的量是0.3mol,氢元素物质的量为0.6mol;二氧化碳的质量13.2g,其物质的量为0.3mol,碳元素物质的量为0.3mol;9.0gC中含氧元素的质量=(9-0.6×1-0.3×12)g=4.8g,则氧元素的物质的量为0.3mol,n(C):n(H):n(O)=1:2:1,则实验式为CH2O,由于相对分子质量为90,则分子式为C3H6O3;
(2)根据分析,C能与NaHCO3溶液发生反应,C一定含有的官能团是羧基(-COOH);
(3)C分子的核磁共振氢谱有4个峰,峰面积之比是1:1:1:3,则分子有1个-CH3,1个-COOH,1个-OH,1个![]() ,则C的结构简式是CH3CH(OH)COOH;
,则C的结构简式是CH3CH(OH)COOH;
(4)C中的羟基不与氢氧化钠反应,羧基可以发生反应,故0.1molC会消耗0.1mol氢氧化钠反应,故所需氢氧化钠溶液的体积是![]() =0.1 L=100 mL。
=0.1 L=100 mL。


科目:高中化学 来源: 题型:
【题目】对-甲基苯甲酸乙酯(F)是有机化工原料,用于合成药物的中间体,某兴趣小组利用中学的简单有机物进行合成,其方案如下:
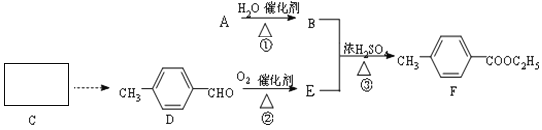
(1)A的结构简式是___________,E中含有的官能团名称是___________。
(2)指出化学反应类型:①___________;②______________。
(3)丁子香酚(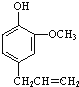 )是一种重要的调味剂,它与F的关系是____________。
)是一种重要的调味剂,它与F的关系是____________。
a.同系物 b.同分异构体 c.同种物质
(4)下列物质不能与丁子香酚发生反应的是___________。
a.NaOH溶液 b.NaHCO3溶液 c.Br2的四氯化碳溶液 d.乙醇
(5)写出反应③的化学方程式:______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2是目前大气中含量最高的一种温室气体,中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~50%。CO2的综合利用是解决温室问题的有效途径。
(1)研究表明CO2和H2在催化剂存在下可发生反应生成CH3OH。己知部分反应的热化学方程式如下:
CH3OH(g)+ ![]() O2(g) =CO2(g)+2H2O(1) △H1=akJmol-1
O2(g) =CO2(g)+2H2O(1) △H1=akJmol-1
H2(g)+![]() O2(g) =H2O(1) △H2=bkJmol-1
O2(g) =H2O(1) △H2=bkJmol-1
H2O(g) = H2O(l) △H3=ckJmol-1
则 CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H=__________kJmol-1
CH3OH(g)+H2O(g) △H=__________kJmol-1
(2)为研究CO2与CO之间的转化,让一定量的CO2与足量碳在体积可变的密闭容器中反应:C(s)+CO2(g)![]() 2CO(g)
2CO(g) ![]() H,反应达平衡后,测得压强、温度对CO的体积分数(φ(CO)%)的影响如图所示。
H,反应达平衡后,测得压强、温度对CO的体积分数(φ(CO)%)的影响如图所示。
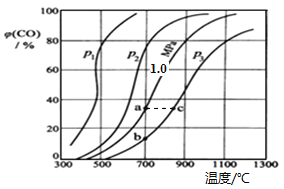
回答下列问题:
①压强p1、p2、p3的大小关系是________;Ka 、 Kb 、 Kc 为a、b、c三点对应的平衡常数,则其大小关系是_________。
②900℃、1.0 MPa时,足量碳与a molCO2反应达平衡后,CO2的转化率为___________ (保留三位有效数字),该反应的平衡常数Kp=_________(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
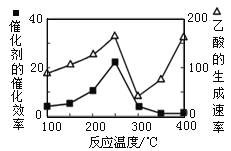
(3)① 以二氧化钛表面覆盖Cu2Al2O4 为催化剂,可以将CO2 和CH4 直接转化成乙酸,CO2(g)+CH4(g)![]() CH3COOH(g)。在不同温度下催化剂的催化效率与乙酸的生成速率如右图所示。250~300 ℃时,乙酸的生成速率降低的主要原因是_____________; 300~400℃时,乙酸的生成速率升高的主要原因是___________。
CH3COOH(g)。在不同温度下催化剂的催化效率与乙酸的生成速率如右图所示。250~300 ℃时,乙酸的生成速率降低的主要原因是_____________; 300~400℃时,乙酸的生成速率升高的主要原因是___________。
② 为了提高该反应中CO2的转化率,可以采取的措施是_____(写一条即可)。
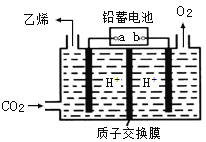
(4)以铅蓄电池为电源可将CO2转化为乙烯,其原理如图所示,电解所用电极材料均为惰性电极。阴极上的电极反应式为___________;每生成0.5mol乙烯,理论上需消耗铅蓄电池中_____mol硫酸。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO和H2在一定条件下可以合成乙醇(CH3CH2OH):2CO(g)+4H2(g) ![]() CH3CH2OH(g)+H2O(g),下列叙述中能说明上述反应在一定条件下已达到最大限度的是( )
CH3CH2OH(g)+H2O(g),下列叙述中能说明上述反应在一定条件下已达到最大限度的是( )
A. CO全部转化为乙醇
B. 正反应和逆反应的化学反应速率均为零
C. 反应体系中乙醇的物质的量浓度不再变化
D. CO和H2以1:2的物质的量之比反应生成乙醇
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答下列问题:
(1)烃A的结构简式为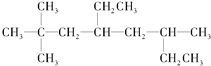 ,用系统命名法命名烃A:__。
,用系统命名法命名烃A:__。
(2)某烃的分子式为C5H12,核磁共振氢谱图中显示4个峰,则该烃的一氯代物有__种,该烃的结构简式为__。
(3)麻黄素又称黄碱,是我国特定中药材麻黄中所含有的一种生物碱。经科学家研究发现其结构为: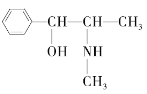 ,下列各物质:
,下列各物质:
A.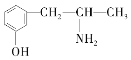 B.
B.![]() C.
C.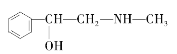 D.
D.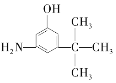 E.
E.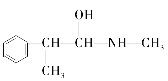
与麻黄素互为同分异构体的是__(填字母,下同),互为同系物的是__(填字母)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是 ( )
A. 甲苯既可使溴的CCl4溶液褪色,也可使KMnO4酸性溶液褪色
B. 有机物![]() 的消去产物有2种
的消去产物有2种
C. 有机物A(C4H6O2)能发生加聚反应,可推知A的结构一定是CH2===CH—COOCH3
D. 可用溴水鉴别直馏汽油、四氯化碳和乙酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】足量铜与一定量的浓硝酸反应,得到硝酸铜溶液和NO2、NO的混合气体,这些气体与1.68L O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入6molL﹣1NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是( )
A.60 mLB.45 mLC.30 mLD.50 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了证明在实验室制备得到的Cl2中会混有HCl,甲同学设计了如图所示的实验装置,按要求回答下列问题。

(1)请根据甲同学的示意图,所需实验装置从左至右的连接顺序:装置②→__________。
(2)装置②中主要玻璃仪器的名称__________、__________、__________。
(3)实验室制备Cl2的离子方程式为____________。
(4)装置③中Cu的作用__________(用化学方程式表示)。
(5)乙同学认为甲同学实验设计仍然存在缺陷,不能证明最终通入AgNO3溶液中的气体只有一种。为此,乙同学提出气体通入装置①之前,要加装一个检验装置⑤,以证明最终通入AgNO3溶液中的气体只有一种。你认为装置⑤应放入__________。
(6)丙同学看到甲同学设计的装置后提出无需多加装置,只需将原来烧杯中的AgNO3溶液换成紫色石蕊试液,如果观察到__________的现象,则证明制Cl2时有HCl挥发出来。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢原子是最轻的原子,人们曾预言它可能是所有元素之母。碳是地球上组成生命的最基本的 元素之一。按要求回答:
(1)宇宙中含量最多的元素是氢和______。基态碳原子的核外电子占有______个原子轨道。
(2)光化学烟雾中除了含有 NOx 外,还含有 HCOOH、![]() (PAN)等二次污染物。
(PAN)等二次污染物。
①PAN 中 C 的杂化方式有______。1mol PAN 中含有的σ键数目为______。组成PAN 的元素的电负性大小顺序为______。
②相同压强下,HCOOH 的沸点比 CH3OCH3______(填“高”或“低”),
(3)水溶液中有 H3O+、H5O2+ 、H9O4 + 等微粒的形式。请画出 H5O2 的结构式:______。
(4)硅和碳在同一主族。下图为 SiO2 晶胞中 Si 原子沿 z 轴方向在 xy 平面的投影图(即俯视图),其 中 O原子略去,Si 原子旁标注的数字表示每个 Si 原子位于 z 轴的高度,则 SiA 与 SiB 之间的距离是______nm。
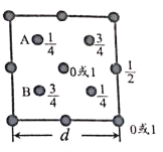 (d 的单位为 nm)
(d 的单位为 nm)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com