

| 1 |
| 2 |
| 0.2mol |
| 2L |
| 1 |
| 2 |
| 0.2mol |
| 4 |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
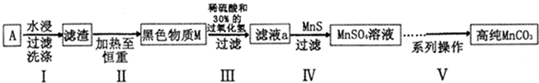
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
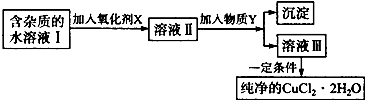
| Fe3+ | Fe+ | Cu+ | |
| �������↑ʼ����ʱp | 1.9 | 7.0 | 4.7 |
| ����������ȫ����ʱp | 3.2 | 9.0 | 6.7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
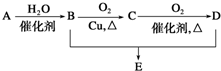 �л���A�IJ����Ǻ���һ������ʯ��ҵ��չˮƽ�ı�־���ɷ�������ϵ��ת����B��D�������г����������л������˵������ȷ���ǣ�������
�л���A�IJ����Ǻ���һ������ʯ��ҵ��չˮƽ�ı�־���ɷ�������ϵ��ת����B��D�������г����������л������˵������ȷ���ǣ�������| A��A�Ľṹ��ʽΪCH2=CH2 |
| B��1molB���ʿ���������Na��Ӧ����0.5molH2 |
| C��B��D��E�������ʿ����ñ���Na2CO3��Һ���� |
| D����B��D�Ʊ�EŨH2SO4ֻ����ˮ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
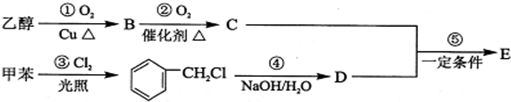
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ���� T/��n/mol T/�� | NO | CO | E | F |
| ��ʼ | 0.100 | 0.100 | 0 | 0 |
| T1 | 0.020 | 0.020 | 0.080 | 0.040 |
| T2 | 0.010 | 0.010 | 0.090 | 0.045 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
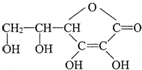 ά����C�Ľṹ��ʽ��ͼ�����ķ���ʽ��
ά����C�Ľṹ��ʽ��ͼ�����ķ���ʽ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com