
【题目】氮的氧化物和硫的氧化物是主要的大气污染物,烟气脱硫脱硝是环境治理的热点问题。回答下列问题:
(1)目前柴油汽车都用尿素水解液消除汽车尾气中的NO,水解液中的NH3将NO还原为无害的物质。该反应中氧化剂与还原剂物质的量之比为___。
(2)KMnO4/CaCO3浆液可协同脱硫,在反应中MnO4-被还原为MnO42-。
①KMnO4脱硫(SO2)的离子方程式为___。
②加入CaCO3的作用是___。
③KMnO4/CaCO3浆液中KMnO4与CaCO3最合适的物质的量之比为___。
(3)利用NaClO2/H2O2酸性复合吸收剂可同时对NO、SO2进行氧化得到硝酸和硫酸而除去。在温度一定时,n(H2O2)/n(NaClO2)、溶液pH对脱硫脱硝的影响如图所示:
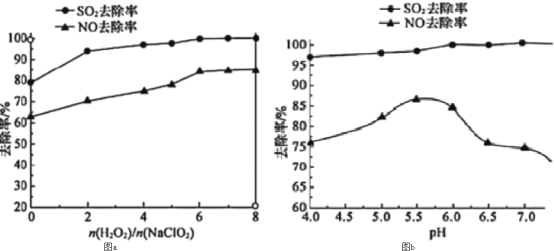
图a和图b中可知脱硫脱硝最佳条件是___。图b中SO2的去除率随pH的增大而增大,而NO的去除率在pH>5.5时反而减小,请解释NO去除率减小的可能原因是___。
【答案】2:3 SO2 +2MnO4-+2H2O === SO42- + 2MnO42- + 4H+ 消耗脱硫过程中的氢离子,有利于平衡正向移动 1:1 n(H2O2):n(NaClO2) = 6:1,pH值在5.5—6.0 可能NO的还原性减弱或则可能是NaClO2、H2O2的氧化性减弱
【解析】
⑴根据氧化还原反应得出氧化剂和还原剂的比例关系。
⑵根据氧化还原反应原理写离子方程式,生成的氢离子和碳酸钙反应,消耗氢离子,利于平衡正向移动,根据比例关系得出高锰酸钾和碳酸钙的比例。
⑶根据图像信息得出脱硫脱硝最佳条件,用氧化还原反应的强弱随pH变化的影响分析减弱的原因。
⑴水解液中的NH3将NO还原为无害的物质氮气,根据氧化还原反应原理,氨气化合价升高3个价态,为还原剂,NO化合价降低2个价态,为氧化剂,根据升降守恒配平原理,因此氨气前配2,NO前面配系数3,因此该反应中氧化剂与还原剂物质的量之比为2:3,故答案为:2:3。
⑵①KMnO4脱硫(SO2)反应生成锰酸根和硫酸根,离子方程式为SO2 +2MnO4-+2H2O === SO42- + 2MnO42- + 4H+,故答案为:SO2 +2MnO4-+2H2O === SO42- + 2MnO42- + 4H+。
②反应过程中生成了硫酸,加入CaCO3的作用是消耗脱硫过程中的氢离子,有利于平衡正向移动,故答案为:消耗脱硫过程中的氢离子,有利于平衡正向移动。
③2molKMnO4反应生成4mol氢离子,4mol氢离子消耗2mol碳酸钙,因此CaCO3浆液中KMnO4与CaCO3最合适的物质的量之比为1:1,故答案为1:1。
⑶根据图中的转化率和去除率关系,可知脱硫脱硝最佳条件是n(H2O2):n(NaClO2) = 6:1,pH值在5.5—6.0;NO在pH>5.5时可能NO的还原性减弱或则可能是NaClO2、H2O2的氧化性减弱,故答案为:n(H2O2):n(NaClO2) = 6:1,pH值在5.5—6.0;可能NO的还原性减弱或则可能是NaClO2、H2O2的氧化性减弱。


科目:高中化学 来源: 题型:
【题目】根据下列图示所得出的结论正确的是( )
甲 乙
乙
丙 丁
丁
A. 图甲是在不同温度下三个恒容容器中反应2H2(g)+CO(g)CH3OH(g) ΔH<0的平衡曲线,曲线X对应的温度相对较高
B. 图乙是一定温度下三种碳酸盐MCO3(M:Mg2+、Ca2+、Mn2+)的沉淀溶解平衡曲线,a点可表示MgCO3的不饱和溶液,且c(Mg2+)<c(CO32-)
C. 图丙为MOH和ROH两种一元碱水溶液在常温下分别加水稀释时pH的变化曲线,可知ROH是强碱
D. 图丁为两个容器中在不同的压强下各投入1 mol CH4和1 mol CO2所发生反应CH4(g)+CO2(g)2CO(g)+2H2(g)的平衡曲线,N点化学平衡常数K=1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下列各装置图的叙述中,正确的是
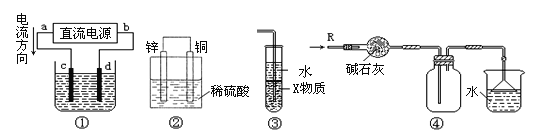
A. 若采用装置①精炼铜,则d极为粗铜,c极为纯铜,电解质溶液为CuSO4溶液
B. 装置②是原电池,能将化学能转化为电能,锌电极发生还原反应
C. 装置③中X若为四氯化碳,可用于吸收氨气或氯化氢,并防止倒吸
D. 装置④可用于收集氨气,并吸收多余的氨气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某化学反应A2(g)+2B2(g)=2AB2(g) (A2、B2、AB2的结构式分别为A=A、B-B、B-A-B),能量变化如图所示,下列有关叙述中正确的是
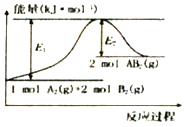
A. 该反应若生成2molAB2(g)则吸收的热量为(El-E2)kJ
B. 该反应的进行一定需要加热或点燃条件
C. 该反应断开化学键消耗的总能量小于形成化学键释放的总能量
D. 生成2molB-B键放出E2kJ能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己知H2O2在催化剂作用下分解速率加快,其能量随反应进程的变化如图所示。下列说法正确的是

A. H2O2分解属于吸热反应
B. 加入催化剂,减小了反应的热效应
C. 加入催化剂,可提高正反应的活化能
D. 反应物的总能量高于生成物的总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】还原沉淀法是处理含铬![]() 和
和![]() 废水常用方法,过程如下:CrO42-
废水常用方法,过程如下:CrO42-![]()
Cr2O72-![]() Cr3+
Cr3+![]() Cr(OH)3 ,已知废水中Cr的含量为
Cr(OH)3 ,已知废水中Cr的含量为![]() ,当溶液中离子浓度小于
,当溶液中离子浓度小于![]() 时认为离子已经沉淀完全,常温下,
时认为离子已经沉淀完全,常温下,![]() 有关叙述中不正确的是
有关叙述中不正确的是
A.上述三个转化中只有一个涉及氧化还原反应
B.第二步离子方程式为:![]()
C.处理含铬废水可使用强碱![]() ,也可以使用弱碱氨水
,也可以使用弱碱氨水
D.当![]() 时,废水中铬元素沉淀完全
时,废水中铬元素沉淀完全
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式中ΔH能表示可燃物燃烧热的是( )
A.2H2(g) + O2(g) = 2H2O(g) ΔH= -483.6kJ·mol-1
B.CO(g) +![]() O2(g) = CO2(g) ΔH= -283kJ·mol-1
O2(g) = CO2(g) ΔH= -283kJ·mol-1
C.CH4(g) + 2O2(g) = CO2(g) +2H2O(g) ΔH= -802kJ·mol-1
D.C(s) +![]() O2(g) = CO(g) ΔH= -108kJ·mol-1
O2(g) = CO(g) ΔH= -108kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表中实验操作、现象以及所得出的结论都正确的是![]()
选项 | 实验操作 | 实验现象 | 实验结论 |
A | 向盛有 | 先出现白色沉淀,后出现黄色沉淀 |
|
B | 将适量 | 一支试管出现白色沉淀,另一支试管无明显现象 | 出现的白色沉淀是 |
C | 取少量 | 产生白色沉淀 |
|
D | 湿润的KI淀粉试纸靠近气体Y | 试纸变蓝 | Y可能是 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,下列有关溶液中微粒的物质的量浓度关系正确的是 ( )
A.0.1 mol/LNa2CO3的溶液中:c(![]() )=2c(H2CO3)+c(H+)- c(OH-)
)=2c(H2CO3)+c(H+)- c(OH-)
B.物质的量浓度之比为1:2的NaClO、NaHCO3混合溶液中:c(HClO)+c(ClO-)=2c(![]() )+2c(
)+2c(![]() )+2c(H2CO3)
)+2c(H2CO3)
C.向3.0 L 0.1 mol·L-1 NaOH溶液中缓慢通入CO2至溶液增重8.8 g时,溶液中: c(Na+)>c(![]() )>c(
)>c(![]() )>c(OH-)>c(H+)
)>c(OH-)>c(H+)
D.等物质的量的CH3COOH、CH3COONa混合溶液pH=4.75中:c(CH3COO-)+c(OH-)>c(CH3COOH)+c(H+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com