
【题目】CO2是一种常用的化工原料。
Ⅰ.以CO2与NH3为原料可以合成尿素[CO(NH2)2]。合成尿素的反应为2NH3(g)+CO2(g)![]() CO(NH2)2(s)+H2O(g)。
CO(NH2)2(s)+H2O(g)。
(1)在不同温度及不同y值下合成尿素,达到平衡时,氨气转化率变化情况如图所示。该反应的ΔH_____0(填“>”、“<”或“=”,下同),若y表示压强,则y1_______y2 , 若y表示反应开始时的水碳比[n(NH3)/n(CO2)],则y1_______y2。

(2)t℃时,若向容积为2L的密闭容器中加入3molNH3和1molCO2,达到平衡时,容器内压强为开始时的0.75倍。若保持条件不变,再向该容器中加入0.5molCO2和1molH2O,NH3的转化率将__________(填“增大”、“减小”或“不变”)。
Ⅱ.CO2与H2反应可用于生产甲醇。
(3)已知氢气与甲醇的燃烧热分别为-285.8 kJ·mol-1、-726.5kJ·mol-1,则CO2与H2反应产生液态甲醇与液态水的热化学方程式为________________。
(4)下图是某甲醇燃料电池工作的示意图。质子交换膜(只有质子能够通过)左右两侧的溶液均为1L 2mol·L-1 H2SO4溶液。电极a上发生的电极反应式为________________________,当电池中有1mol e-发生转移时左右两侧溶液的质量之差为______g (假设反应物耗尽,忽略气体的溶解)。

【答案】< > < 减小 CO2(g) +3H2(g)=CH3OH(l) +H2O(l) △H=-130.9kJ/mol CH3OH +H2O-6e- =CO2+6H+ 12
【解析】
Ⅰ.(1)根据图示,升高温度,NH3转化率减小,平衡逆向移动;2NH3(g)+CO2(g)![]() CO(NH2)2(s)+H2O(g),正反应气体物质的量减小,加压平衡正向移动,氨气的转化率增大;增大NH3的浓度,NH3的转化率减小;(2)利用“三段式”计算平衡常数,根据
CO(NH2)2(s)+H2O(g),正反应气体物质的量减小,加压平衡正向移动,氨气的转化率增大;增大NH3的浓度,NH3的转化率减小;(2)利用“三段式”计算平衡常数,根据![]() 的关系判断平衡移动方向;Ⅱ.(3)由H2(g)和甲醇的燃烧热分别为285.8 kJ·mol-1、726.5kJ·mol-1,可知二者燃烧的热方程式分别为:H2(g)+1/2O2(g)=H20(l) ΔH=-285.8 kJ/mol ①;CH3OH (l)+3/2O2(g)=CO2(g)+2H20(l) ΔH=-726.5kJ·mol-1 ②,根据盖斯定律书写CO2与H2反应产生液态甲醇与液态水的热化学方程式;(4)电极a是负极,甲醇失电子生成二氧化碳和氢离子;当电池中有1mol e-发生转移时,a极消耗
的关系判断平衡移动方向;Ⅱ.(3)由H2(g)和甲醇的燃烧热分别为285.8 kJ·mol-1、726.5kJ·mol-1,可知二者燃烧的热方程式分别为:H2(g)+1/2O2(g)=H20(l) ΔH=-285.8 kJ/mol ①;CH3OH (l)+3/2O2(g)=CO2(g)+2H20(l) ΔH=-726.5kJ·mol-1 ②,根据盖斯定律书写CO2与H2反应产生液态甲醇与液态水的热化学方程式;(4)电极a是负极,甲醇失电子生成二氧化碳和氢离子;当电池中有1mol e-发生转移时,a极消耗![]() mol水,b极生成0.5mol水。
mol水,b极生成0.5mol水。
Ⅰ.(1)根据图示,升高温度,NH3转化率减小,平衡逆向移动,所以正反应放热,ΔH<0;2NH3(g)+CO2(g)![]() CO(NH2)2(s)+H2O(g),正反应气体物质的量减小,加压平衡正向移动,氨气的转化率增大;同温下,压强为y1时氨气转化率大于y2,所以y1>y2;增大NH3的浓度,NH3的转化率减小,水碳比[n(NH3)/n(CO2)]为y1时氨气转化率大于y2,所以y1<y2;
CO(NH2)2(s)+H2O(g),正反应气体物质的量减小,加压平衡正向移动,氨气的转化率增大;同温下,压强为y1时氨气转化率大于y2,所以y1>y2;增大NH3的浓度,NH3的转化率减小,水碳比[n(NH3)/n(CO2)]为y1时氨气转化率大于y2,所以y1<y2;
(2)2NH3(g)+CO2(g)![]() CO(NH2)2(s)+H2O(g)
CO(NH2)2(s)+H2O(g)
开始 1.5 0.5 0
转化 2x x x
平衡 1.5-2x 0.5-x x
![]()
x=0.25
K=![]() ,再向该容器中加入0.5molCO2和1molH2O,
,再向该容器中加入0.5molCO2和1molH2O,![]() >K,平衡逆向移动,NH3的转化率将减小;
>K,平衡逆向移动,NH3的转化率将减小;
Ⅱ.(3)由H2(g)和甲醇的燃烧热分别为285.8 kJ·mol-1、726.5kJ·mol-1可知,二者燃烧的方程式分别为:H2(g)+1/2O2(g)=H20(l) ΔH=-285.8 kJ/mol ①;CH3OH (l)+3/2O2(g)=CO2(g)+2H20(l) ΔH=-726.5kJ·mol-1 ②,根据盖斯定律①×3-②得CO2(g) +3H2(g)=CH3OH(l) +H2O(l) △H=-130.9kJ/mol;
(4)电极a是负极,甲醇失电子生成二氧化碳和氢离子,电极a上发生的电极反应式为CH3OH +H2O-6e- =CO2+6H+;当电池中有1mol e-发生转移时,a极消耗![]() mol水,b极生成0.5mol水,所以左右两侧溶液的质量之差为12g。
mol水,b极生成0.5mol水,所以左右两侧溶液的质量之差为12g。


科目:高中化学 来源: 题型:
【题目】在恒温恒压下,向密闭容器中充入4 mol SO2和2 mol O2,发生如下反应:2SO2(g)+O2(g)![]() 2SO3(g) ΔH<0,2min后,反应达到平衡,生成SO3为1.4 mol,同时放出热量Q kJ。则下列分析正确的是( )
2SO3(g) ΔH<0,2min后,反应达到平衡,生成SO3为1.4 mol,同时放出热量Q kJ。则下列分析正确的是( )
A. 在该条件下,反应前后的压强之比为6∶5.3
B. 若反应开始时容器体积为2 L,则v(SO3)=0.35 mol/(L·min)
C. 若把“恒温恒压下”改为“恒压绝热条件下”反应,平衡后n(SO3)<1.4 mol
D. 若把“恒温恒压下”改为“恒温恒容下”反应,达平衡时放出热量大于Q kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种Cu-Li可充电电池的工作原理如图所示,其中非水系电解液和水系电解液被锂离子固体电解质陶瓷片(LISICON)隔开。下列说法正确的是
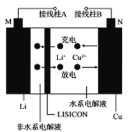
A. 陶瓷片允许水分子通过
B. 电池放电时,N极上发生氧化反应
C. 电池充电时,接线柱B应与外接直流电源的正极相连
D. 电池充电时,阳极反应为Li++e-=Li
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2 L密闭容器中,800 ℃时,反应2NO+O2![]() 2NO2体系中,n(NO)随时间的变化如下表:
2NO2体系中,n(NO)随时间的变化如下表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)如图表示各物质浓度的变化曲线,
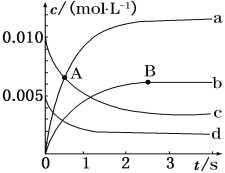
A点处,v(正)___________v(逆), A点正反应速率_________B点正反应速率。 (用“大于”、“小于”或“等于”填空)
(2)图中表示O2变化的曲线是___________。用NO2表示从0~2 s内该反应的平均速率v=____________________________。
(3) 能使该反应的反应速率增大的是____________。
A.及时分离出NO2气体 B.升高温度
C.减小O2的浓度 D.选择高效的催化剂
(4) 能说明该反应已经达到平衡状态的是___________。
A.容器内压强保持不变 B.v(NO)=2v(O2)
C.容器内的密度保持不变 D.v逆(NO2)=2v正(O2)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NH3催化还原NO是重要的烟气脱硝技术,其反应过程与能量关系如图;研究发现在以Fe2O3为主的催化剂上可能发生的反应过程如下图,下列说法正确的是( )

A. 脱硝的总反应为:4NH3(g)+4NO(g)+O2(g)![]() 4N2(g)+6H2O(g)
4N2(g)+6H2O(g)
B. NH3催化还原NO为吸热反应
C. 过程1中NH3断裂非极性键
D. 过程中NO为氧化剂,Fe2+为还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示A处通入潮湿的Cl2,关闭活塞B时D中干燥的红色布条颜色无变化;打开活塞B时D处干燥的红色布条褪色,则C中的试剂(足量)不可能是
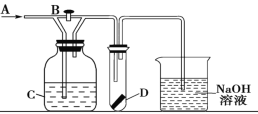
A.饱和氯化钠溶液B.氢氧化钙悬浊液C.饱和碳酸钠溶液D.浓硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列方程式书写正确的是( )
A. NaHSO4在水溶液中的电离方程式:NaHSO4===Na++HSO4-
B. HF与NaOH溶液反应:H+(aq)+OH-(aq) = H2O(l) ΔH=-57.3 kJ/mol
C. 1g H2燃烧生成液态水放出142.9 kJ的热量,其热化学方程式:2H2(g)+ O 2(g) = 2H2O (l) ΔH = —142.9 kJ·mol-1
D. CaCO3沉淀溶解平衡方程式:CaCO3(s) ![]() Ca2+(aq)+CO32-(aq)
Ca2+(aq)+CO32-(aq)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某个体小煤矿曾发生瓦斯爆炸事故,造成人员伤亡。在煤矿矿井里,必须采取安全措施,如通风、严禁烟火等,而且要随时检查瓦斯的体积分数,如果空气中含甲烷的体积分数为5%~15.4%,遇到明火会发生爆炸。发生最强烈爆炸时空气中甲烷所占的体积分数约是
A. 5% B. 9.1% C. 10.5% D. 15%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以A(C2H2)为原料合成食用香料E和吡咯(pyrrole)的路线如图所示,部分反应条件及产物略去。其中D在一定条件下可被氧化成酮。
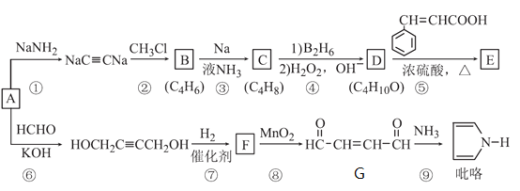
回答下列问题:
(1)A的官能团名称是_______________;C的名称是_______________;
(2)⑥的反应类型是_______________。⑧的反应类型是_______________。
(3)反应⑤的化学方程式为____________________________。
(4)满足下列条件的肉桂酸(![]() )的同分异构体共有_________种(不考虑立体异构):①含有苯环 ②能让溴的四氯化碳溶液褪色 ③能水解。与G互为同分异构体,且核磁共振氢谱只有一组峰的有机物的结构简式是________。(任写一种)
)的同分异构体共有_________种(不考虑立体异构):①含有苯环 ②能让溴的四氯化碳溶液褪色 ③能水解。与G互为同分异构体,且核磁共振氢谱只有一组峰的有机物的结构简式是________。(任写一种)
(6)参照上述合成路线,设计一条由A和乙醛为起始原料制备2,5-二甲基吡咯(![]() )的合成路线_________________________________。
)的合成路线_________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com