
【题目】如图所示,某同学设计了一个燃料电池并探究氯碱工业原理的相关问题,其中乙装置中X为阳离子交换膜。请按要求回答相关问题:

(1)石墨电极(C)作___极,丙池中滴有酚酞,实验开始后观察到的现象是_____,甲中甲烷燃料电池的负极反应式为________。
(2)若消耗2.24 L(标况)氧气,则乙装置中铁电极上生成的气体体积(标况)为___ L。
(3)丙中以CuSO4溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的是_______。
A.b电极为粗铜
B.粗铜接电源正极,发生还原反应
C.CuSO4溶液的浓度保持不变
D.利用阳极泥可回收Ag、Pt、Au等金属
(4)若丙中以稀H2SO4为电解质溶液,电极材料b为铝,则能使铝表面生成一层致密的氧化膜,该电极反应式为__________。
(5)假设乙装置中氯化钠溶液足够多,若在标准状况下,有224 mL氧气参加反应,则乙装置中阳离子交换膜,左侧溶液质量将_______,(填“增大”“减小”或“不变”),且变化了_____克。
【答案】阳 两电极均有气泡冒出,左边a电极附近溶液变红 CH4+10OH--8e-=CO32-+7H2O 4.48 AD 2Al+3H2O-6e-=Al2O3+6H+ 增大 0.88
【解析】
在燃料电池中,投放燃料的电极是负极,投放氧化剂的电极是正极。在甲池中通入O2的Pt电极为正极,通入CH4的Pt电极为负极。
(1)与原电池负极相连的为电解池的阴极,与正极相连的电极为阳极,阳极发生氧化反应,阴极发生还原反应,据此分析实验现象;
(2)根据串联电路中转移电子数相等计算铁电极上生成氢气的体积;
(3)铜的精炼时,粗铜为阳极,纯铜为阴极,阳极上Cu以及活泼性比Cu强的金属失电子,阴极上铜离子得电子生成Cu;
(4)电极材料b为铝,b为阳极,Al失电子生成氧化铝;
(5)根据氧气的体积计算氧气的物质的量,然后计算电子转移的物质的量,结合同一闭合回路中电子转移数目相等,Fe电极上H+变为H2,C电极上Cl-变为Cl2,乙池中,乙装置中是阳离子交换膜,只允许Na+通过,根据Na+带一个单位正电荷,其物质的量与电子转移的物质的量相等,通过比较增加与减少的质量,确定左侧质量变化情况。
(1)甲池中通入燃料CH4的电极为负极,通入O2的电极为正极,根据图示可知乙池中Fe电极连接电源负极为阴极,石墨电极(C)连接电源正极,作阳极;
在丙池中滴有酚酞,a电极为阴极,发生反应:2H++2e-=H2↑,H+不断放电,破坏了附近溶液中H2O的电离平衡,最终达到平衡时,溶液中c(OH-)>c(H+),溶液显碱性,使酚酞试液变为红色;b电极为阳极,发生氧化反应:4OH--4e-=2H2O+O2↑,因此丙池实验开始后观察到的现象是:两电极均有气泡冒出,左边a电极附近溶液变红;
在燃料电池甲中,负极上CH4失电子发生氧化反应,与溶液中OH-结合形成CO32-,负极的因此负极的电极反应式为:CH4+10OH--8e-=CO32-+7H2O;
(2)串联电池中转移电子数相等,若在标准状况下,有2.24 L氧气参加反应,则转移电子的物质的量n(e-)=![]() ×4=0.4 mol,乙装置中铁电极上H+放电生成H2,每产生1 mol H2,转移2 mol电子,则转移0.4 mol电子时产生H2的物质的量为n(H2)=
×4=0.4 mol,乙装置中铁电极上H+放电生成H2,每产生1 mol H2,转移2 mol电子,则转移0.4 mol电子时产生H2的物质的量为n(H2)=![]() =0.2 mol,试液反应产生H2在标准状况下的体积V(H2)=0.2 mol×22.4 L/mol=4.48 L;
=0.2 mol,试液反应产生H2在标准状况下的体积V(H2)=0.2 mol×22.4 L/mol=4.48 L;
(3)A.电解精炼铜,粗铜为阳极,与电源正极连接,精铜为阴极,与电源负极连接。a与负极相连为阴极,b电极连接电源正极为阳极,所以b电极材料为粗铜,A正确;
B.粗铜接电源正极,作阳极,阳极上发生氧化反应,B错误;
C.阳极上Cu以及活泼性比Cu强的金属失电子,阴极上铜离子得电子生成Cu,溶解的金属与析出的金属质量不相等,所以CuSO4溶液的浓度会改变,C错误;
D.粗铜为阳极,阳极上Ag、Pt、Au等活泼性比Cu弱的金属在阳极不反应,形成阳极泥,所以利用阳极泥可回收Ag、Pt、Au等金属,D正确;
故合理选项是AD;
(4)电极材料b为铝,b为阳极,Al失电子生成氧化铝,酸性条件下,能使阳极铝表面生成一层致密的氧化膜,则铝电极的电极方程式为:2Al+3H2O-6e-=Al2O3+6H+;
(5)n(O2)=![]() =0.01 mol,电子转移n(e-)=4n(O2)=0.04 mol,在乙池中,Fe电极为阴极,发生还原反应,电极反应式为:2H++2e-=H2↑,转移0.04 mol电子,放出H2的物质的量为0.02 mol,其质量m(H2)=0.02 mol×2 g/mol=0.04 g;由于乙装置中离子交换膜是阳离子交换膜,只允许阳离子Na+通过,左侧H+放电使溶液中阳离子减少,因此Na+由右侧向左侧通过, Na+带一个单位正电荷,转移0.04 mol电子,则左侧增加0.04 mol Na+,其质量是m(Na+)=0.04 mol×23 g/mol=0.92 g,由于左侧增加质量大于减少质量,因此左侧质量会增加,增加质量为△m=m(Na+)-m(H2)=0.92 g-0.04 g=0.88 g。
=0.01 mol,电子转移n(e-)=4n(O2)=0.04 mol,在乙池中,Fe电极为阴极,发生还原反应,电极反应式为:2H++2e-=H2↑,转移0.04 mol电子,放出H2的物质的量为0.02 mol,其质量m(H2)=0.02 mol×2 g/mol=0.04 g;由于乙装置中离子交换膜是阳离子交换膜,只允许阳离子Na+通过,左侧H+放电使溶液中阳离子减少,因此Na+由右侧向左侧通过, Na+带一个单位正电荷,转移0.04 mol电子,则左侧增加0.04 mol Na+,其质量是m(Na+)=0.04 mol×23 g/mol=0.92 g,由于左侧增加质量大于减少质量,因此左侧质量会增加,增加质量为△m=m(Na+)-m(H2)=0.92 g-0.04 g=0.88 g。


科目:高中化学 来源: 题型:
【题目】目前工业上利用甲烷催化裂解生产不含一氧化碳和二氧化碳的清洁氢气。该过程多用铁、钴和镍等过渡金属纳米催化剂:CH4(g)![]() C(s)+2H2(g),已知温度升高,甲烷的平衡转化率增大。下列有关说法不正确的是( )
C(s)+2H2(g),已知温度升高,甲烷的平衡转化率增大。下列有关说法不正确的是( )
A.甲烷裂解属于吸热反应
B.在反应体系中加催化剂,反应速率增大
C.增大体系压强,不能提高甲烷的转化率
D.在1500℃以上时,甲烷的转化率很高,但几乎得不到炭黑,是因为在高温下该反应为放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】LED产品的使用为城市增添色彩。如图是氢氧燃料电池驱动LED发光的一种装置示意图。下列有关叙述正确的是( )

A.该装置将化学能最终只转化为电能
B.b处为电池正极,发生还原反应
C.a处通入O2
D.通入O2的电极上发生的电极反应为O2+4H++4e-=2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学实验是学习理解化学知识的基础,它以其魅力和丰富的内涵在化学学习中发挥着独特的功能和作用。请回答下列问题:
实验室欲配制100mL1mol·L-1的Na2CO3溶液。
(1)配制上述溶液,下列没有用到的仪器是__(填标号)。
A.烧杯 B.大试管 C.胶头滴管 D.100mL容量瓶
(2)除上述仪器外,还一定用到的玻璃仪器是__。
(3)从下表中选择称量Na2CO3·10H2O固体所需要的仪器有__(填标号)。
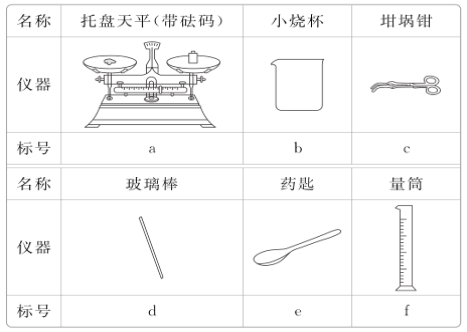
(4)下列情况使所配溶液的浓度如何变化?
①未洗涤溶解Na2CO3·10H2O的烧杯__(填“偏大”“偏小”或“不变”,后同)。
②容量瓶使用前用蒸馏水洗过,内壁附有水珠__。
③定容时加蒸馏水超过了刻度线,将多出的液体吸出__。
④定容时俯视容量瓶刻度线__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.PM2.5是指大气中直径≤2.5×10-6 m的颗粒物,则受PM2.5污染的大气定能产生丁达尔效应
B.根据电解质在水溶液中电离的程度,将电解质分为强电解质和弱电解质
C.黑火药的配方为“一硫二硝三木炭”,其中“硝”是指硝酸
D.![]() 、
、![]() 是制造氢弹的原料,它们是同一种核素
是制造氢弹的原料,它们是同一种核素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电化学原理在防止金属腐蚀、能量转换等方面应用广泛。
(1)①钢铁在海水中容易发生电化学腐蚀,正极反应式是__________。
②图中,为减缓钢闸门的腐蚀,材料B可以选择__________(填“Zn”或“Cu”)。
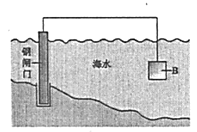
(2)如图为钢铁防护模拟实验装置,则铁做__________极,检测钢铁保护效果的方法是:取少量铁电极附近的溶液于试管中,_________,则说明保护效果好。

(3)氢氧燃料电池是一种新型的化学电源,其构造如图所示:

a、b为多孔石墨电极,通入的气体由孔隙中逸出,并在电极表面放电。
①a的电极反应式是_________;
②若电池共产生3.6g水,则电路中通过了_______mol的电子。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】东晋《华阳国志·南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)闻名中外,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
(1)镍元素基态原子的电子排布式为___,3d能级上的未成对电子数为___。
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。
①[Ni(NH3)6]SO4中阴离子的立体构型是___。
②在[Ni(NH3)6]2+中Ni2+与NH3之间形成的化学键称为___,提供孤电子对的成键原子是___。
③氨的沸点___(填“高于”或“低于”)膦(PH3),原因是___。
(3)单质铜及镍都是由___键形成的晶体;元素铜与镍的第二电离能分别为ICu=1958kJ·mol-1、INi=1753kJ·mol-1,ICu>INi的原因是___。
(4)某镍白铜合金的立方晶胞结构如图所示。
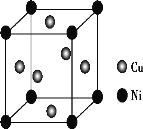
①晶胞中铜原子与镍原子的数量比为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某气态烷烃和气态单烯烃组成的混合气体,其密度是同条件下H2密度的13倍,把标准状况下2.24 L,该混合体通入足量的溴水中,溴水增重1.4 g。
(1)该混合烃的平均摩尔质量为________;其中一定含有________(写名称)。
(2)通过简计算,确定另一种烃的分子组成:_________。
(3)写出该混合烃中单烯烃所有可能的异构体(考虑顺反异构)任意写两种________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮族元素包括N、P、As、Sb和Bi五种元素。
(1)下列关于氮族元素的说法正确的是___。
a.N2可用于填充霓虹灯。其发光原理是电子从能量较低的轨道跃迁到能量较高的轨道,以光的形式释放能量
b.P、Na、S三种元素的第一电离能由大到小的顺序是:P>S>Na
c.基态As原子中,电子占据的最高能级为4d
d.Bi原子中最外层有5个能量相同的电子
(2)NH3在水中的溶解度比PH3大得多,其原因是___![]() 向硫酸铜溶液中加入过量氨水,然后加入适量乙醇,溶液中析出深蓝色的[Cu(NH3)4]SO4晶体。该晶体中含有的化学键除普通的共价键外,还有___和___。
向硫酸铜溶液中加入过量氨水,然后加入适量乙醇,溶液中析出深蓝色的[Cu(NH3)4]SO4晶体。该晶体中含有的化学键除普通的共价键外,还有___和___。
(3)PCl3分子中,Cl-P-Cl键的键角___109°28'(填“>”“<”或“2”![]() 。
。
(4)白磷(P4)是磷的一种单质,它属于分子晶体,其晶胞结构如图。已知该晶体的密度为ρg·cm-3,晶胞的边长为acm,则阿伏加德罗常数为___mol-1(用含p、a的式子表示![]() 。
。
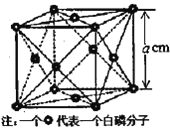
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com